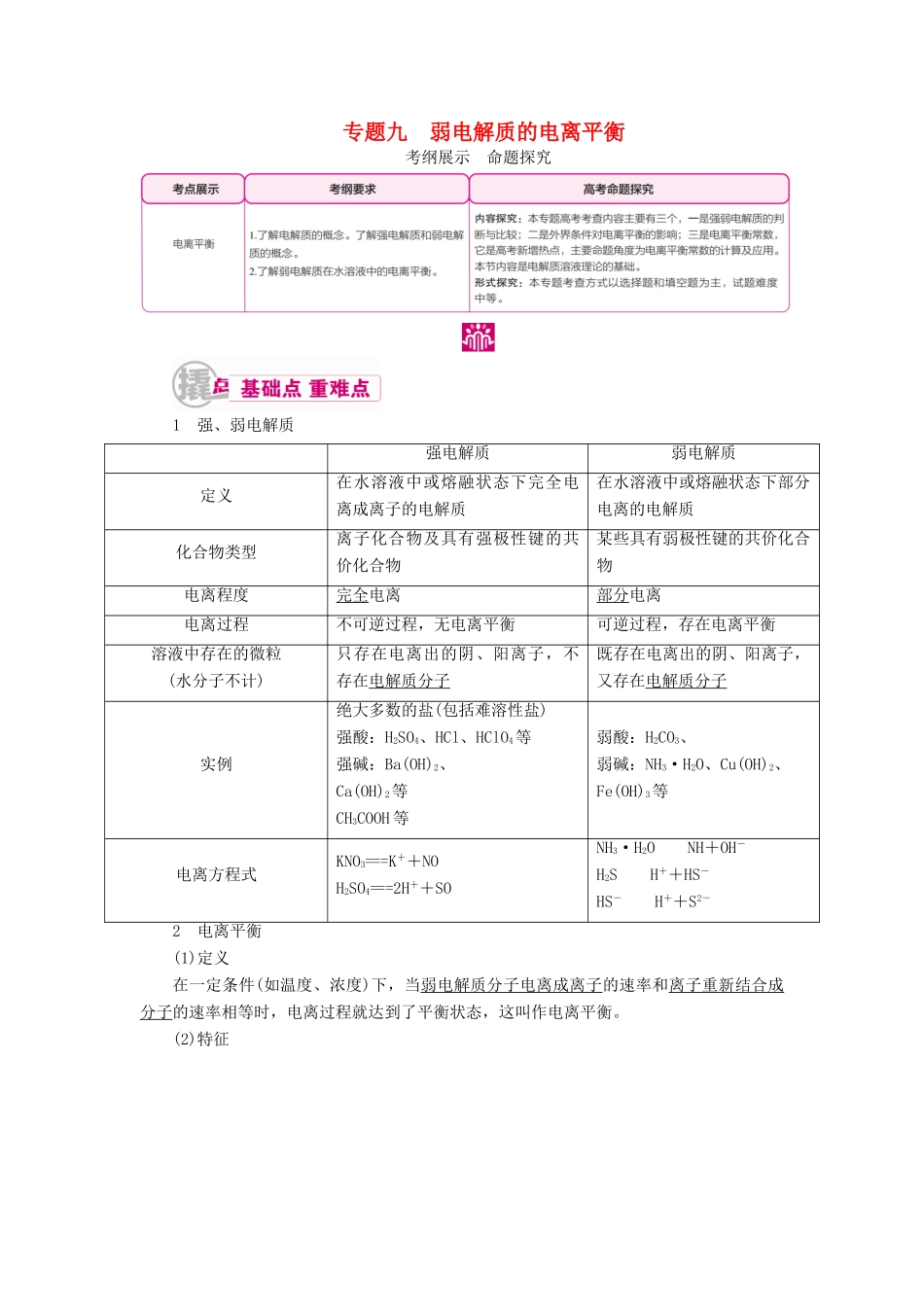
专题九 弱电解质的电离平衡考纲展示 命题探究1 强、弱电解质强电解质 弱电解质定义在水溶液中或熔融状态下完全电离成离子的电解质在水溶液中或熔融状态下部分电离的电解质化合物类型离子化合物及具有强极性键的共价化合物某些具有弱极性键的共价化合物 电离程度完全电离部分电离电离过程不可逆过程,无电离平衡可逆过程,存在电离平衡溶液中存在的微粒(水分子不计)只存在电离出的阴、阳离子,不存在电解质分子既存在电离出的阴、阳离子,又存在电解质分子实例绝大多数的盐(包括难溶性盐)强酸:H2SO4、HCl、HClO4等强碱:Ba(OH)2、Ca(OH)2等CH3COOH 等弱酸:H2CO3、弱碱:NH3·H2O、Cu(OH)2、Fe(OH)3等电离方程式KNO3===K++NOH2SO4===2H++SONH3·H2ONH+OH-H2SH++HS-HS-H++S2-2 电离平衡(1)定义在一定条件(如温度、浓度)下,当弱电解质分子电离成离子的速率和离子重新结合成分子的速率相等时,电离过程就达到了平衡状态,这叫作电离平衡
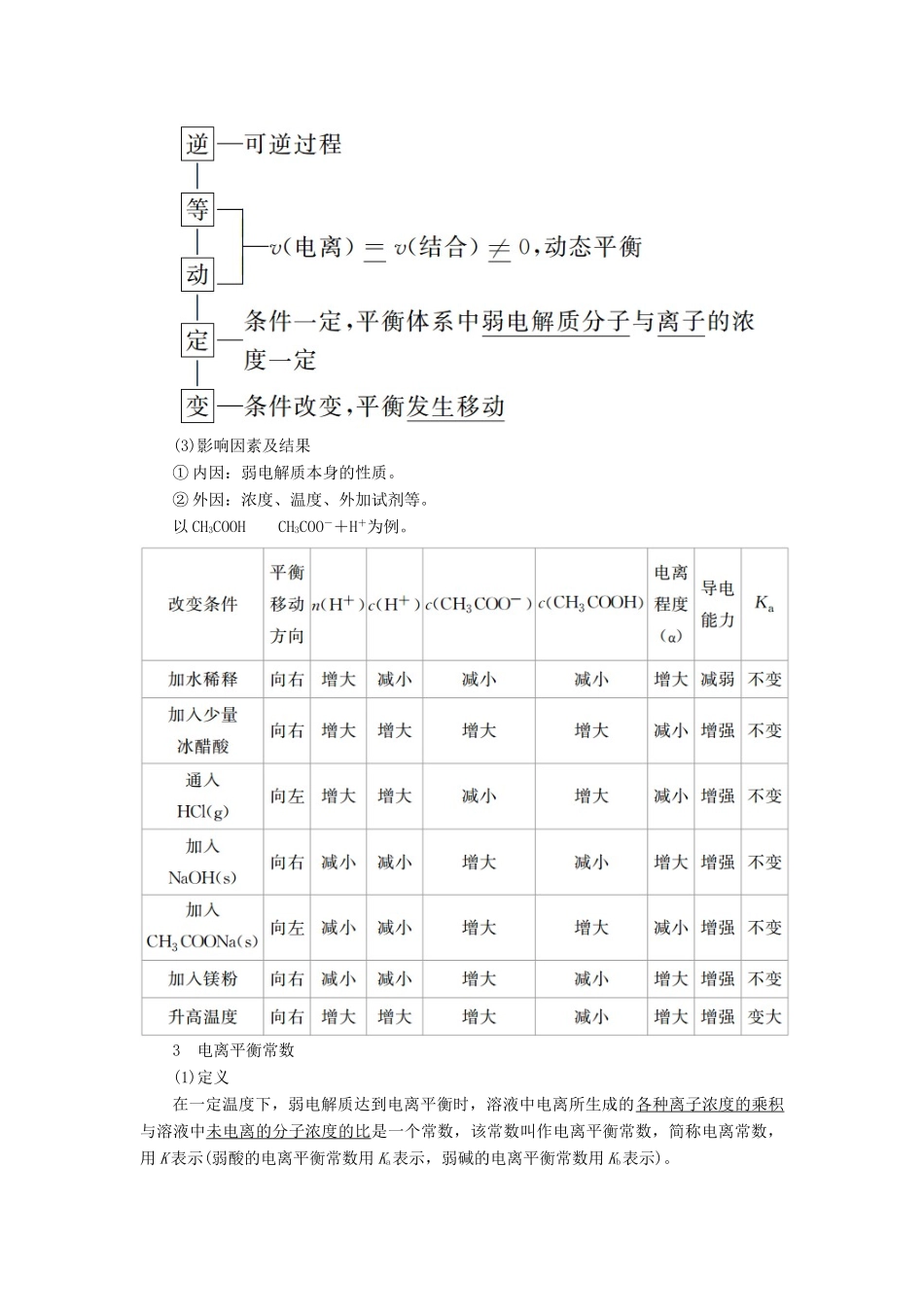
(2)特征(3)影响因素及结果① 内因:弱电解质本身的性质
② 外因:浓度、温度、外加试剂等
以 CH3COOHCH3COO-+H+为例
3 电离平衡常数(1)定义在一定温度下,弱电解质达到电离平衡时,溶液中电离所生成的各种离子浓度的乘积与溶液中未电离的分子浓度的比是一个常数,该常数叫作电离平衡常数,简称电离常数,用 K 表示(弱酸的电离平衡常数用 Ka表示,弱碱的电离平衡常数用 Kb表示)
(2)特征① 电离平衡常数② 多元弱酸是分步电离的,各级电离平衡常数的大小关系式是 K1≫ K 2≫ K 3……,所以多元弱酸的酸性决定于其第一步电离
学霸巧学卡 电解质强弱判断的注意事项(1)电解质的强弱与化学键没有必然联系,主要区别是其在水溶液中或熔融状态能否完全电离