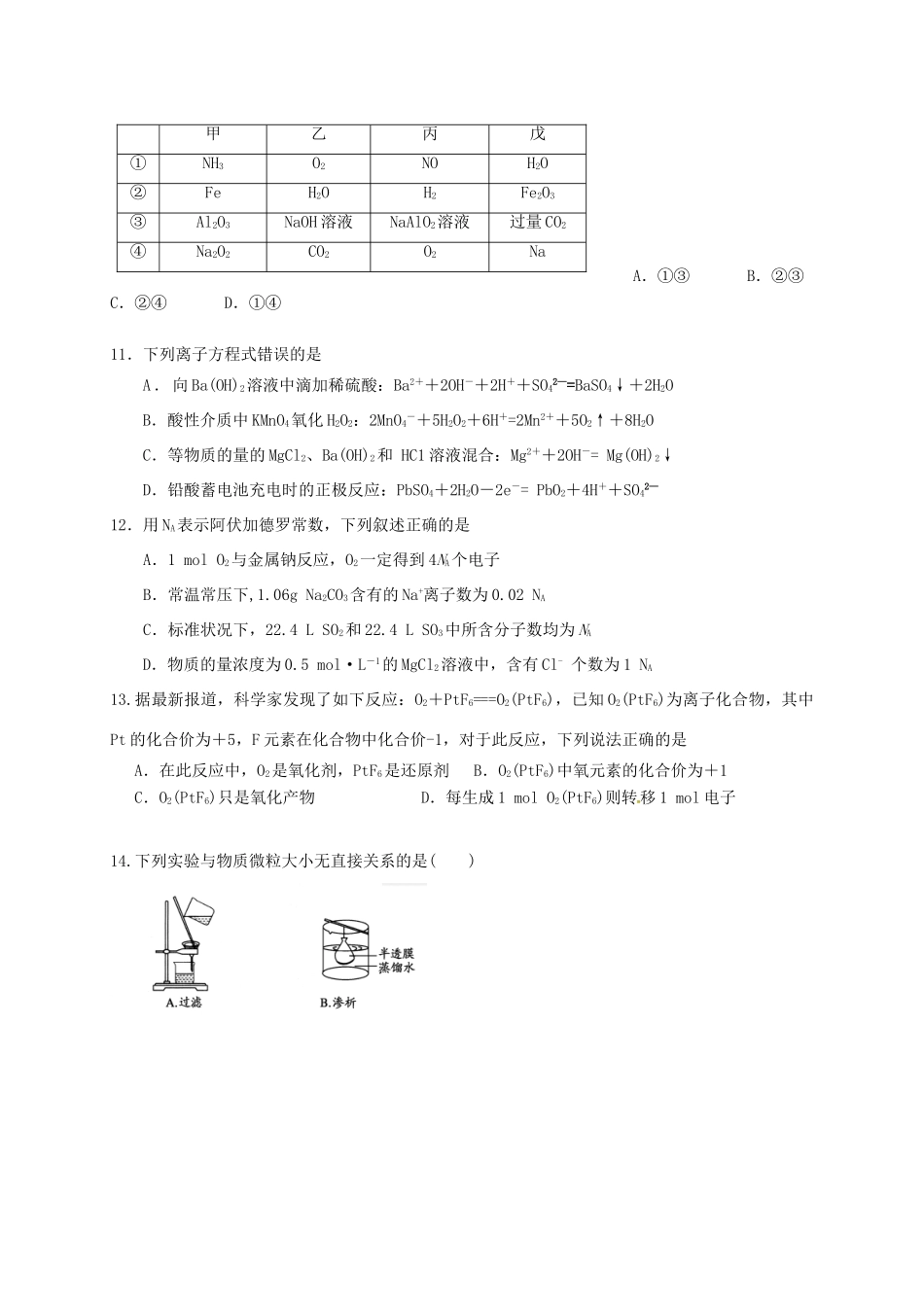
河南省太康县2016届高三化学上学期第二次考试试题考生须知1、满分为100分。考试时间90分钟。2、可能用到的相对原子量:H-1C-12N-14O-16F-19S-32Na-23Mg-24Al-27Cl-35.5Ba137I卷(共54分)一、单项选择题(本题包括18小题,每小题3分,共54分,每小题只有一个正确答案)1.下列说法正确的是A.非金属氧化物一定是非电解质。B.NOx、CO2、PM2.5颗粒都会导致酸雨C.煤经气化、液化和干馏三个物理变化过程,可变为清洁能源D.高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强2.下列操作中,完全正确的一组是()①用试管夹夹持试管时,试管夹从试管底部上套,夹在试管的中上部②给盛有液体的体积超过1/3容积的试管加热③把鼻孔靠近容器口去闻气体的气味④将试管平放,用纸槽往试管里送入固体粉末后,然后竖立试管⑤取用放在细口瓶的液体时,取下瓶塞倒立放在桌面上,倾倒液体时,瓶上的标签对着地面⑥将烧瓶放在桌上,用力塞紧塞子⑦用坩埚钳夹取加热后的蒸发皿⑧将滴管垂直伸进试管内滴加液体⑨稀释浓硫酸时,把水迅速倒入盛有浓硫酸的量筒中[来⑩检验装置的气密性时,把导管的一端浸入水中,用手捂住容器的外壁或用酒精灯微热。A.①④⑦⑩B.①④⑤⑦⑩C.①④⑤⑦⑧⑩D.④⑤⑦⑧⑩3.常温下,下列各组离子在指定溶液中一定能大量共存的是A.滴入酚酞呈无色的溶液中:K+、Al3+、Cl-、CO32-B.澄清的溶液中:Na+、K+、MnO4—、AlO2—C.=10-13mol·L-1的溶液:Na+、[Ag(NH3)2]+、OH-、NO3-D.c(I-)=0.1mol·L-1的溶液中:Na+、H+、ClO-、SO42-4.我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3×10-9m)恢复了磁性。“钴酞菁”分子的结构和性质与人体内的血红素及植物体内的叶绿素非常相似。下列说法中不正确的是A.“钴酞菁”分子所形成的分散系不具有丁达尔效应B.“钴酞菁”分子能透过滤纸C.此项工作可以用来改变分子的某些物理性质D.此项工作可广泛应用于光电器件、生物技术等方面5.两个体积相同的容器,一个盛有NO,另一个盛有N2和O2,在同温同压下两容器内的气体一定具有相同的①原子总数;②质子总数;③分子总数;④质量。A.①③B.②④C.①D.④6.在标准状况下,1L氧气约含有n个分子,则阿伏加德罗常数的值可表示为A.n/22.4B.n/32C.n/16D.22.4n7.用下列实验装置或操作进行相应实验,能达到实验目的的是A.用图1装置验证化学能转化为电能B.用图2所示装置检验溴乙烷与NaOH醇溶液共热产生的乙烯C.用图3装置制备氢氧化亚铁D.利用图4装置证明酸性:CH3COOH>H2CO3>苯酚8..某混合溶液中所含离子的物质的量浓度如下表,则M可能为()所含离子NOSOH+M物质的量浓度(mol·L-1)2121A.Mg2+B.Ba2+C.F-D.Na+9.相同体积的氯化钠、氯化镁、氯化铝溶液分别与过量的硝酸银溶液反应,所生成的沉淀物质的量相同,则原氯化钠、氯化镁、氯化铝溶液的物质的量浓度之比为()A.1:2:3B.3:2:1C.6:3:1D.6:3:210.甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化)。下列各组物质中,不满足图示转化关系的是A.①③B.②③C.②④D.①④11.下列离子方程式错误的是A.向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42—=BaSO4↓+2H2OB.酸性介质中KMnO4氧化H2O2:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2OC.等物质的量的MgCl2、Ba(OH)2和HC1溶液混合:Mg2++2OH-=Mg(OH)2↓D.铅酸蓄电池充电时的正极反应:PbSO4+2H2O-2e-=PbO2+4H++SO42—12.用NA表示阿伏加德罗常数,下列叙述正确的是A.1molO2与金属钠反应,O2一定得到4NA个电子B.常温常压下,1.06gNa2CO3含有的Na+离子数为0.02NAC.标准状况下,22.4LSO2和22.4LSO3中所含分子数均为NAD.物质的量浓度为0.5mol·L-1的MgCl2溶液中,含有Cl-个数为1NA13.据最新报道,科学家发现了如下反应:O2+PtF6===O2(PtF6),已知O2(PtF6)为离子化合物,其中Pt的化合价为+5,F元素在化合物中化合价-1,对于此反应,下列说法正确的是A.在此反应中,O2是氧化剂,PtF6是还原剂B.O2(PtF6)中氧元素的化合价为+1C.O2(PtF6)只是氧化产物...