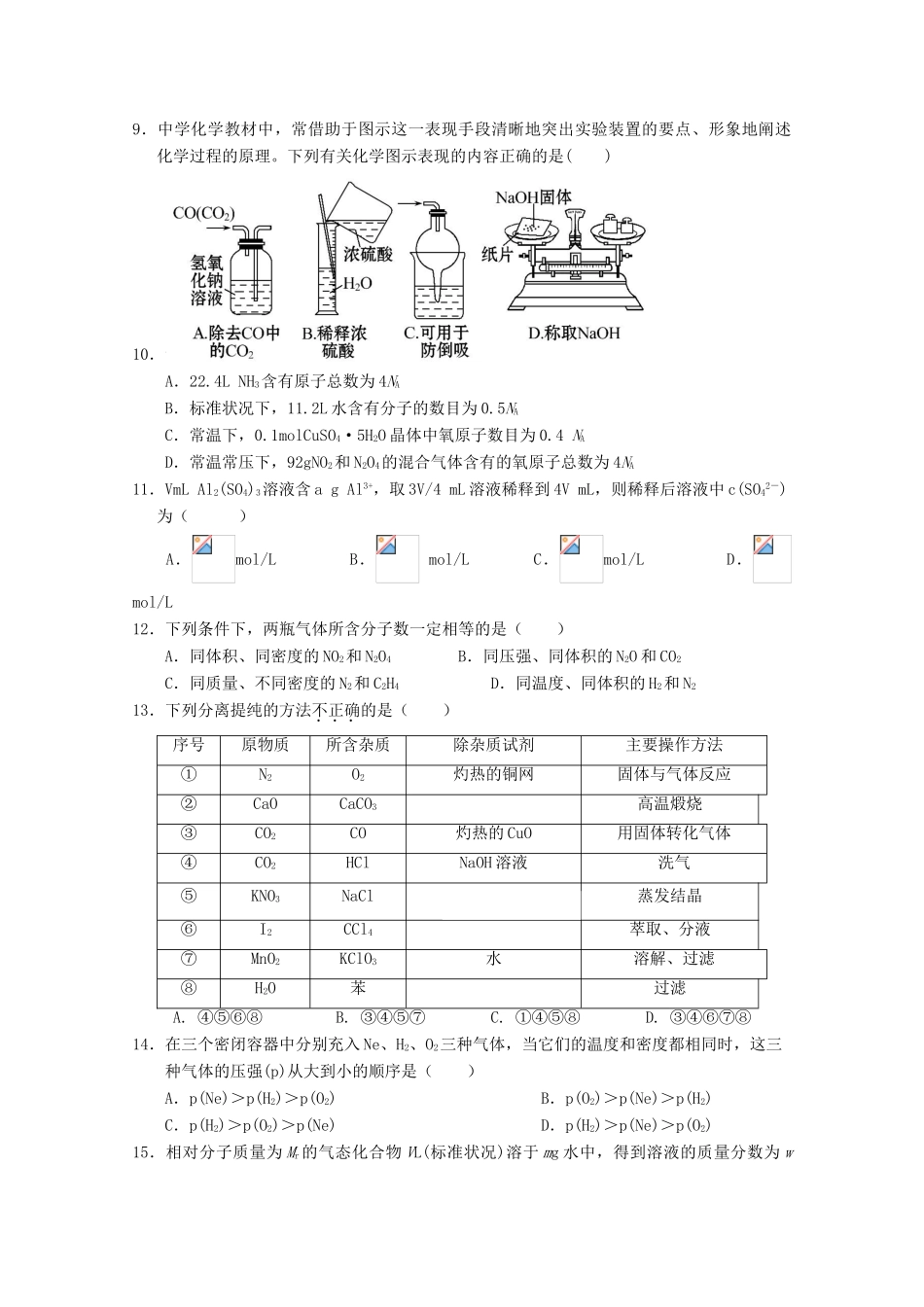
湖北省荆州市沙市区2017-2018学年高一化学上学期第二次双周考试题时间:90分钟分数:100分考试时间:2017年9月28日可能用到的相对原子质量:H1He4C12N14O16Na23Al27S32Cl35
5Ne20第Ⅰ卷(选择题共40分)选择题(本题包括20小题,每小题2分,共40分,每小题只有一个选项符合题意)1.下列说法正确的是()A.1molOH-的质量为17g·mol-1B.2molH2O的摩尔质量是1molH2O的摩尔质量的2倍C.1mol水中含有2mol氢和1mol氧D.3
01×1023个SO2分子的质量为32g2.下列关于实验的描述中正确的是()A
容量瓶使用前先放在烘箱里烘干B
分液操作时,先将分液漏斗中上层液体从上口倒出后,再将下层液体从下口放出C
定容时,胶头滴管不能伸入到容量瓶口中D
萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大3.标准状况下,等体积的NH3和CH4两种气体,下列有关说法错误的是()A.所含分子数目相同B.所含氢原子物质的量之比为3:4C.质量之比为16:17D.密度之比为17:164.下列实验操作均要用玻璃棒,其中玻璃棒的作用及其目的相同的是()①过滤②蒸发③溶解④向容量瓶转移液体A.①和②B.①和④C.③和④D.①和③5.amolH2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为()A.mol-1B.mol-1C.mol-1D.mol-16.设NA为阿伏加德罗常数的值,下列说法不正确的是()A.分子总数为NA的NO2和CO2混合气体含有的氧原子数为2NAB.0
2mol/L的K2SO4溶液中含有0
2NA个K+C.常温常压下,16gCH4和1molNH3所含质子数均为10NAD.101kPa、4℃时,18mL水和同条件下17gNH3所含分子数相等7.某溶液可能含有SO、CO、Cl-中的一种或几种,为确定该溶液