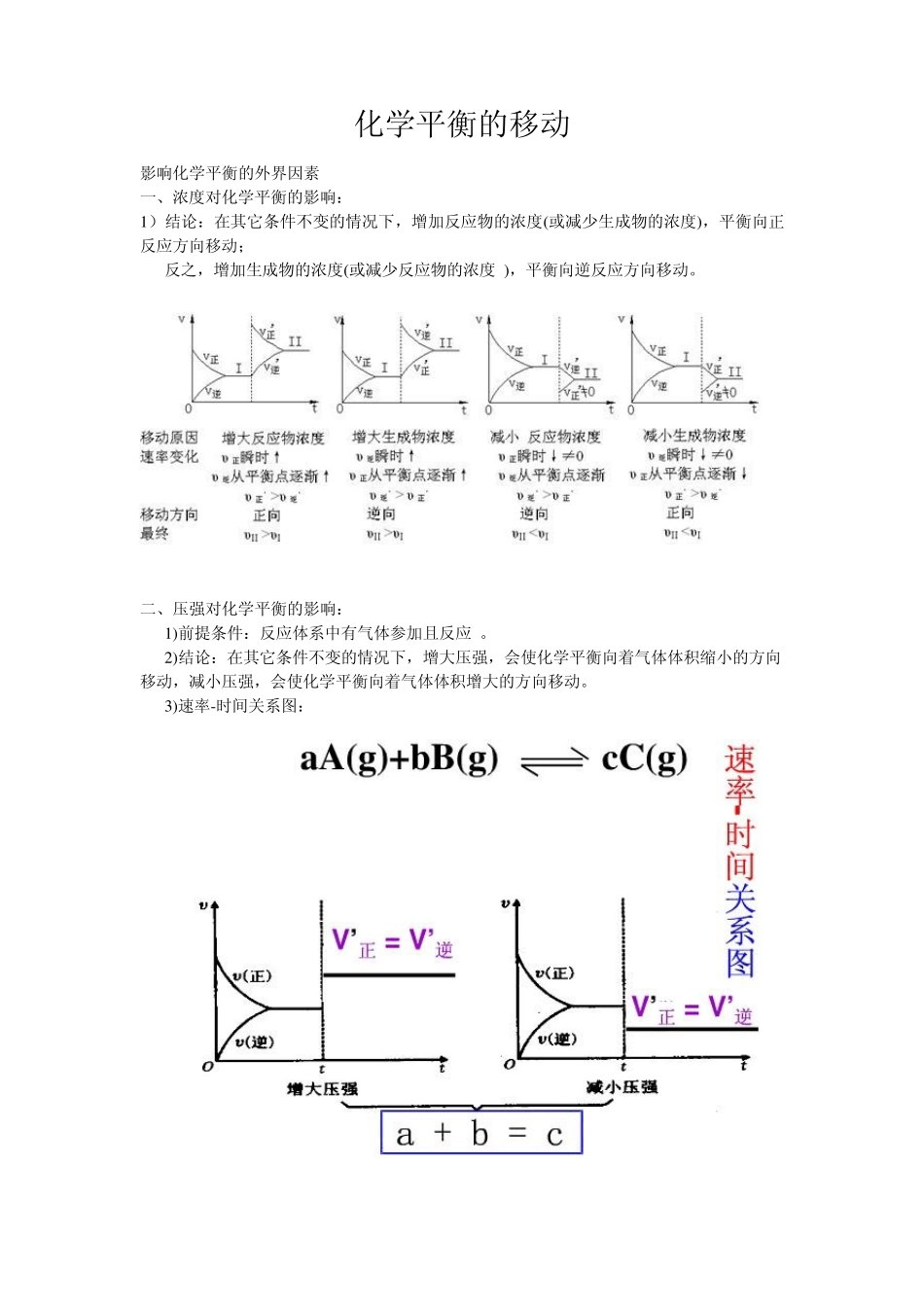
化学平衡的移动 影响化学平衡的外界因素 一、浓度对化学平衡的影响: 1 )结论:在其它条件不变的情况下,增加反应物的浓度(或减少生成物的浓度),平衡向正反应方向移动; 反之,增加生成物的浓度(或减少反应物的浓度 ),平衡向逆反应方向移动
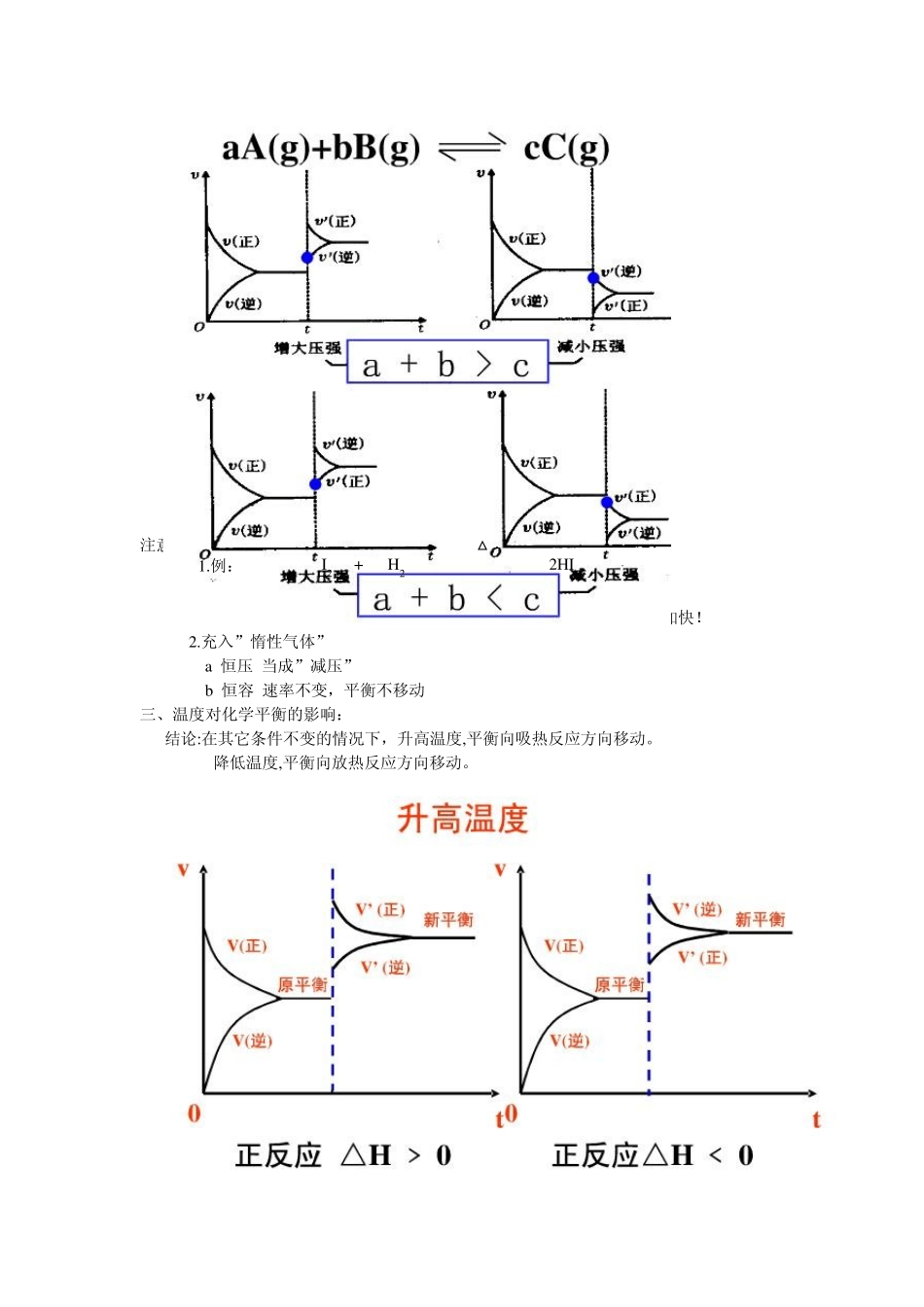
二、压强对化学平衡的影响: 1 )前提条件:反应体系中有气体参加且反应
2 )结论:在其它条件不变的情况下,增大压强,会使化学平衡向着气体体积缩小的方向移动,减小压强,会使化学平衡向着气体体积增大的方向移动
3 )速率-时间关系图: 注意: 增大体系的压强,平衡不移动,但浓度增大,颜色加深,速率加快
充入”惰性气体” a 恒压 当成”减压” b 恒容 速率不变,平衡不移动 三、温度对化学平衡的影响: 结论:在其它条件不变的情况下,升高温度,平衡向吸热反应方向移动
降低温度,平衡向放热反应方向移动
例: I2 + H2 2HI △ 四、催化剂对化学平衡的影响: 催化剂对可逆反应的影响:同等程度改变化学反应速率,V ’正= V ’逆,只改变反应到达平衡所需要的时间,而不影响化学平衡的移动
平衡移动的结果 影响平衡的条件 平衡移动的方向 平衡移动的结果 浓度 增大反应物 向正向移动 使反应物浓度减小 减小生成物 使生成物浓度增大 减小反应物 向逆向移动 使反应物浓度增大 增大生成物 使生成物浓度减小 压强 增大压强 向体积缩小移动 使压强减小 减小压强 向体积增大移动 使压强增大 温度 升高温度 向吸热方向移动 使温度降低 降低温度 向放热方向移动 使温度升高 要引起化学平衡的移动,必须是由于外界条件的改变而引起 V 正≠ V 逆
平衡移动原理(勒夏特列原理):改变影响化学平衡的一个条件(如浓度、压强、或温度),平衡就向能减弱这种改变的方向移动
练习: 1.关于催化剂的叙述,正确的是 ( ) A
催化剂在化学反应前后性