第 29 讲 难溶电解质的溶解平衡考纲要求1
了解难溶电解质的溶解平衡及影响因素
了解沉淀溶解平衡的应用
理解溶度积的含义及其表达式,能进行相关的计算
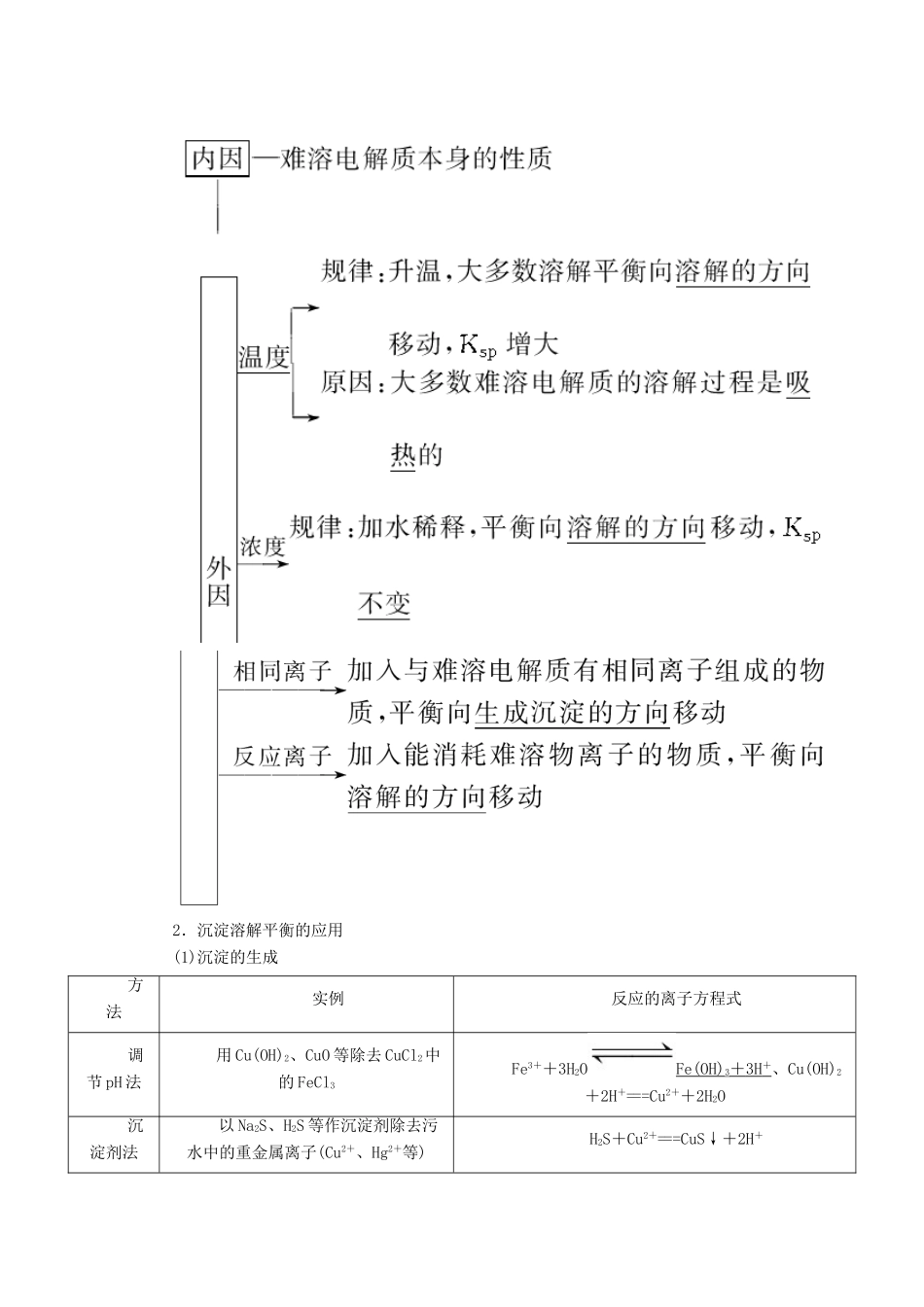
考点一 沉淀溶解平衡及其应用1.沉淀溶解平衡(1)电解质在水中的溶解度在 20 ℃时,电解质在水中的溶解度与溶解性的关系如下:(2)溶解平衡的建立过程固体溶质溶液中的溶质(3)特征(4)影响因素 2.沉淀溶解平衡的应用(1)沉淀的生成方法实例反应的离子方程式调节 pH 法用 Cu(OH)2、CuO 等除去 CuCl2中的 FeCl3Fe3++3H2OFe(OH)3+ 3H + 、Cu(OH)2+2H+===Cu2++2H2O沉淀剂法以 Na2S、H2S 等作沉淀剂除去污水中的重金属离子(Cu2+、Hg2+等)H2S+Cu2+===CuS↓+2H+(2)沉淀的溶解① 酸溶解法:如 CaCO3溶于盐酸,离子方程式为 CaCO3+2H+===Ca2++H2O+CO2↑
② 盐溶解法:如 Mg(OH)2 溶于 NH4Cl 溶液,离子方程式为 Mg(OH)2+2NH===Mg 2 + + 2NH3·H2O
(3)沉淀的转化① 实质:沉淀溶解平衡的移动
② 特征:a.一般说来,溶解度小的沉淀转化为溶解度更小的沉淀容易实现
b.沉淀的溶解度差别越大,越容易转化
③ 应用:a.锅炉除垢:将 CaSO4转化为 CaCO3,离子方程式为:CaSO4+CO===CaCO3+SO
b.矿物转化:CuSO4溶液遇 ZnS(闪锌矿)转化为 CuS(铜蓝)的离子方程式为:Cu2+(aq)+ZnS(s)===CuS(s)+Zn2+(aq)
【感悟测评】 判断正误(正确的打“√”,错误的打“×”)(1)向 0
1 mol/L 的 AgNO3溶液中加入过量的盐酸完全反应后溶液中无 Ag+
( )(2)沉淀溶解平衡也属于化学平衡,属于动态平衡,即