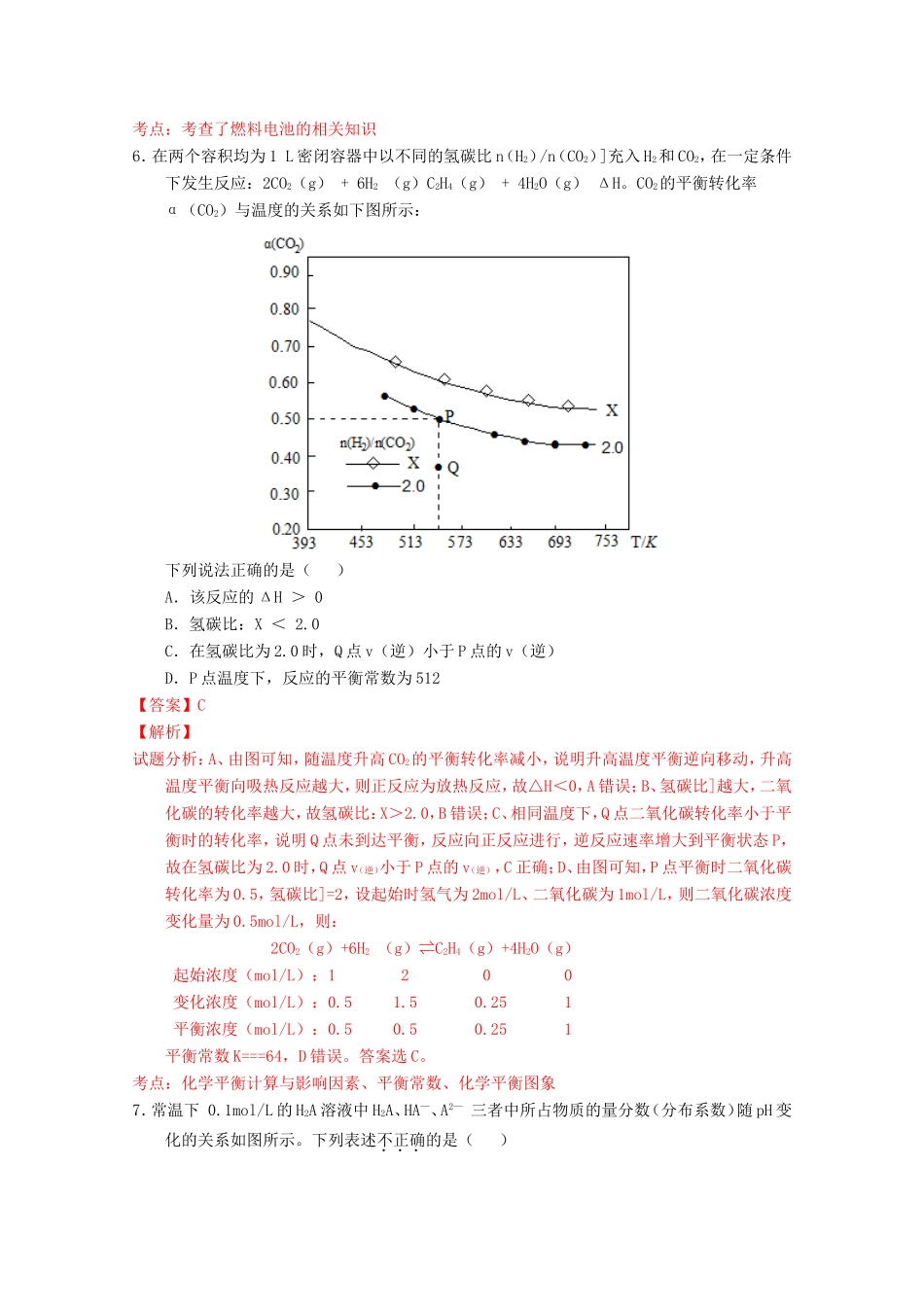
相对原子质量(原子量):H-1C-12N-14O-16Na-23第I卷(选择题共42分)一、选择题(本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求)1.化学与科学、技术、社会、环境密切相关,下列做法中不正确的是()A.回收废旧电池,主要目的是回收其中的金属B.减少燃煤使用,改用风能、太阳能等能源,符合“低碳生活”的理念C.在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质D.用浸泡过高锰酸钾溶液的硅藻土吸收水果中的乙烯,可以实现水果保鲜的目的【答案】A考点:生活中的化学2.下列物质按纯净物、混合物、电解质、非电解质的顺序组合的一组为()A.生石灰、漂白粉、氯化铜、碳酸钠B.胆矾、盐酸、铁、碳酸钙C.蒸馏水、氨水、碳酸氢钠、二氧化硫D.纯盐酸、空气、硫酸、干冰【答案】C【解析】试题分析:A、碳酸钠属于盐,是电解质,错误;B、铁是单质不是电解质,碳酸钙属于盐,是电解质,错误;C、蒸馏水是纯净物、氨水是混合物、碳酸氢钠是电解质、二氧化硫是非电解质,正确;D、纯盐酸也混合物,错误,答案选C。考点:考查物质分类的判断3.常温下,下列各组离子在指定溶液中一定能大量共存的是()A.能溶解Al(OH)3的溶液:NH4+、K+、SO42-、HCO3-B.0.1mol/L的AlCl3溶液中:Na+、K+、SO42-、HCO3-C.25℃时,水电离出的c(H+)=1×l0-l3mol/L的溶液中:K+、Ba2+、NO3-、S2-D.能使酚酞变红的溶液:Na+、Ba2+、NO3-、Cl-【答案】D考点:离子共存4.下列实验目的对应的实验操作和实验原理均正确的是()实验目的实验操作实验原理A提纯混有少量硝酸钾的氯化钠在较高温度下制得浓溶液再冷却结晶、过滤、干燥氯化钠溶解度随温度升高变化不大,而硝酸钾溶解度随温度升高显著增大B配制FeCl3溶液将FeCl3固体溶解于适量硫酸溶液H+抑制FeCl3水解C检验溶液中是否含有NH4+取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体NH3溶于水后溶质的主要存在形式是NH4+、OH-D验证Fe(OH)3的溶解度小于Mg(OH)2将FeCl3溶液加入Mg(OH)2悬浊液中,振荡3Mg(OH)2+2Fe3+2Fe(OH)3+3Mg2+【答案】D【解析】试题分析:A.提纯混有少量硝酸钾的氯化钠的正确操作是:蒸发结晶、趁热过滤、洗涤、干燥,A项错误;B.配制FeCl3溶液时,将FeCl3固体溶解与适量浓盐酸中,再加水稀释到相应浓度,B项错误;C.NH3溶于水后溶质的主要存在形式是NH3•H2O,NH3•H2O电离产生OH-,C项错误;D.Mg(OH)2可与FeCl3溶液水解出的氢离子结合而溶于FeCl3溶液,D项正确;答案选D。考点:考查化学实验基本操作,实验原理正误判断5.右图为一种微生物燃料电池结构示意图,关于该电池叙述正确的是()A.分子组成为Cm(H2O)n的物质一定是糖类B.微生物所在电极区放电时发生还原反应C.放电过程中,H+从正极区移向负极区D.正极反应式为:MnO2+4H++2e—=Mn2++2H2O【答案】DMnO2Mn2+CO2Cm(H2O)n微生物用电器质子(H+)交换膜考点:考查了燃料电池的相关知识6.在两个容积均为1L密闭容器中以不同的氢碳比n(H2)/n(CO2)]充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)C2H4(g)+4H2O(g)ΔH。CO2的平衡转化率α(CO2)与温度的关系如下图所示:下列说法正确的是()A.该反应的ΔH>0B.氢碳比:X<2.0C.在氢碳比为2.0时,Q点v(逆)小于P点的v(逆)D.P点温度下,反应的平衡常数为512【答案】C【解析】试题分析:A、由图可知,随温度升高CO2的平衡转化率减小,说明升高温度平衡逆向移动,升高温度平衡向吸热反应越大,则正反应为放热反应,故△H<0,A错误;B、氢碳比]越大,二氧化碳的转化率越大,故氢碳比:X>2.0,B错误;C、相同温度下,Q点二氧化碳转化率小于平衡时的转化率,说明Q点未到达平衡,反应向正反应进行,逆反应速率增大到平衡状态P,故在氢碳比为2.0时,Q点v(逆)小于P点的v(逆),C正确;D、由图可知,P点平衡时二氧化碳转化率为0.5,氢碳比]=2,设起始时氢气为2mol/L、二氧化碳为1mol/L,则二氧化碳浓度变化量为0.5mol/L,则:2CO2(g)+6H2(g)⇌C2H4(g)+4H2O(g)起始浓度(mol/L):1...