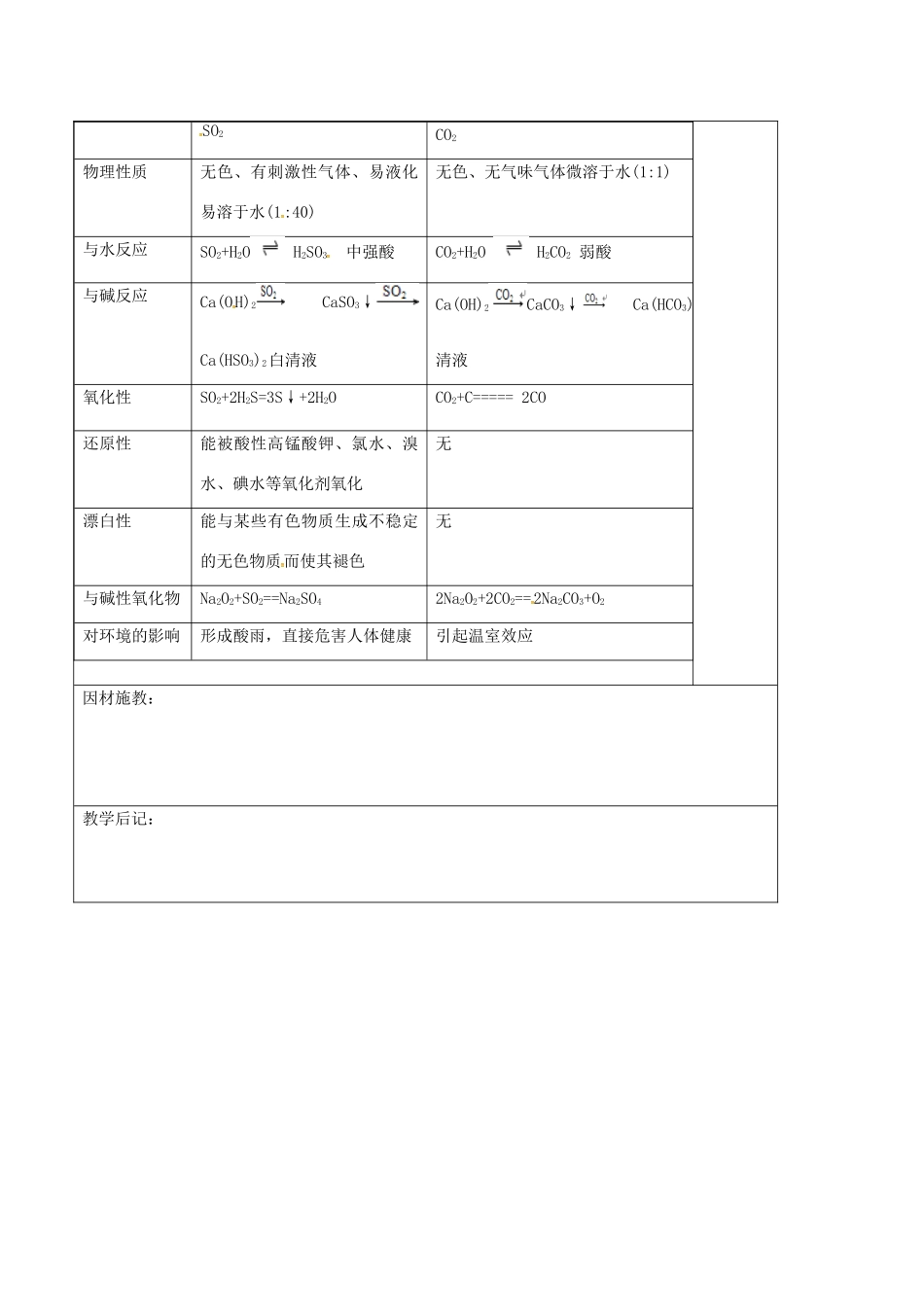
《硫及其化合物》授课题目课题:《硫及其化合物》拟课时第3课时明确目标1.掌握硫单质及其化合物的主要性质,了解其应用。2.了解硫的重要化合物对环境质量的影响。3.二氧化硫和三氧化硫。4.硫的氧化物对大气的污染。4.硫酸。重点难点重点:硫及其化合物的重要性质和用途课型□讲授□习题□复习□讨论□其它教学内容设计师生活动设计4.浓硫酸与稀硫酸的鉴别方法一:取少量蒸馏水,向其中加入少量试样硫酸,如能放出大量热则为浓硫酸,反之则为稀硫酸;方法二:观察状态,浓硫酸为粘稠状液体,而稀硫酸为粘稠度较小的溶液;方法三:比较同体积试样质量,因为浓硫酸的密度较大,相同体积的浓硫酸和稀硫酸,浓硫酸的质量大得多;方法四:取少量试样,向其中投入铁片,若产生大量气体则为稀硫酸,若无明显现象(钝化)则为浓硫酸;方法五:用玻璃棒蘸取试样在纸上写字,立即变黑(浓硫酸的脱水性)为浓硫酸,另一为稀硫酸;方法六:将胆矾晶体(CuSO4·5H2O)分别投入少量试样内,若有颜色改变(蓝色消失或变无色),则为浓硫酸(浓硫酸的吸水性),另一为稀硫酸;方法七:取少量试样,分别投入一小块铜片,稍加热,发生反应的(有气泡产生、溶液变蓝)为浓硫酸,无现象的是稀硫酸。SO的检验被检液—————→取清液————→有无白色沉淀(判断有无SO)。一、SO2与CO2的比较与鉴别例1下列物质能与SO2气体起反应,但无沉淀产生的是()①溴水②Ba(OH)2溶液③石灰水④Na2CO3⑤稀H2SO4⑥Na2SO4⑦Na2SO3A.只有①B.①④⑤C.④⑥⑦D.①④⑦教师评讲例题,师生总结。学生回顾相关内容,并练习《金版学案》对应内容SO2CO2物理性质无色、有刺激性气体、易液化易溶于水(1:40)无色、无气味气体微溶于水(1:1)与水反应SO2+H2OH2SO3中强酸CO2+H2OH2CO2弱酸与碱反应Ca(OH)2CaSO3↓Ca(HSO3)2白清液Ca(OH)2CaCO3↓Ca(HCO3)清液氧化性SO2+2H2S=3S↓+2H2OCO2+C=====2CO还原性能被酸性高锰酸钾、氯水、溴水、碘水等氧化剂氧化无漂白性能与某些有色物质生成不稳定的无色物质而使其褪色无与碱性氧化物Na2O2+SO2==Na2SO42Na2O2+2CO2==2Na2CO3+O2对环境的影响形成酸雨,直接危害人体健康引起温室效应因材施教:教学后记: