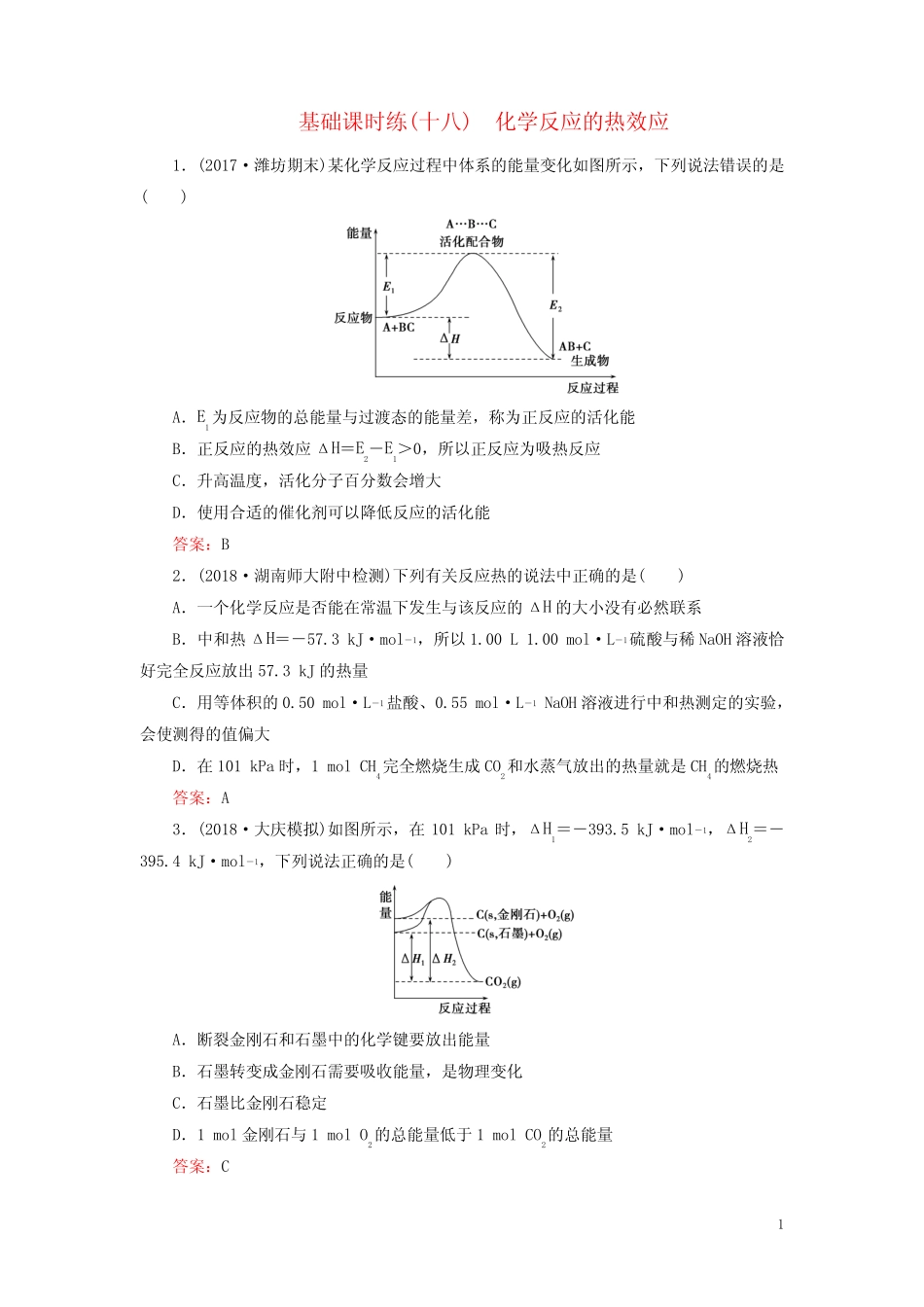
1基础课时练(十八)化学反应的热效应1.(2017·潍坊期末)某化学反应过程中体系的能量变化如图所示,下列说法错误的是()A.E1为反应物的总能量与过渡态的能量差,称为正反应的活化能B.正反应的热效应ΔH=E2-E1>0,所以正反应为吸热反应C.升高温度,活化分子百分数会增大D.使用合适的催化剂可以降低反应的活化能答案:B2.(2018·湖南师大附中检测)下列有关反应热的说法中正确的是()A.一个化学反应是否能在常温下发生与该反应的ΔH的大小没有必然联系B.中和热ΔH=-57
3kJ·mol-1,所以1
00mol·L-1硫酸与稀NaOH溶液恰好完全反应放出57
3kJ的热量C.用等体积的0
50mol·L-1盐酸、0
55mol·L-1NaOH溶液进行中和热测定的实验,会使测得的值偏大D.在101kPa时,1molCH4完全燃烧生成CO2和水蒸气放出的热量就是CH4的燃烧热答案:A3.(2018·大庆模拟)如图所示,在101kPa时,ΔH1=-393
5kJ·mol-1,ΔH2=-395
4kJ·mol-1,下列说法正确的是()A.断裂金刚石和石墨中的化学键要放出能量B.石墨转变成金刚石需要吸收能量,是物理变化C.石墨比金刚石稳定D.1mol金刚石与1molO2的总能量低于1molCO2的总能量答案:C24.(2017·天津期末)向Na2CO3溶液中滴加盐酸,反应过程中能量变化如图所示
下列说法正确的是()A.反应HCO-3(aq)+H+(aq)===CO2(g)+H2O(l)为放热反应B.CO2-3(aq)+2H+(aq)===CO2(g)+H2O(l)ΔH=ΔH1+ΔH2+ΔH3C.ΔH1>ΔH2,ΔH2<ΔH3D.H2CO3(aq)===CO2(g)+H2O(l),若使用催化剂,则ΔH3变小解析:选B由题图可知,反应物具有的总能量低于生成物具有的总能量,则