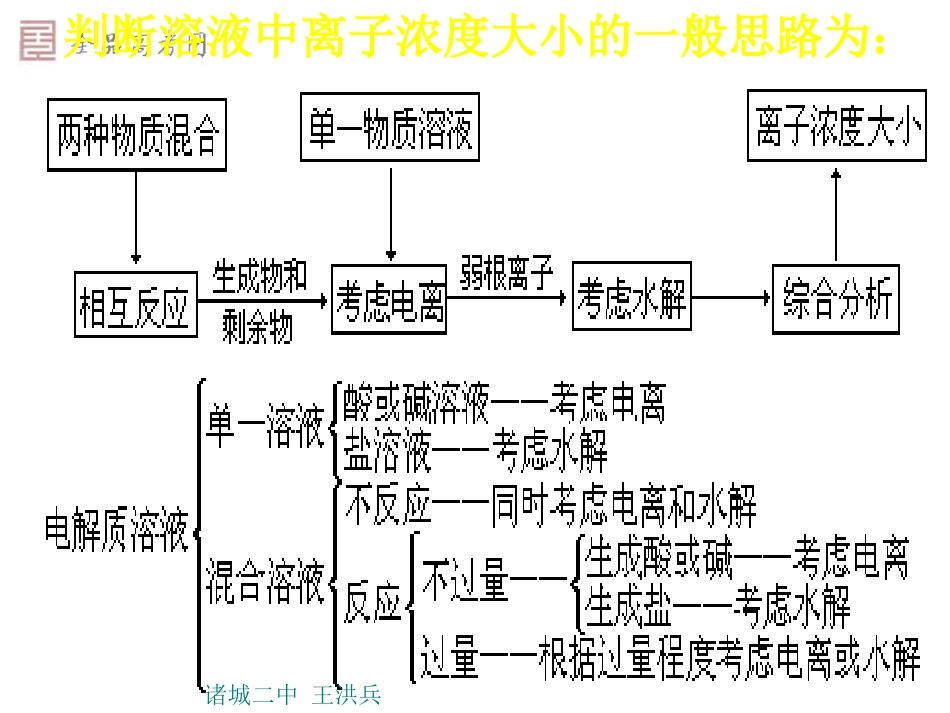
判断溶液中离子浓度大小的一般思路为:诸城二中王洪兵【例3】比较NH4Cl溶液中离子浓度的大小
【例1】CH3COOH溶液中有哪些微粒
比较离子浓度大小关系
【例2】H2S溶液中离子浓度大小关系
[H2S]>[H+]>[HS-]>[S2-]>[OH-][CH3COOH]>[H+]>[CH3COO-]>[OH-]CCl->CNH4+>CH+>COH-2、溶质为一种盐•①考虑电解质的电离,将其电离成离子•②考虑“弱离子”的水解•③c(不水解离子)>c(水解离子)•④根据溶液的酸碱性得出CH+和COH-的大小
•一、若溶液中只含有一种溶质•1、溶质为弱酸或弱碱•①考虑弱电解质的电离非常微弱
•c(不电离分子)>c(离子)•②多元弱酸分步电离•c(第一步电离得到的离子)>c(第二步离子)注意:1、若溶液中含有等物质的量浓度的CH3COO-和CH3COOH,NH4+和NH3
H2O等两种或两种以上溶质
2、一般主要考虑弱电解质的电离(电离程度大于水解程度),特殊情况则应根据题目条件推导.二、若溶液中有两种溶质【例4】物质的量相同CH3COOH和CH3COONa溶液中离子浓度大小关系
【例5】物质的量相同NH4Cl和NH3
H2O溶液中离子浓度大小关系
[CH3COO-]>[Na+]>[H+]>[OH-][NH4+]>[Cl-]>[OH-]>[H+](1)两物质不反应((22)两种物质反应
)两种物质反应
1、等体积等浓度的MOH强碱溶液和HA弱酸溶液混和后,混和液中有关离子的浓度应满足的关系是()[M+]>[A-]>[OH-]>[H+][NH4+]>[Cl-]>[OH-]>[H+]2、将PH=2的盐酸与PH=12的氨水等体积混合,在所得的混合溶液中,下列关系式正确的是()注意:先考虑反应溶液中的溶质,然后再比较浓度大小
分析:两物质完全反应,所以反应后溶液中的溶质为MA分析:两物质反应