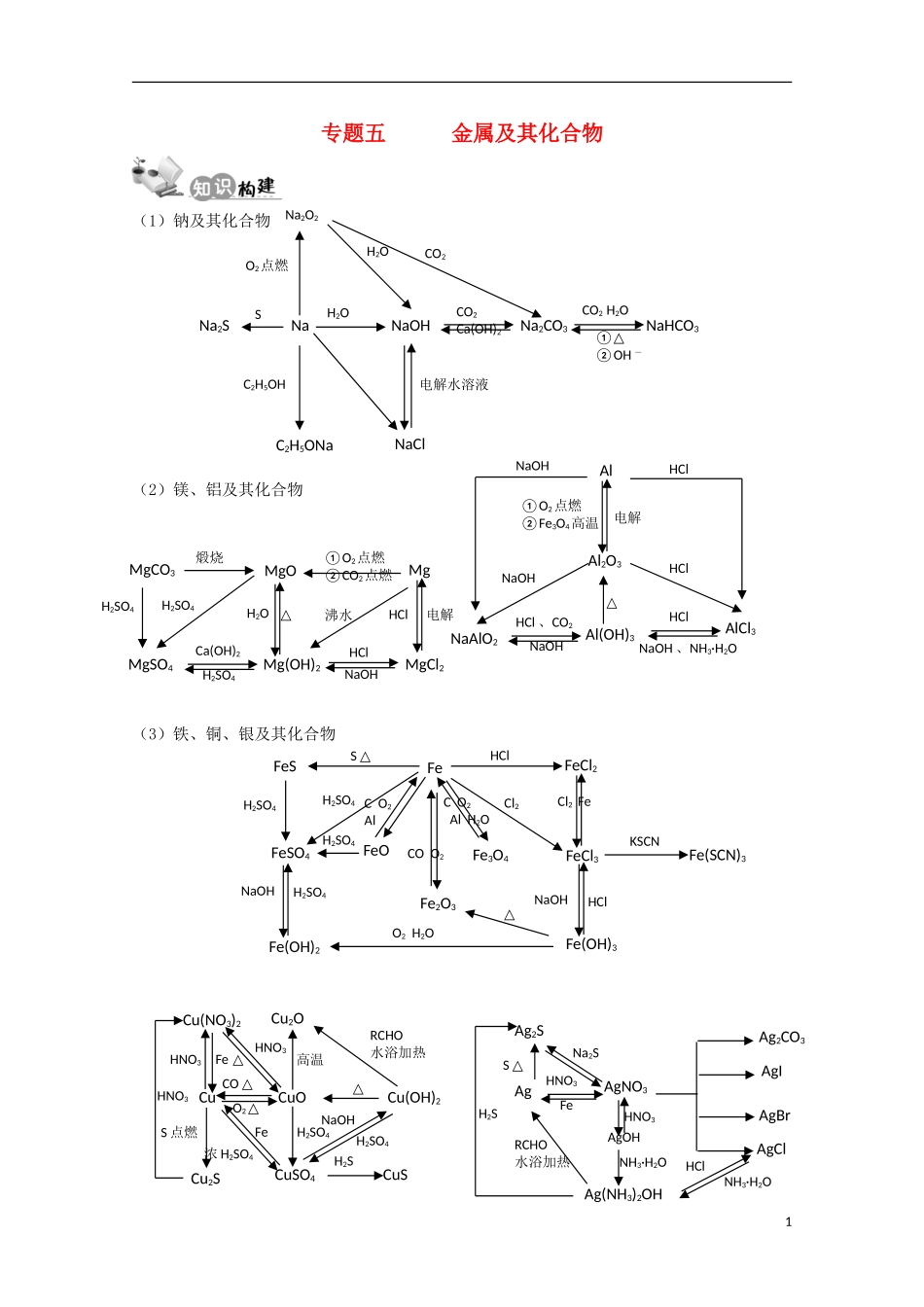
专题五金属及其化合物(1)钠及其化合物(2)镁、铝及其化合物(3)铁、铜、银及其化合物1NaNa2SNaOHNa2CO3NaHCO3CO2H2O①△②OH-CO2Ca(OH)2H2OSNa2O2H2OO2点燃CO2C2H5ONaNaClC2H5OH电解水溶液HCl△MgMgOMgCO3Mg(OH)2MgCl2MgSO4H2SO4H2SO4H2SO4电解沸水HClNaOHCa(OH)2H2O煅烧①O2点燃②CO2点燃Cl2FeFeOH2SO4Cl2FeFeCl2FeSFeSO4Fe2O3FeCl3Fe(SCN)3Fe(OH)3Fe(OH)2Fe3O4H2SO4H2SO4H2SO4HClNaOHHClNaOHCO2AlH2OCO2AlCOO2O2H2O△S△KSCNH2SO4△NaOHFeFeHNO3CuH2SO4△HNO3CuOCu(OH)2Cu2OCu(NO3)2CuSO4Cu2SCuSH2S浓H2SO4S点燃O2△CO△HNO3高温RCHO水浴加热AgOHNa2SS△FeAgAgNO3Ag2SAg(NH3)2OHRCHO水浴加热Ag2CO3AgIAgBrAgClH2SHNO3HNO3NH3·H2ONH3·H2OHClAlAl2O3NaAlO2AlCl3Al(OH)3①O2点燃②Fe3O4高温电解NaOHNaOHNaOHNaOH、NH3·H2OHClHClHClHCl、CO2△【备考策略】在江苏近三年的高考中,第I卷主要考查典型物质的性质及其应用,而第Ⅱ卷则将元素化合物知识的考查分散到多个题型中,结合化学理论、化学实验和计算等进行考查。元素化合物知识是中学化学的核心,必须打牢基础。高考以识记、理解、综合应用、探究等各种能力层次呈现,以应用为主,第1卷较简单而第Ⅱ卷中中等难度的题目居多,似乎有将框图题挪于选择题中的趋势。第I卷中涉及的主打金属元素Al、Fe、Cu,第Ⅱ卷中常考查陌生金属如Zn、Ma、Cr、Co等。2013年的备考中,在复习元素化合物知识时,应以化学基本理论为指导,与化学实验相结合,这样不仅能够知其然,还能够知其所以然。就能较好地掌握元素化合物知识。结合化学基本理论复习元素化合物,并以此强化基本理论知识,突出应用。类型一、金属及其化合物性质例1.(2012·海南化学卷)在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:I:向废液中投入过量铁屑,充分反应后分离出固体和滤液:II:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。己知:Ksp[Fe(OH)3]=4.0×10-38回答下列问题:(1)FeCl3蚀刻铜箔反应的离子方程式为:(2)过程I加入铁屑的主要作用是,分离得到固体的主要成分是,从固体中分离出铜需采用的方法是;(3)过程II中发生反应的化学方程式为;(4)过程II中调节溶液的pH为5,金属离子浓度为。(列式计算)【知识总结】金属及其化合物的特性1.金属单质的性质:与水、酸反应,注意铁与水蒸气反应、铝与NaOH溶液反应、铝热反应。2.金属氧化物的性质:与水、酸反应,注意Na2O2与水反应、Fe3O4与盐酸反应。3.金属阳离子的性质:与OH-反应,注意Al3+、Fe3+与H2O、OH-/、HCO3-、CO32-、AlO2-的反应,注意Fe3+的氧化性。【变式训练1】下列实验中,溶液颜色有明显变化的是A.少量明矾溶液加入到过量NaOH溶液中B.往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液C.少量Na2O2固体加入到过量NaHSO3溶液中D.往酸性高锰酸钾溶液中滴入少量Fe2(SO4)3溶液类型二、金属及其化合物的转化2例2.(2012·徐州市三模)铝是一种很重要的金属,可以发生一系列反应制备物质。Al①Fe3O4高温Al2O3②NaOHNaAlO2③H2SO4Al2(SO4)3④足量CO2Al(OH)3⑤△⑥FeAl⑦Al①Fe3O4高温Al2O3②NaOHNaAlO2③H2SO4Al2(SO4)3④足量CO2Al(OH)3⑤△⑥FeAl⑦下列说法错误的是()A.反应①又称铝热反应,曾用于野外焊接铁轨B.利用②③反应都能产生氢气,产生等量氢气消耗Al的质量也相等且转移电子数也相等C.常用反应⑥制备Al(OH)3,方法是向Al2(SO4)3溶液中滴加NaOH溶液至恰好完全沉淀D.工业上常用反应⑦制备金属铝,制备过程中常加入冰晶石以降低Al2O3的熔点【方法总结】金属及其化合物的相关“题眼”1.物理性质及用途:银白色的常见金属Na、Mg、Al,淡黄色的Na2O2,白色胶状沉淀Al(OH)3(还有H4SiO4)2.特征反应:两性Al2O3、Al(OH)3的反应,铝铁的钝化、Fe3+与SCN-、苯酚的显色反应,银氨溶液的银镜反应,3.反应条件:电解氧化铝、氯化镁、氯化钠制单质、用C、Al、CO高温还原制备铁、铜等过渡金属,电解硫酸铜溶液,铜银催化醇氧化等。4.重要反应:Al+HCl(NaOH/H2O、Fe2O3)、Na2O2+H2O(CO2、SO2)、Mg+(N2、CO2、CH3CH2OH、NH4Cl)、Fe+H2O、Fe2O3+Al、Fe3++SCN-(Fe、Cu、H2S、...