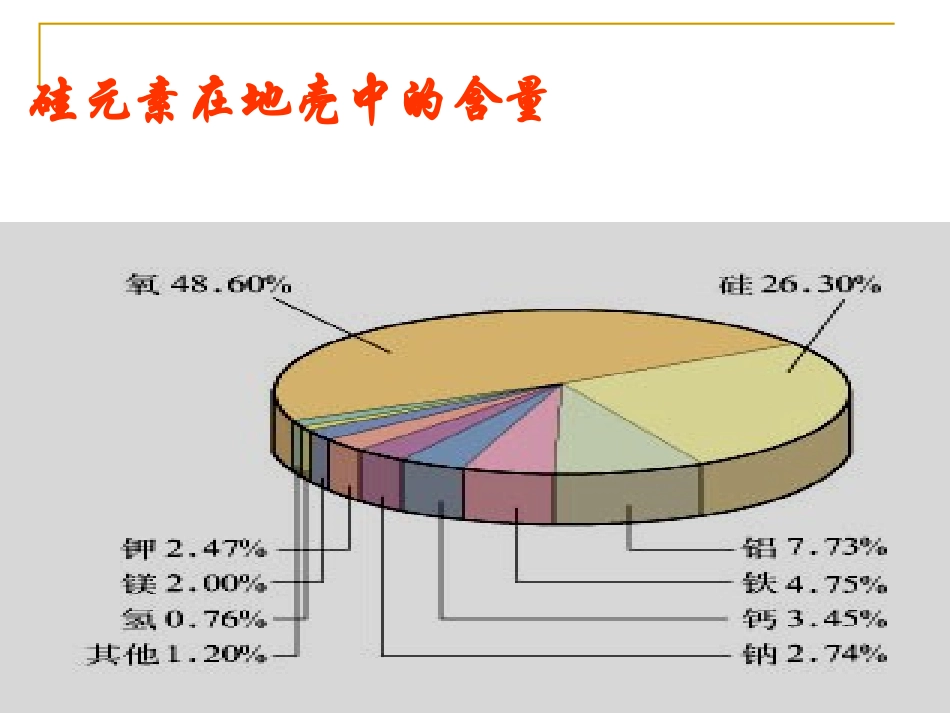
第二单元钠、镁及其化合物硅酸盐矿物与硅酸盐产品2014-12-17硅元素在地壳中的含量一、硅酸盐硅酸盐1、硅酸盐的表示形式活泼金属氧化物·SiO2·H2O【练习】改写成氧化物的形式1、钙长石:CaAl2SiO62、石棉:CaMg3Si4O123、普通玻璃:CaNa2Si6O14CaO·3MgO·4SiO2CaO·Na2O·6SiO2CaO·Al2O3·SiO22、硅酸钠的性质Na2SiO3其水溶液俗称水玻璃用途:粘合剂,防腐剂、防火剂t二、传统的硅酸盐产品:1、陶瓷陶器的制作工序2、水泥A
主要成分硅酸三钙(3CaO•SiO2)、硅酸二钙(2CaO•SiO2)、铝酸三钙(3CaO•Al2O3)B
原料:黏土、石灰石、石膏b
设备:水泥回转窑c
条件:高温锻烧水泥回转窑雄伟的体育馆让人骄傲的三峡工程世贸大厦3、玻璃A
原料:纯碱、石灰石、石英(SiO2)B
设备:玻璃熔炉C
条件:高温熔融D
成分:Na2SiO3、CaSiO3、SiO2E
主要反应:Na2CO3+SiO2=Na2SiO3+CO2↑CaCO3+SiO2=CaSiO3+CO2↑F
种类:普通玻璃、钢化玻璃、有色玻璃、光学玻璃、防弹玻璃、铅玻璃等三、二氧化硅SiO2二氧化硅广泛存在于自然界中,与其他矿物共同构成了岩石
天然二氧化硅也叫硅石,是一种坚硬难熔的固体1
存在:石英制品水晶玛瑙2
物理性质:固体熔沸点比较高不溶于水硬度比较大联想-------沙子3
结构:SiO2是正四面体的空间网状结构,因此性质很稳定③与碱性氧化物反应①与碳酸钠、碳酸钙反应④与HF的反应:②与强碱反应:SiO2+4HF=SiF4↑+2H2O高温SiO2+CaO=CaSiO3SiO2+2NaOH=Na2SiO3+H2O4、二氧化硅的化学性质⑤与C反应制粗硅SiO2+2C=Si+2CO↑(粗硅)高温1
为什么在实验室中盛放NaOH溶