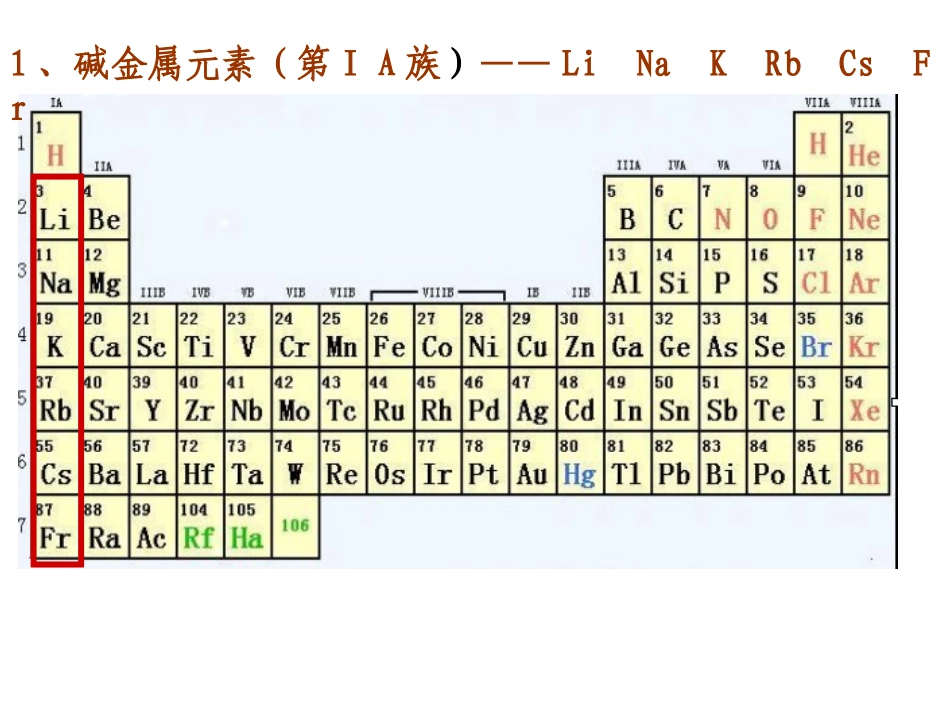
第一节(2)第一章物质结构元素周期律1、碱金属元素(第ⅠA族)——LiNaKRbCsFr(1)碱金属的原子结构元素名称核电荷数原子结构示意图最外层电子数电子层数原子半径碱金属元素锂(Li)钠(Na)钾(K)铷(Rb)铯(Cs)3111937551111123456电子层数逐渐增大原子半径逐渐增大原子结构1
相似性:原子最外层电子都只有一个电子相似性:都易失电子,则具强还原性,均能与氧气和水反应
化学性质决定(2)碱金属的原子结构与化学性质的关系2
递变性:从上到下电子层数↑,原子半径↑,递变性:从上到下,越来越易失电子,则还原性逐渐↑,金属性↑LiNaKRbCs与O2反应与H2O反应从上到下,与H2O反应越来越剧烈,生成的碱的碱性越强
说明从上到下,金属性(活泼性)越来越强从上到下,与O2反应越来越剧烈,与O2反应的产物越来越复杂
(3)碱金属元素的主要物理性质(相似性和递变性)元素名称颜色和状态密度熔点沸点锂银白色,柔软0
534180
51347钠银白色,柔软0
9钾银白色,柔软0
65774铷银白色,柔软1
89688铯略带金色光泽,柔软1
4密度逐渐增大熔沸点逐渐降低1
锂电池是一种高能电池
锂是制造氢弹不可缺少的材料
锂是优质的高能燃料(已经用于宇宙飞船、人造卫星和超声速飞机);4.铷铯主要用于制备光电管、真空管
铯原子钟是目前最准确的计时仪器
碱金属元素的用途:2.液态钠可用作核反应堆的传热介质;3
钾的化合物最大用途是做钾肥
硝酸钾还用于做火药
LiLiNaNaKKRbRbCsCsFrFrIAIA电子层数↑原子半径↑失电子能力↑金属性(还原性)↑碱金属元素的递变性1、下列元素中,原子半径最小的是(),最易失电子的是()A、NaB、LiC、KD、CsBD2、随着核电荷数的增加,碱金属元素的单质(