离子反应第二课时=KCl、Na2SO4、BaCl2是不是电解质
它们在水溶液中以什么形式存在
写出这些物质的电离方程式
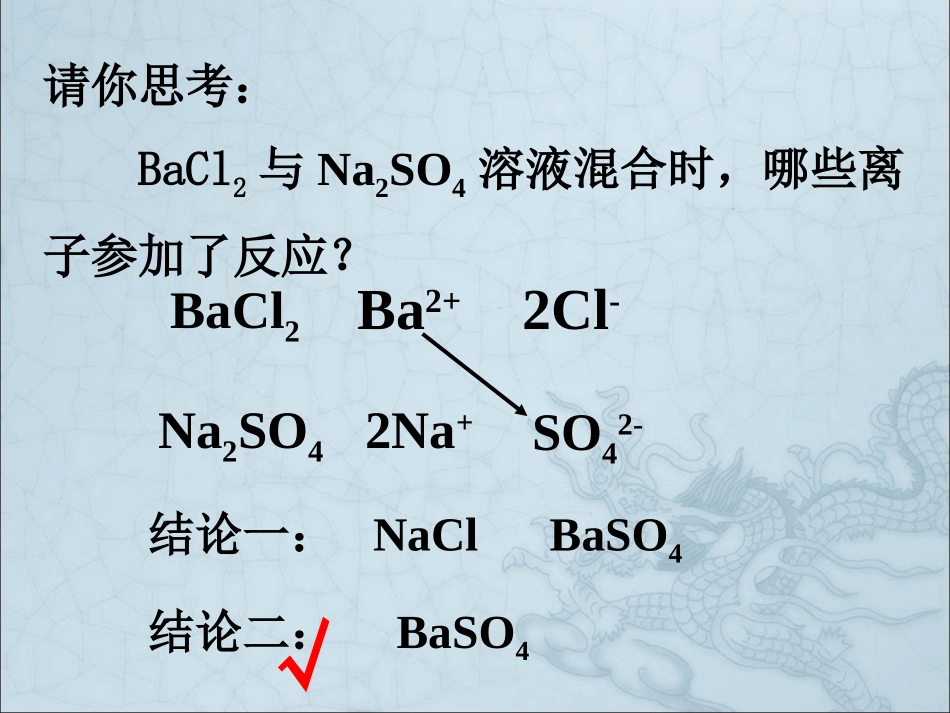
KClK++Cl-BaCl2=Na2SO42Na++SO42-Ba2++2Cl-=请你思考:BaCl2与Na2SO4溶液混合时,哪些离子参加了反应
BaCl2Ba2+2Cl-Na2SO42Na+SO42-结论一:NaClBaSO4结论二:BaSO4√一、离子反应:有离子参加的反应
1、离子反应的特点:离子反应总是向着某些离子浓度减小的方向进行
2、复分解型离子反应发生的条件:生成物有沉淀、气体、弱电解质难溶物易挥发难电离1、概念:用实际参加反应的离子符号来表示反应的式子叫离子方程式
二、离子方程式:以Na2SO4溶液与BaCl2溶液反应为例
离子方程式如何书写呢
(1)写(2)拆BaCl2+Na2SO4=BaSO4↓+2NaClBa2++2Cl-+2Na++SO42-=BaSO4↓+2Na++2Cl-(3)删Ba2++SO42-=BaSO4↓(4)查原子守恒电荷守恒系数最简化2、离子方程式的书写步骤改写的规则:改写的规则:((11)可写成离子的物质:)可写成离子的物质:易溶于水、易电离的物质
强酸:强酸:HH22SOSO44、、HClHCl、、HNOHNO33等等B
强碱:强碱:NaOHNaOH、、KOHKOH、、Ba(OH)Ba(OH)22等等C
可溶性盐(可溶性盐(课本后的溶解性表课本后的溶解性表))((22)仍用化学式表示的物质)仍用化学式表示的物质A
难溶物质:难溶物质:BaSOBaSO44、、Cu(OH)Cu(OH)22等等B
难电离物质:水、难电离物质:水、NHNH33
HH22OO、、CHCH33COOHCOOH等等C
气体:气体:COCO22、、HH22、、SOSO22等等D
单质:单质:HH22、