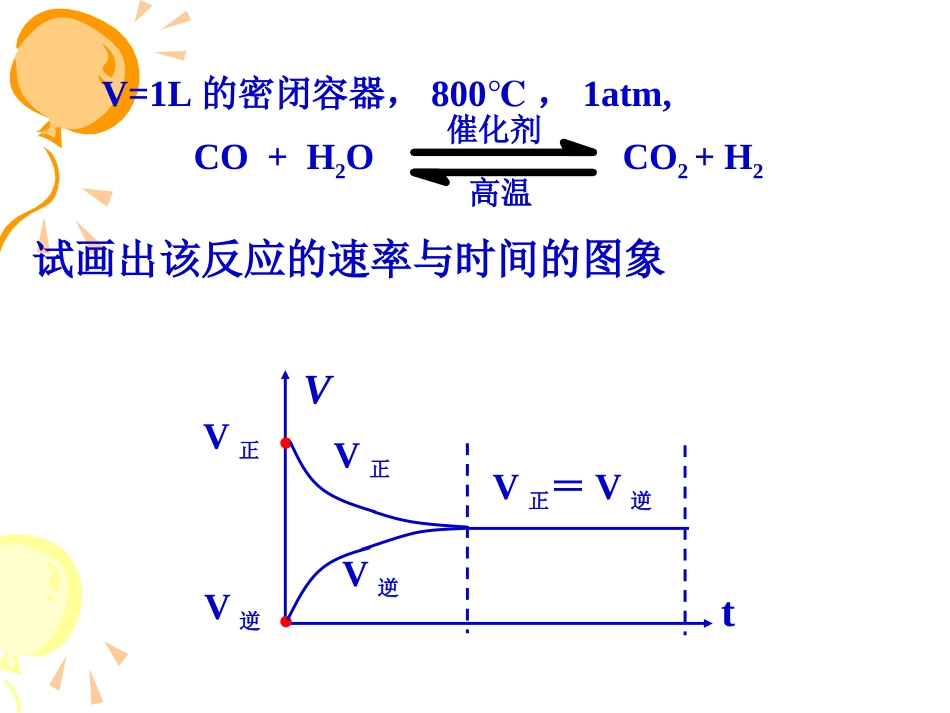
第二章化学反应速率和化学平衡第三节化学平衡一、可逆反应在同一条件下,既能向正反应方向进行同时又能向逆反应方向进行的反应特点:同一条件、同时进行、反应物生成物同时存在(反应不能进行到底)V=1L的密闭容器,800℃,1atm,CO+H2OCO2+H2催化剂高温试画出该反应的速率与时间的图象Vt●V正●V逆V正V逆V正=V逆二、化学平衡状态1、化学平衡状态指在一定条件下的可逆反应里,正反应和逆反应的速率相等,反应混合物中各组分的浓度保持不变的状态
①前提条件:一定条件(恒温恒压或恒温恒容)②研究对象:密闭容器的可逆反应③平衡本质:V正=V逆≠0④平衡标志:各物质的浓度不变2、化学平衡的特征③动:动态平衡②等:V正=V逆≠0④定:反应条件一定,反应混合物中各组分的浓度一定⑤变:条件改变,平衡将被破坏
①逆:可逆反应①同一种物质:该物质的生成速率等于它的消耗速率
②不同的物质:速率之比等于方程式中各物质的计量数之比,但必须是不同方向的速率
化学平衡状态的标志:(1)等速标志,υ正=υ逆(本质特征)(2)恒浓标志,反应混合物中各组成成分的浓度保持不变(外部表现):①各组成成分的质量、物质的量、分子数、体积(气体)、物质的量浓度均保持不变
②各组成成分的质量分数、物质的量分数、气体的体积分数均保持不变
③若反应前后的物质都是气体,且总体积不等,则气体的总物质的量、总压强(恒温、恒容)、平均摩尔质量、混合气体的密度(恒温、恒压)均保持不变
④反应物的转化率、产物的产率保持不变
在一定温度下,反应X2(g)+Y2(g)2XY(g)达到平衡的标志是⑴单位时间内同时生成nmolX2和nmolXY⑵单位时间内生成2nmolXY的同时生成nmolY2⑶容器内总压强不随时间变化⑷单位时间内有nmolX—X键断裂,同时有nmolY—Y键断裂⑸单位时间内生成nmolX2同时生成nmolY2⑹V正=V逆=