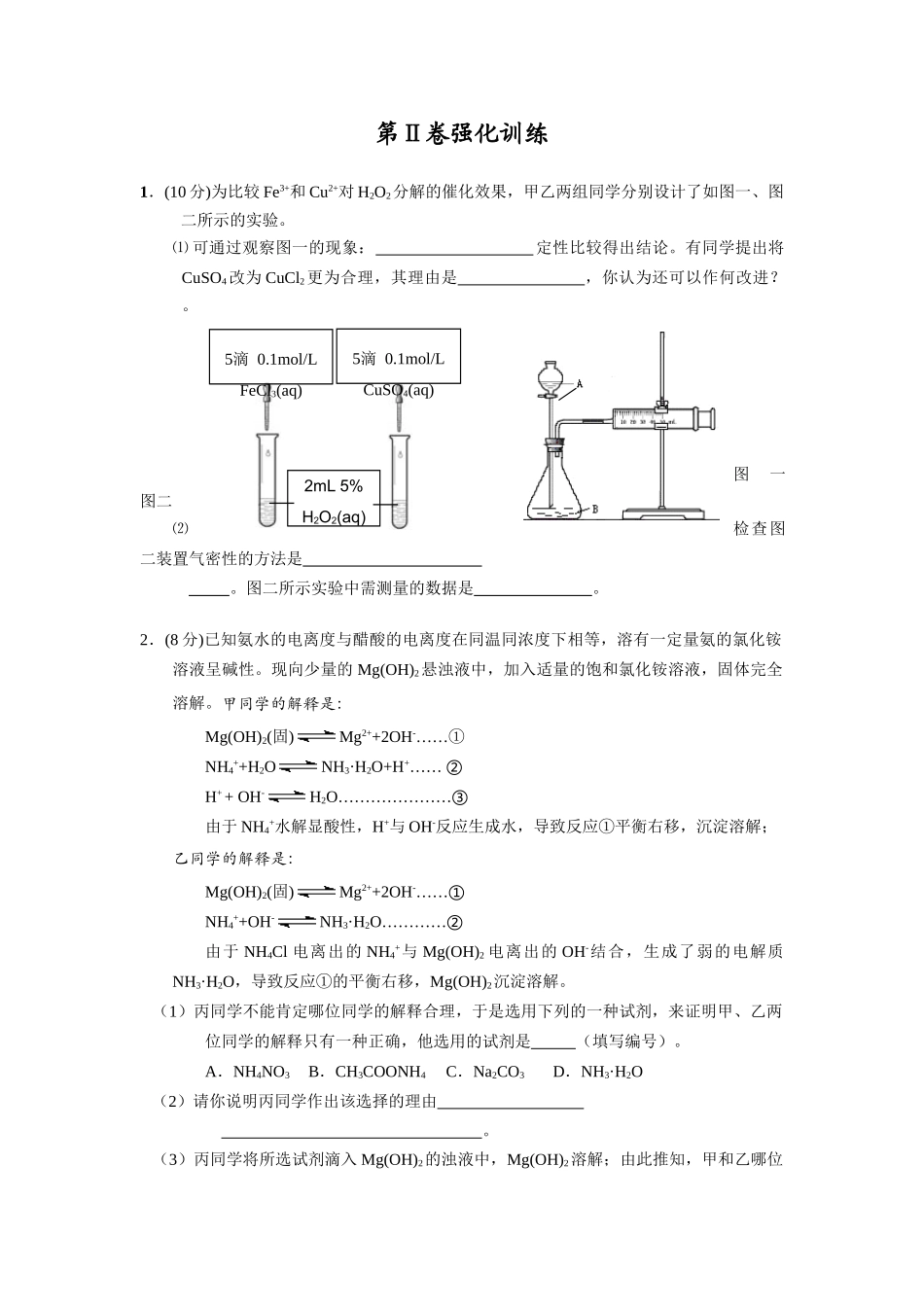
第Ⅱ卷强化训练1.(10分)为比较Fe3+和Cu2+对H2O2分解的催化效果,甲乙两组同学分别设计了如图一、图二所示的实验
⑴可通过观察图一的现象:定性比较得出结论
有同学提出将CuSO4改为CuCl2更为合理,其理由是,你认为还可以作何改进
图一图二⑵检查图二装置气密性的方法是
图二所示实验中需测量的数据是
2.(8分)已知氨水的电离度与醋酸的电离度在同温同浓度下相等,溶有一定量氨的氯化铵溶液呈碱性
现向少量的Mg(OH)2悬浊液中,加入适量的饱和氯化铵溶液,固体完全溶解
甲同学的解释是:Mg(OH)2(固)Mg2++2OH-……①NH4++H2ONH3·H2O+H+……②H++OH-H2O…………………③由于NH4+水解显酸性,H+与OH-反应生成水,导致反应①平衡右移,沉淀溶解;乙同学的解释是:Mg(OH)2(固)Mg2++2OH-……①NH4++OH-NH3·H2O…………②由于NH4Cl电离出的NH4+与Mg(OH)2电离出的OH-结合,生成了弱的电解质NH3·H2O,导致反应①的平衡右移,Mg(OH)2沉淀溶解
(1)丙同学不能肯定哪位同学的解释合理,于是选用下列的一种试剂,来证明甲、乙两位同学的解释只有一种正确,他选用的试剂是(填写编号)
A.NH4NO3B.CH3COONH4C.Na2CO3D.NH3·H2O(2)请你说明丙同学作出该选择的理由
(3)丙同学将所选试剂滴入Mg(OH)2的浊液中,Mg(OH)2溶解;由此推知,甲和乙哪位2mL5%H2O2(aq)5滴0
1mol/LFeCl3(aq)5滴0
1mol/LCuSO4(aq)同学的解释更合理(填“甲”或“乙”);完成NH4Cl饱和溶液使Mg(OH)2悬浊溶解的离子方程式
3.(14分)茶是潮汕人民最离不开的饮品,其中含有多种有益于人体健康的成分,据测定茶叶中含有450种以上的有机成分与15种以上的