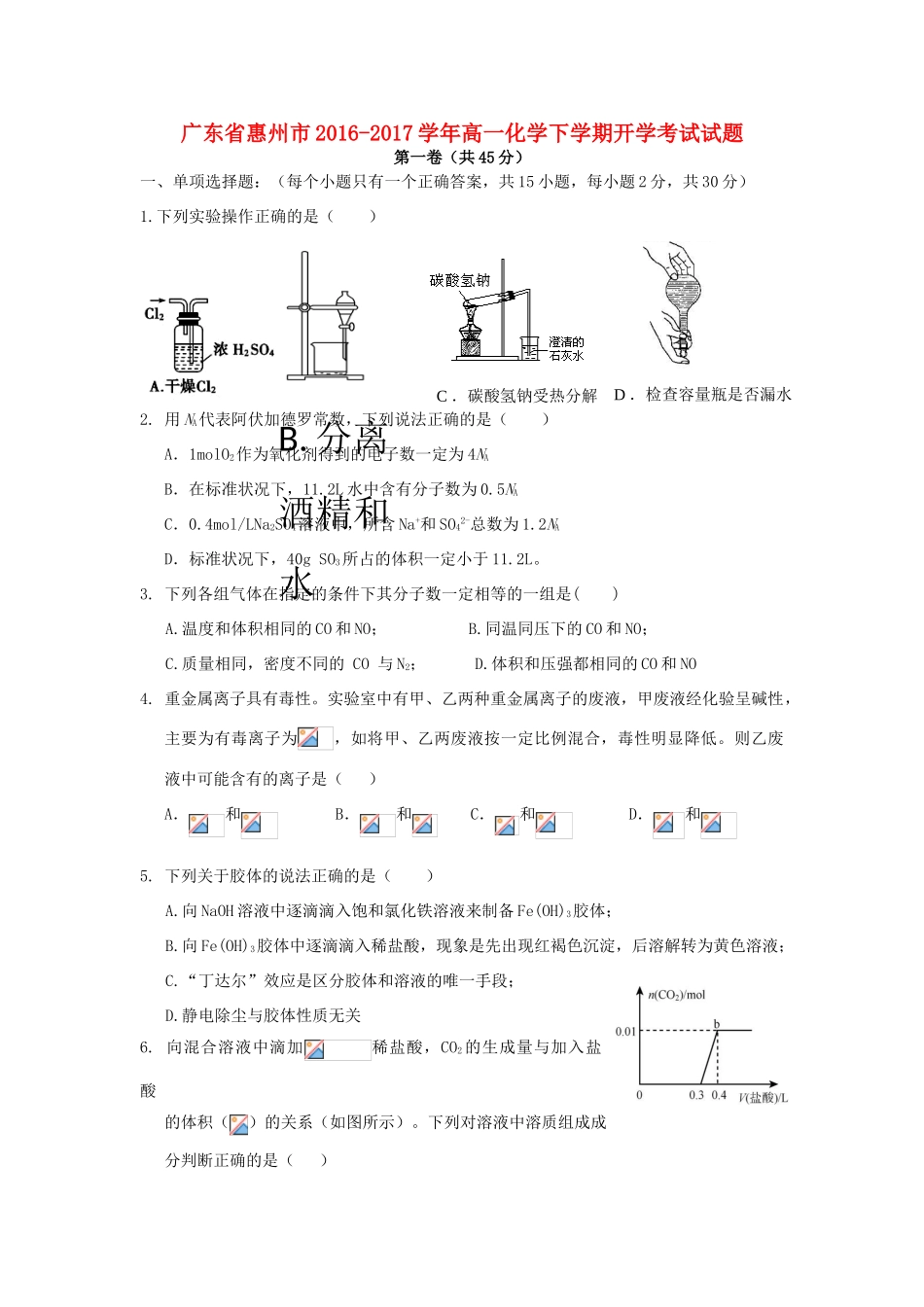
广东省惠州市2016-2017学年高一化学下学期开学考试试题第一卷(共45分)一、单项选择题:(每个小题只有一个正确答案,共15小题,每小题2分,共30分)1.下列实验操作正确的是()2.用NA代表阿伏加德罗常数,下列说法正确的是()A.1molO2作为氧化剂得到的电子数一定为4NAB.在标准状况下,11.2L水中含有分子数为0.5NAC.0.4mol/LNa2SO4溶液中,所含Na+和SO42-总数为1.2NAD.标准状况下,40gSO3所占的体积一定小于11.2L。3.下列各组气体在指定的条件下其分子数一定相等的一组是()A.温度和体积相同的CO和NO;B.同温同压下的CO和NO;C.质量相同,密度不同的CO与N2;D.体积和压强都相同的CO和NO4.重金属离子具有毒性。实验室中有甲、乙两种重金属离子的废液,甲废液经化验呈碱性,主要为有毒离子为,如将甲、乙两废液按一定比例混合,毒性明显降低。则乙废液中可能含有的离子是()A.和B.和C.和D.和5.下列关于胶体的说法正确的是()A.向NaOH溶液中逐滴滴入饱和氯化铁溶液来制备Fe(OH)3胶体;B.向Fe(OH)3胶体中逐滴滴入稀盐酸,现象是先出现红褐色沉淀,后溶解转为黄色溶液;C.“丁达尔”效应是区分胶体和溶液的唯一手段;D.静电除尘与胶体性质无关6.向混合溶液中滴加稀盐酸,CO2的生成量与加入盐酸的体积()的关系(如图所示)。下列对溶液中溶质组成成分判断正确的是()C.碳酸氢钠受热分解D.检查容量瓶是否漏水B.分离酒精和水A.原溶液中溶质为Na2CO3和NaHCO3B.原溶液中溶质为NaOH和Na2CO3C.原溶液中溶质为Na2CO3D.原溶液中溶质为NaHCO37.下列选项中的各操作,能使原溶液导电性明显变强的是()A.向0.1mol/L的NaOH溶液中加入等体积的0.1mol/L的HCl溶液;B.向0.1mol/L的NaOH溶液中加入等体积的0.1mol/L的CH3COOH溶液;C.向0.1mol/L的Ba(OH)2溶液中加入等体积的0.1mol/L的H2SO4溶液;D.向0.1mol/L的NH3·H2O溶液中加入等体积的0.1mol/L的CH3COOH溶液;8.根据下列反应:①2Fe2++Cl2=2Fe3++2Cl-②2Fe3++Cu=Cu2++2Fe2+③Fe+Cu2+=Fe2++Cu④HClO+H++Cl-=Cl2+H2O则判断下列各组物质的氧化性由强到弱的顺序正确的是()A.Cl2>Fe3+>HClO>Cu2+>Fe2+B.Cl2>HClO>Fe3+>Cu2+>Fe2+C.HClO>Cl2>Fe3+>Cu2+>Fe2+D.HClO>Fe3+>Cl2>Cu2+>Fe2+9.在一定条件下,分别以高锰酸钾、氯酸钾、过氧化氢为原料制取氧气,当制得同温、同压下相同体积的氧气时,三个反应中转移的电子数之比为()A.1:1:lB.2:2:1C.1:1:2D.4:3:210.漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年,亚氯酸(HClO2为弱酸)不稳定可分解,反应的离子方程式为:5HClO2=4ClO2↑+H++Cl-+2H2O。向NaClO2溶液中滴加H2SO4,开始时HClO2分解反应反应缓慢,随后反应迅速,其原因是()A.在酸性条件下,亚氯酸钠的氧化性增强B.溶液中的Cl-起催化作用C.ClO2逸出,使反应的生成物浓度降低D.溶液中的H+起催化作用11.下列各图示中能较长时间看到白色沉淀的是()A.①②④B.①②③C.①②D.②③④12.下列叙述中正确的是()A.液溴易挥发,在存放液溴的试剂瓶中应进行水封B.能使湿润的淀粉碘化钾试纸变成蓝色的物质一定是氯气C.某溶液中加入四氯化碳,下层紫色,证明原溶液中存在I-D.某溶液中加入BaCl2溶液,产生不溶于硝酸的白色沉淀,则该溶液中一定含有SO42-13.用4种溶液进行试验,下表中”操作及现象”与”溶液”不相符的是()选项操作及现象溶液A向溶液中通入SO2,溶液不变浑浊,再滴加氯水,溶液变浑浊BaCl2溶液B向溶液中通入SO2和SO3混合气体,溶液变浑浊,无任何气体产生Ba(NO3)2溶液C向溶液中通入SO2,溶液变浑浊,继续通入SO2至过量,浑浊消失,在加入足量NaOH溶液,又变浑浊Ca(OH)2溶液D向溶液中通入SO2,溶液紫色褪去KMnO4溶液14.一定温度下,1mol金属铜与足量某浓度的硝酸完全反应,生成NO2与NO的物质的量之比为1:3,则反应过程中转移的电子为()A.2molB.3molC.4molD.5mol15.已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液中,形成无色的溶液,其化学方程式是:PbSO4+2NH4Ac==Pb(Ac)2+(NH4)2SO4。当Pb(Ac)2(醋酸铅)溶液中通入H2S时,有黑色沉淀和弱电解质生成。表示这个反应的有关离子方程式正确的是()A.Pb(...