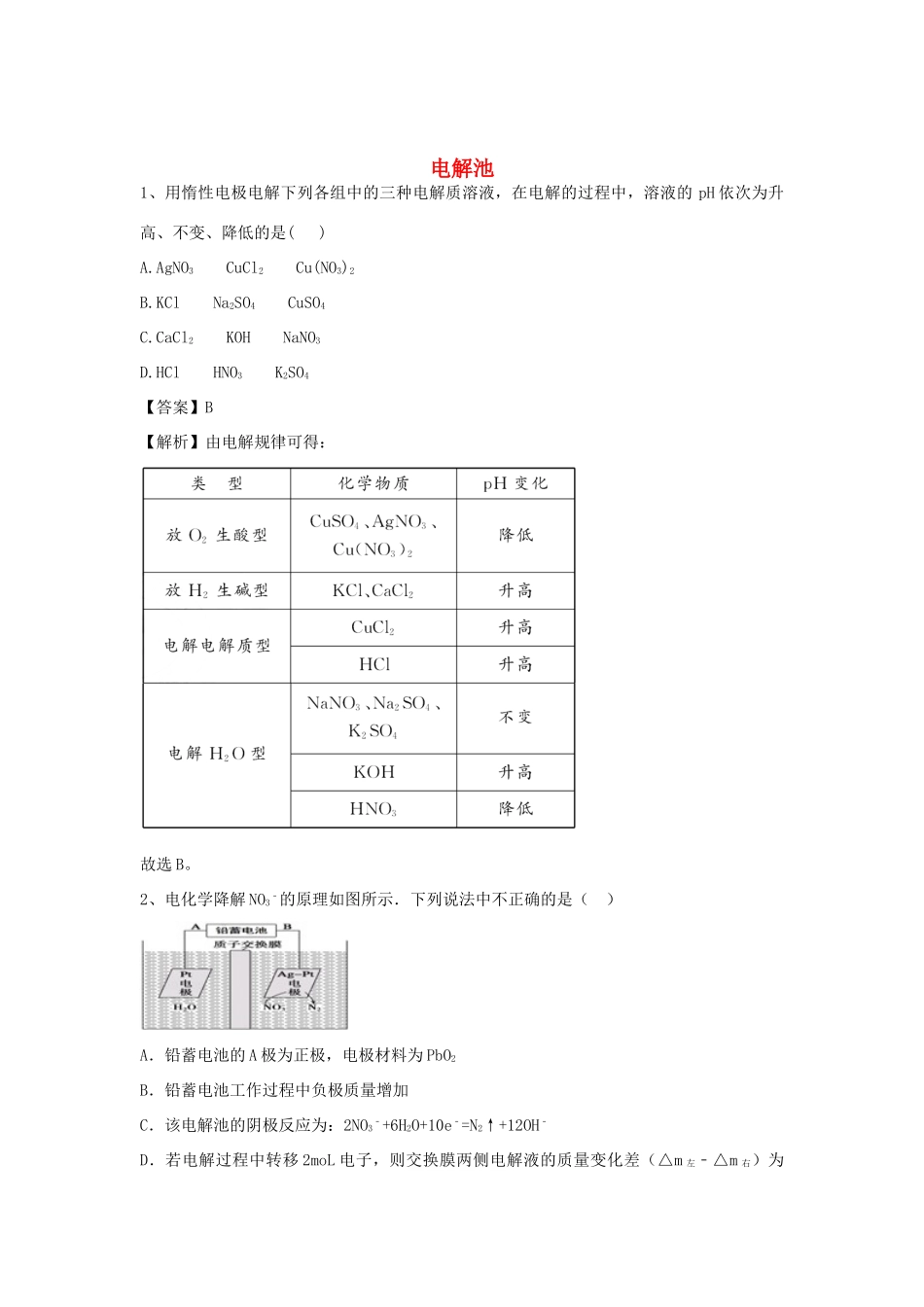
电解池1、用惰性电极电解下列各组中的三种电解质溶液,在电解的过程中,溶液的pH依次为升高、不变、降低的是()A.AgNO3CuCl2Cu(NO3)2B.KClNa2SO4CuSO4C.CaCl2KOHNaNO3D.HClHNO3K2SO4【答案】B【解析】由电解规律可得:故选B。2、电化学降解NO3﹣的原理如图所示.下列说法中不正确的是()A.铅蓄电池的A极为正极,电极材料为PbO2B.铅蓄电池工作过程中负极质量增加C.该电解池的阴极反应为:2NO3﹣+6H2O+10e﹣=N2↑+12OH﹣D.若电解过程中转移2moL电子,则交换膜两侧电解液的质量变化差(△m左﹣△m右)为10.4g【答案】D【解析】A.根据图知,电解槽右边部分N元素化合价由+5价变为0价,所以硝酸根离子发生还原反应,则Ag﹣Pt电极为阴极、Pt电极为阳极,所以A是正极、电极材料为PbO2,故A正确;B.铅蓄电池工作过程中负极为Pb失电子生成硫酸铅,所以负极质量增加,故B正确;C.阴极上硝酸根离子得电子发生还原反应,电极反应式为2NO3﹣+6H2O+10e﹣=N2↑+12OH﹣,故C正确;D.转移2mol电子时,阳极(阳极反应为H2O失电子氧化为O2和H+)消耗1mol水,产生2molH+进入阴极室,阳极室质量减少18g;阴极的电极反应式为2NO3﹣+6H++10e﹣=N2↑+6OH﹣,转移2mol电子,阴极室中放出0.2molN2(5.6g),同时有2molH+(2g)进入阴极室,因此阴极室质量减少3.6g,故膜两侧电解液的质量变化差(△m左﹣△m右)=18g﹣3.6g=14.4g,故D错误;故选D.3、如下图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。根据要求回答相关问题:(1)通入氧气的电极为________(填“正极”或“负极”),写出负极的电极反应式________________________________________________________________________________________________________________________________________________。(2)铁电极为________(填“阳极”或“阴极”),石墨电极(C)的电极反应式为________________________________________________________________________________________________________________________________________________。(3)反应一段时间后,乙装置中生成氢氧化钠主要在________(填“铁极”或“石墨极”)区,简述理由是________________________________________________________________________________________________________________________________________________。(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为________________________________________________________________________________________________________________________________________________,反应一段时间后,硫酸铜溶液浓度将________(填“增大”“减小”或“不变”)。(5)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为________;丙装置中阴极析出铜的质量为________。【答案】(1)正极CH3OCH3-12e-+16OH-===2CO32-+11H2O(2)阴极2Cl--2e-===Cl2↑(3)铁极石墨(C)极为阳极,氯离子发生氧化反应,铁极为阴极,H+反应生成H2,OH-过量,由于阳离子交换膜只允许钠离子向阴极区移动,故氢氧化钠主要在阴极区生成(4)Zn-2e-===Zn2+、Cu-2e-===Cu2+减小(5)0.2×6.02×102312.8g【解析】甲装置中甲醚(CH3OCH3)与氧气反应,甲醚被氧化,氧气被还原,故在正极通入氧气,在负极通入甲醚。甲醚在碱溶液中最终生成CO32-和H2O。乙装置中铁极与负极相连,铁极为阴极,石墨(C)极为阳极;丙装置中粗铜为阳极,与甲的正极相连,精铜为阴极。由于粗铜中含有锌等比铜活泼的金属,Zn2+得电子能力比Cu2+弱,根据电子守恒,阳极铜、锌失去电子总数等于阴极上析出的铜得电子总数,故硫酸铜溶液浓度会降低。n(O2)=0.1mol,O2+4e-+2H2O===4OH-,n(e-)=0.4mol,乙装置中,铁极为阴极,电极反应为2H++2e-===H2↑,根据电子守恒知,n(H2)=0.2mol,丙装置中阴极:Cu2++2e-===Cu,由电子守恒知,m(Cu)=0.2mol×64g/mol=12.8g。4、CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I-=2CuI↓+I2而得到。现以石墨为阴极,以Cu为阳极电解KI...