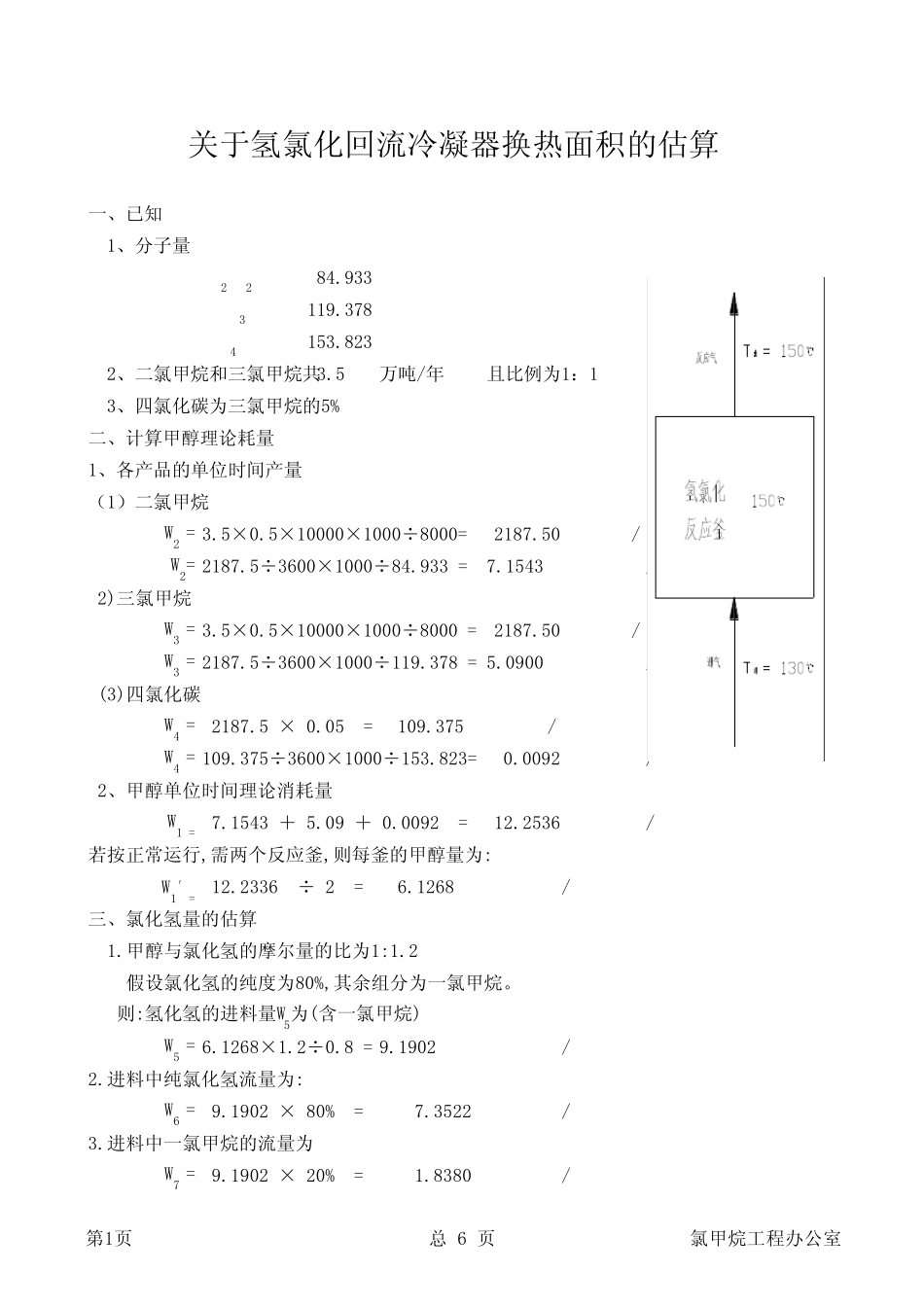
一、已知 1、分子量CH2Cl284
933CHCl3119
378CCl4153
823 2、二氯甲烷和三氯甲烷共3
5万吨/年且比例为1:1 3、四氯化碳为三氯甲烷的5%二、计算甲醇理论耗量1、各产品的单位时间产量(1)二氯甲烷W2 = 3
5×10000×1000÷8000=2187
50Kg/hW2= 2187
5÷3600×1000÷84
933 =7
1543mol/s 2)三氯甲烷W3 = 3
5×10000×1000÷8000 =2187
50Kg/hW3 = 2187
5÷3600×1000÷119
378 = 5
0900mol/s (3)四氯化碳W4 = 2187
05 =109
375Kg/hW4 = 109
375÷3600×1000÷153
0092mol/s 2、甲醇单位时间理论消耗量W1 = 7
1543 + 5
09 + 0
0092 =12
2536mol/s若按正常运行,需两个反应釜,则每釜的甲醇量为:W1′= 12
2336 ÷ 2 =6
1268mol/s三、氯化氢量的估算 1
甲醇与氯化氢的摩尔量的比为1:1
2 假设氯化氢的纯度为80%,其余组分为一氯甲烷
则:氢化氢的进料量W5为(含一氯甲烷)W5 = 6
1268×1
1902mol/s2
进料中纯氯化氢流量为:W6 = 9
1902 × 80% =7
3522mol/s3
进料中一氯甲烷的流量为W7 = 9
1902 × 20% =1
8380mol/s关于氢氯化回流冷凝器换热面积的估算第1页总 6 页氯甲烷工程办公室四、氢氯化反应釜出口气体的估算 假设甲醇的转化率为100%,一氯甲烷的选择性为100%1
一氯甲烷量CH3Cl = 6
1258+1
8380 =7
9648mol/s2
生成水H2O = 6