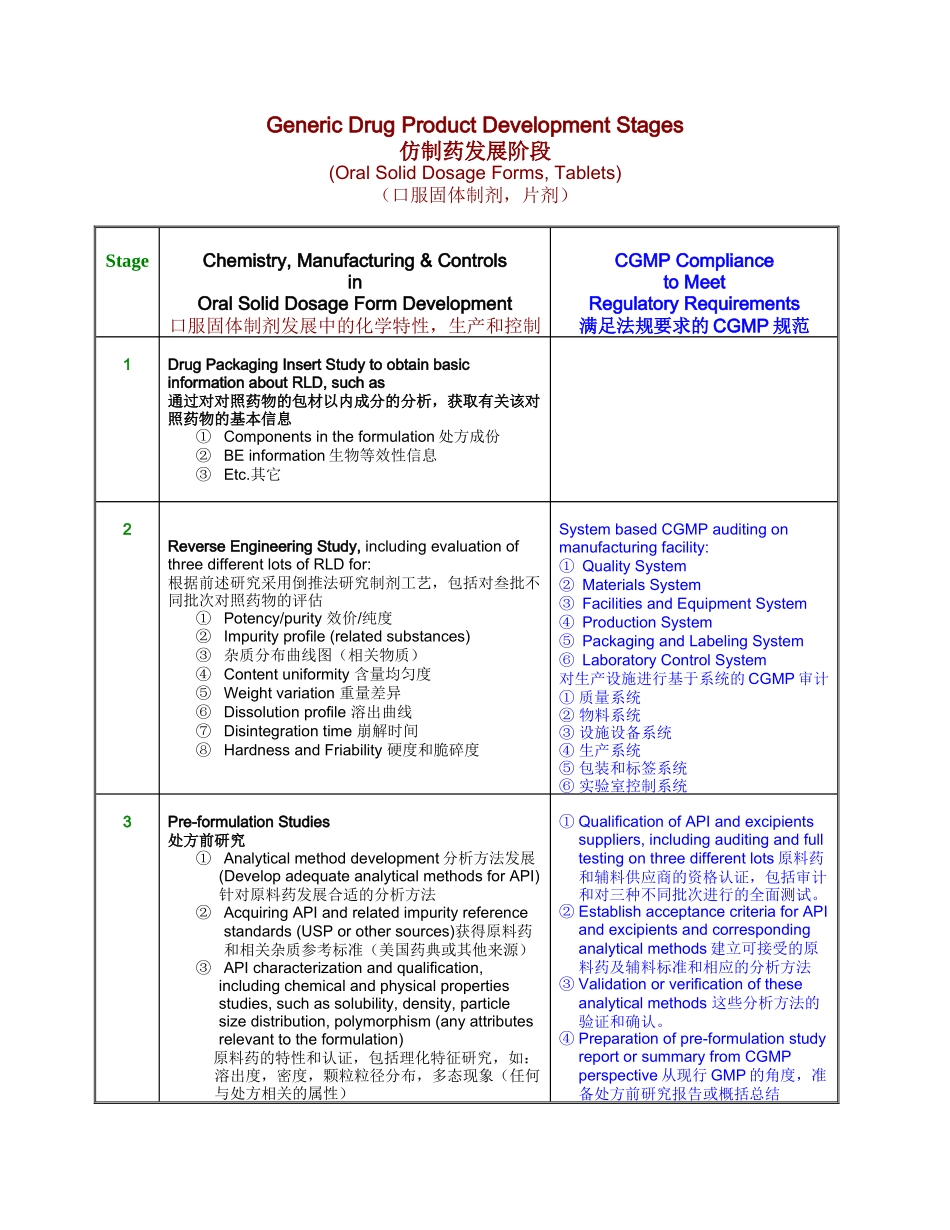
GenericDrugProductDevelopmentStages仿制药发展阶段(OralSolidDosageForms,Tablets)(口服固体制剂,片剂)StageChemistry,Manufacturing&ControlsinOralSolidDosageFormDevelopment口服固体制剂发展中的化学特性,生产和控制CGMPCompliancetoMeetRegulatoryRequirements满足法规要求的CGMP规范1DrugPackagingInsertStudytoobtainbasicinformationaboutRLD,suchas通过对对照药物的包材以内成分的分析,获取有关该对照药物的基本信息①Componentsintheformulation处方成份②BEinformation生物等效性信息③Etc
其它2ReverseEngineeringStudy,includingevaluationofthreedifferentlotsofRLDfor:根据前述研究采用倒推法研究制剂工艺,包括对叁批不同批次对照药物的评估①Potency/purity效价/纯度②Impurityprofile(relatedsubstances)③杂质分布曲线图(相关物质)④Contentuniformity含量均匀度⑤Weightvariation重量差异⑥Dissolutionprofile溶出曲线⑦Disintegrationtime崩解时间⑧HardnessandFriability硬度和脆碎度SystembasedCGMPauditingonmanufacturingfacility:①QualitySystem②MaterialsSystem③FacilitiesandEquipmentSystem④ProductionSystem⑤P