第十七章 碱金属和碱土金属 [教学要求] 1.熟悉碱金属和碱土金属的通性;了解碱金属和碱土金属的单质及物理性质和化学性质
2.了解M + 和M 2+离子的特征;熟悉氧化物、氧氢化物、盐类
[教学重点] 1.碱金属和碱土金属的通性
2.氧化物、氧氢化物、盐类
[教学难点] 1.碱金属和碱土金属的单质及物理性质和化学性质
2.M + 和M 2+离子的特征
[教学时数] 2 学时 [教学内容] 碱金属和碱土金属是周期表ⅠA族和ⅡA族元素
ⅠA族包括锂、钠、钾、铷、铯、钫六种金属元素
它们的氧化物溶于水呈碱性,所以称为碱金属
ⅡA族包括铍、镁、钙、锶、钡、镭六种金属元素
由于钙、锶、钡的氧化物在性质上介于“碱性的”和“土性的”(以前把粘土的主要成分,既难溶于水又难熔融的Al2O3称为“土”)之间
其中锂、铷、铯、铍是稀有金属,钫和镭是放射性元素
钠、钾、镁、钙和钡在地壳内蕴藏较丰富,它们的单质和化合物用途广泛,本章将重点介绍它们
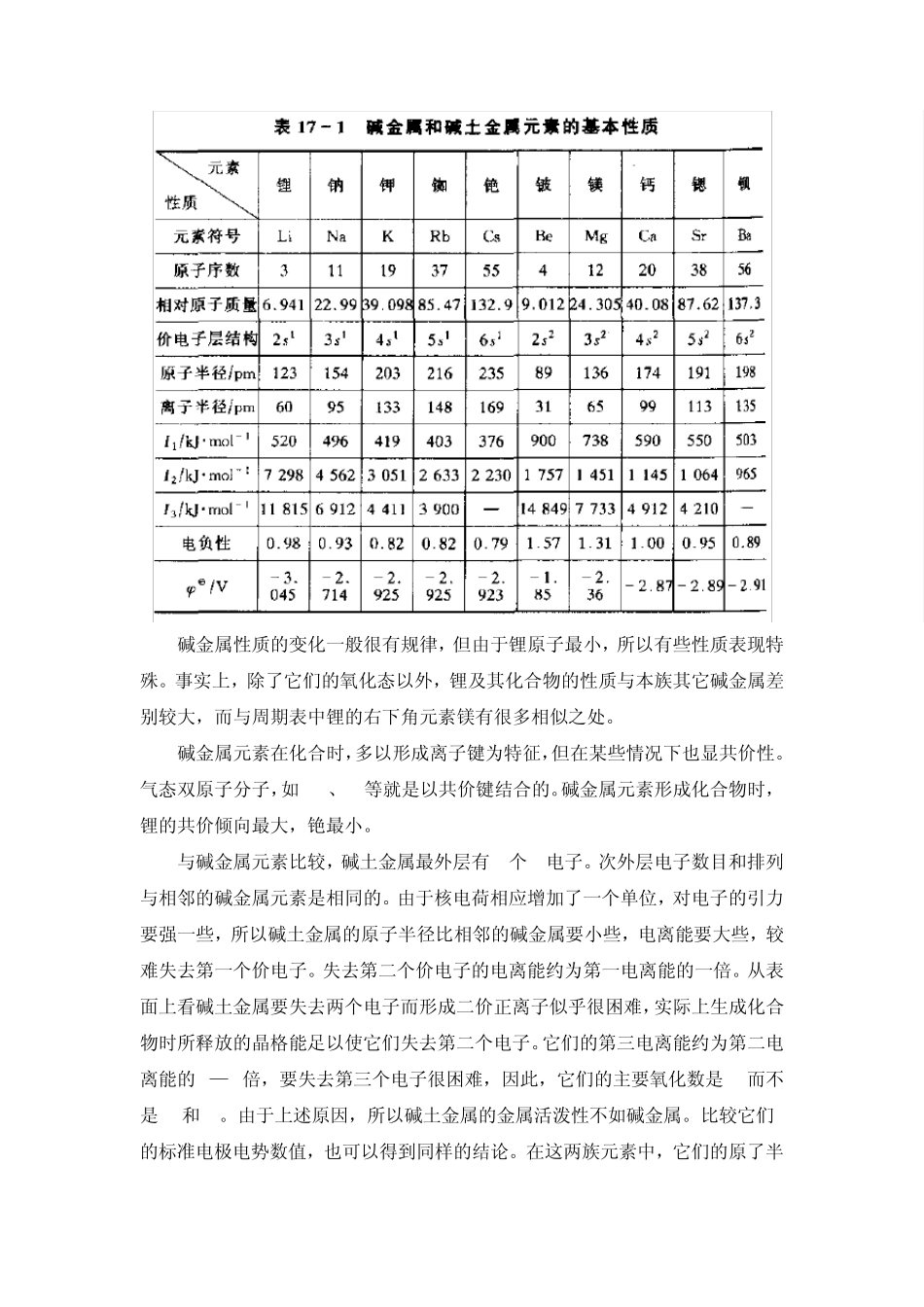
§17-1 碱金属和碱土金属的通性 表17—1列举了碱金属和碱土金属的一些重要性质
碱金属元素原子的价电子层结构为ns1
因此,碱金属元素只有+1氧化态
碱金属原子最外层只有一个电子,次外层为8电子(Li为2电子),对核电荷的屏蔽效应较强,所以这一个价电子离核校远,特别容易失去,因此,各周期元素的第一电离能以碱金属为最低
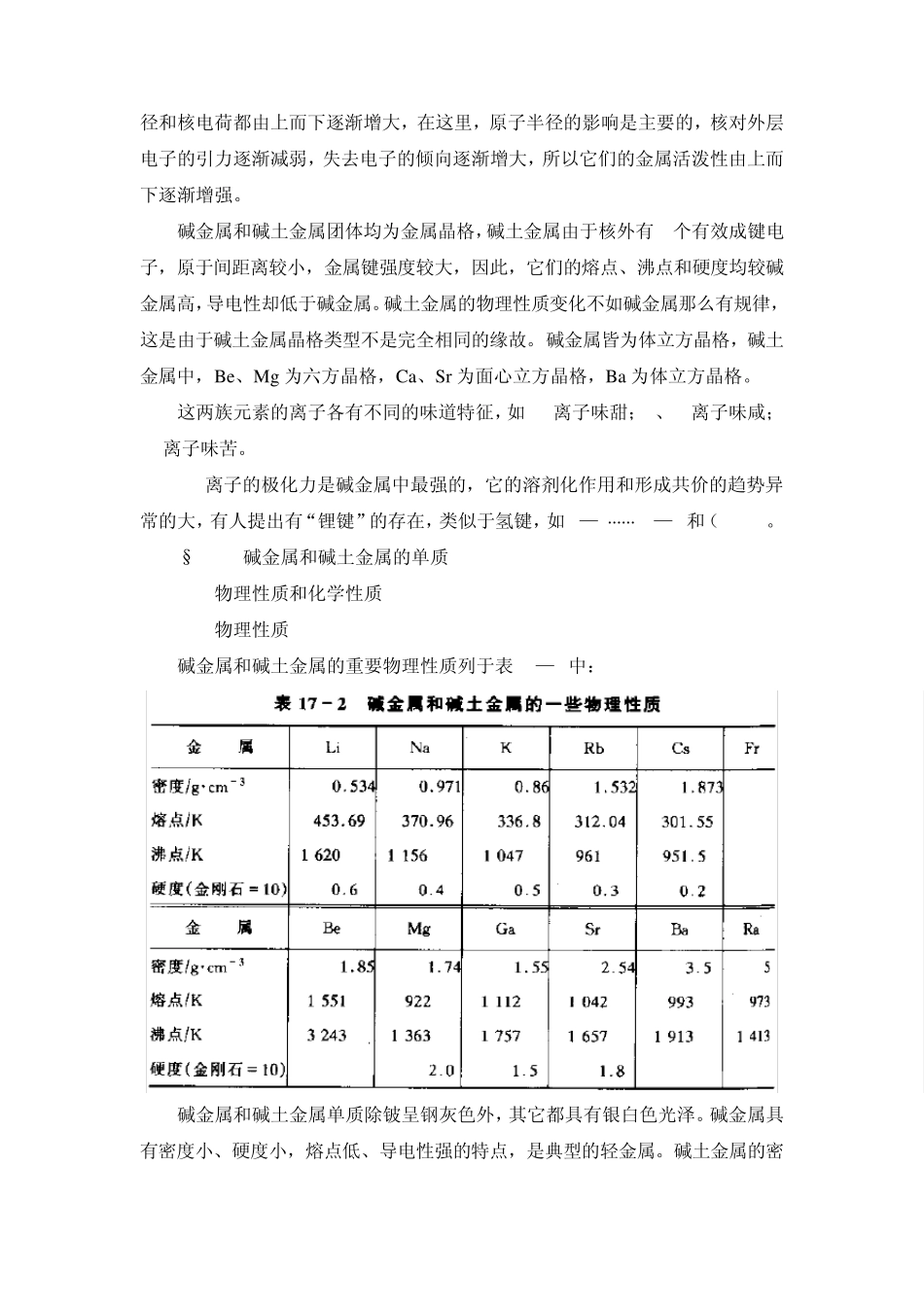
与同周期的元素比较,碱金属原子体积最大,只有一个成键电子,在固体中原子间的引力较小,所以它们的熔点、沸点、硬度、升华热都很低,并随着 Li一 Na—K一 Rb一 Cs的顺序而下降
随着原子量的增加(即原子半径增加),电离能和电负性也依次降低,见表17—1
碱金属性质的变化一般很有规律,但由于锂原子最小,所以有些性质表现特殊
事实上,除了它们的氧化态以外,锂及其化合物的性质与本族其它碱金属差别较大,而与周期表中锂的右下角元