2011 届高考化学二轮专题复习学案:2
2 化学反应速率和化学平衡(新课标)【考纲点击】1
了解化学反应速率的概念,反应速率的定量表示方法
了解催化剂在生产、生活和科学研究领域中的重大作用
理解外界条件(浓度、温度、压强、催化剂等)对反应速率的影响,认识其一般规律
了解化学反应速率的调控在生活、生产和科学研究领域中的作用
了解化学反应的可逆性
了解化学平衡建立的过程
理解化学平衡常数的含义,能够利用化学平衡常数进行简单的计算
理解外界条件(温度、压强、催化剂)对化学反应平衡的影响,认识其一般规律
了解化学平衡的调控在生活、生产和科学研究领域中的重要作用
【核心要点突破】一、可逆反应达到平衡状态的判据点拨:例举反应mA(g)+nB(g) pC(g)’qD(g)是否平衡状态混合物体系中各成① 各物质的物质的量或各物质的物质的量的分数一定② 各物质的质量或各物质质量分数一定③ 各气体的体积或体积分数一定是④ 总体积、总压力、总物质的量一定不一定正反应速率与逆反应速率的关系① 在单位时间内消耗了 m mol A 同时生成,m molA,即 V 正=V 逆是② 在单位时间内消耗了 n molB 同时消耗了 p mol C
则 V 正=V逆是③VA:VB:VC:VD=m:n:p:q,V 正不一定等于 V 逆不一定④ 在单位时问内生成 n mol B
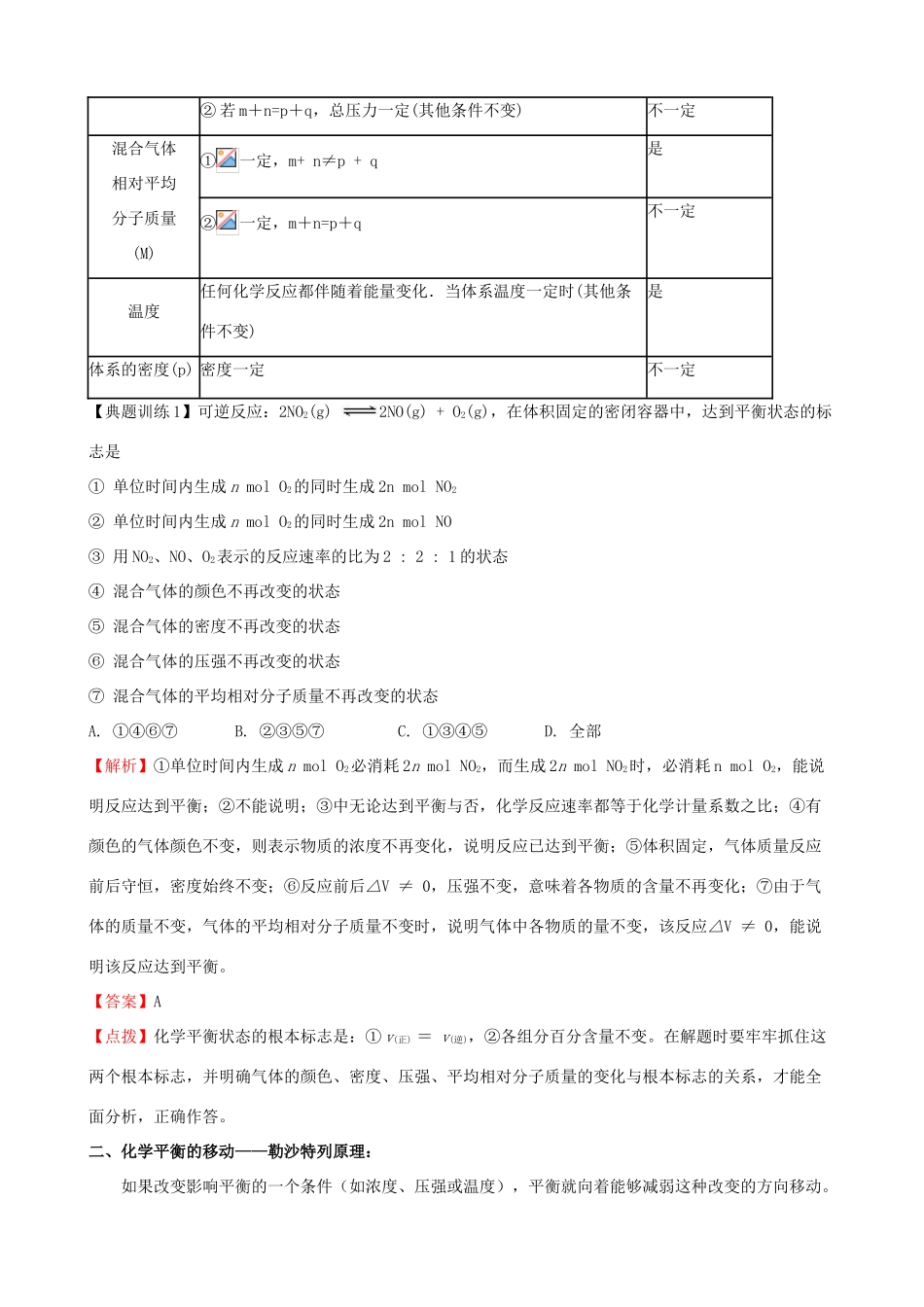
同时消耗 q mol D,因均指 V 逆 不一定压强①m+ n≠p + q 时
总压力一定(其他条件不变)是② 若 m+n=p+q,总压力一定(其他条件不变)不一定混合气体相对平均分子质量(M)①一定,m+ n≠p + q是②一定,m+n=p+q不一定温度任何化学反应都伴随着能量变化.当体系温度一定时(其他条件不变)是体系的密度(p) 密度一定不一定【典题训练 1】可逆反应:2NO2(g) 2NO(g