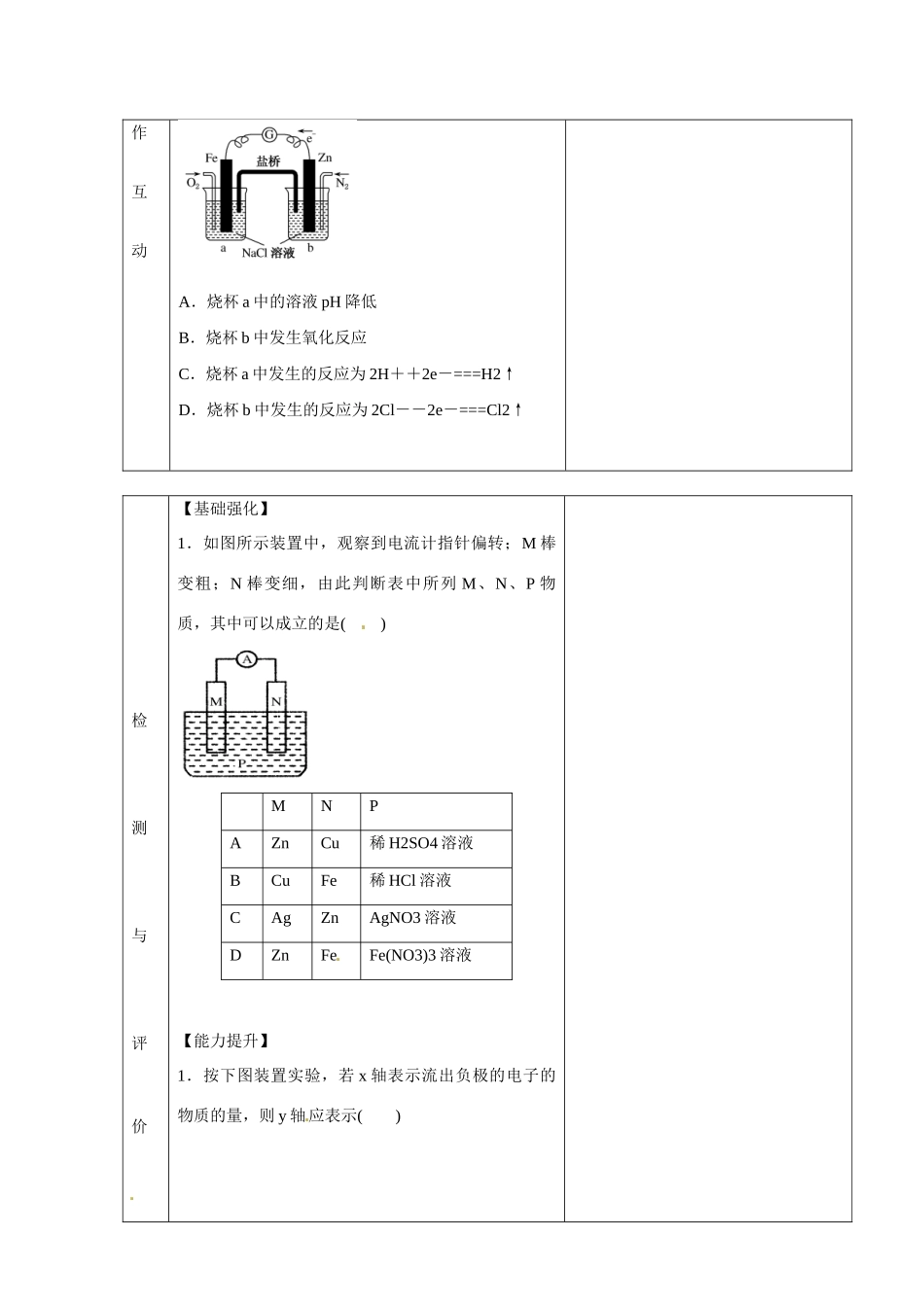
甘肃省金昌市第一中学 2014 年高中化学 4-1-3 原电池导学案 新人教版选修 4 学习目标1.能够正确熟练书写电极反应方程式。2.理解并掌握原电池原理在化学中的应用。学习重点理解并掌握原电池原理在化学中的应用学习难点理解并掌握原电池原理在化学中的应用 精讲与点拨自主研讨【自主学习】二、电池正、负极的判断根据组成原电池的电极材料判断:一般由 作负极,活泼性较弱的金属或能够导电的非金属材料(如石墨、碳棒等)作 极。根据电流方向或电子流动方向判断:提供电子的电极(电子流出的电极)为 极;接受电 子的电极(电子流入的电极)为 极。即电流由正极流向负极,电子是由负极流向正极。(3)根据两电极发生的变化来判断:负极 电子,发生 反应;正极 电子,发生 反应。根据电解质溶液中离子的定向移动方向来判断:阳离子移向的电极是 极,阴离子移向的电极是 极。根据一般现象来判断:溶解的一极为 极,质量增加或放出气体的一极为 极。合 【例题精讲】例 1:根据下图,下列判断中正确的是( )作互动A.烧杯 a 中的溶液 pH 降低B.烧杯 b 中发生氧化反应C.烧杯 a 中发生的反应为 2H++2e-===H2↑D.烧杯 b 中发生的反应为 2Cl--2e-===Cl2↑ 检测与评价【基础强化】1.如图所示装置中,观察到电流计指针偏转;M 棒变粗;N 棒变细,由此判断表中所列 M、N、P 物质,其中可以成立的是( )MNPAZnCu稀 H2SO4 溶液BCuFe稀 HCl 溶液CAgZnAgNO3 溶液DZnFeFe(NO3)3 溶液【能力提升】1.按下图装置实验,若 x 轴表示流出负极的电子的物质的量,则 y 轴应表示( )①c(Ag+) ② c(NO) ③ a 棒的质量 ④ b 棒的质量 ⑤溶液的质量A.①③ B.③④ C.①②④ D.②课后反思: