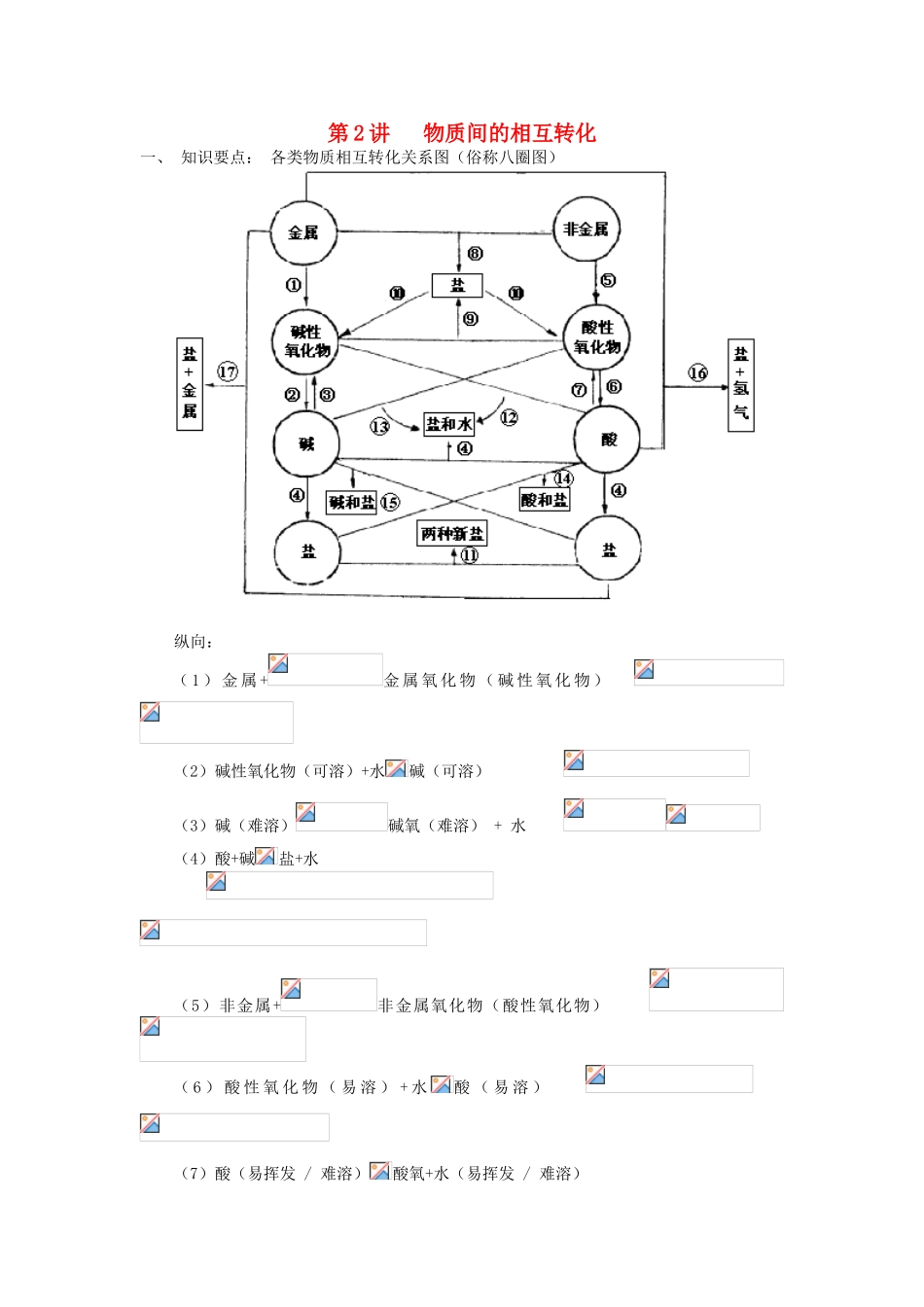
第 2 讲 物质间的相互转化一、 知识要点: 各类物质相互转化关系图(俗称八圈图)纵向:( 1 ) 金 属 +金 属 氧 化 物 ( 碱 性 氧 化 物 ) (2)碱性氧化物(可溶)+水碱(可溶)(3)碱(难溶)碱氧(难溶) + 水(4)酸+碱盐+水 (5)非金属+非金属氧化物(酸性氧化物) ( 6 ) 酸 性 氧 化 物 ( 易 溶 ) + 水酸 ( 易 溶 ) (7)酸(易挥发 / 难溶)酸氧+水(易挥发 / 难溶) 从纵向来看,金属碱性氧化物碱盐,碱系列非金属酸性氧化物酸(含氧酸)盐,酸系列横向:(8)金属+非金属(无氧酸)盐 (9)碱氧+酸氧(含氧酸)盐(10)含氧酸盐碱氧+酸氧(11)盐+盐两种新盐(12)酸+碱氧盐+水(13)碱+酸氧盐+水(14)酸+盐新酸+新盐 (15)碱+盐新碱+新盐(16)金属+酸盐+(17)金属+盐新盐+新金属二、化学反应发生的条件(一) 复分解反应的发生条件1
复分解反应需在溶液里才可能发生,在固态时无自由移动的离子时不发生反应
但即使在溶液里,还要看生成物是否满足下列条件之一: ① 产生沉淀 ② 放出气体 ③ 生成难电离的水2
复分解反应常发生在下列几条反应规律中:① 酸+碱盐+水② 酸+碱性氧化物盐+水③ 碱+酸性氧化物盐+水④ 酸+盐新酸+新盐⑤ 碱+盐新碱+新盐(反应物的碱和盐均要溶于水)⑥ 盐+盐两种新盐(反应物均要溶于水)对于盐+酸新盐+新酸,有如下规律:① 较强酸较弱酸(强制弱)如: ② 高沸点(不易挥发的)酸低沸点(易挥发的)酸
酸、碱、盐的溶解性规律(溶解性口诀)酸溶碱难溶,盐要分别看钾、钠、铵盐,硝酸盐,完全溶解不困难碳酸、磷酸、亚硫酸、硅酸以及氢硫酸,只溶钾、钠、铵盐酸不溶银、亚汞,硫酸不溶银、钙、钡、铅(二)
金属活动顺序表及其使用范围:(1)金属活动顺序: (2)在金属活动性顺序里,位于氢以前的较