课时23电解池及其应用能力摸底课前热身1
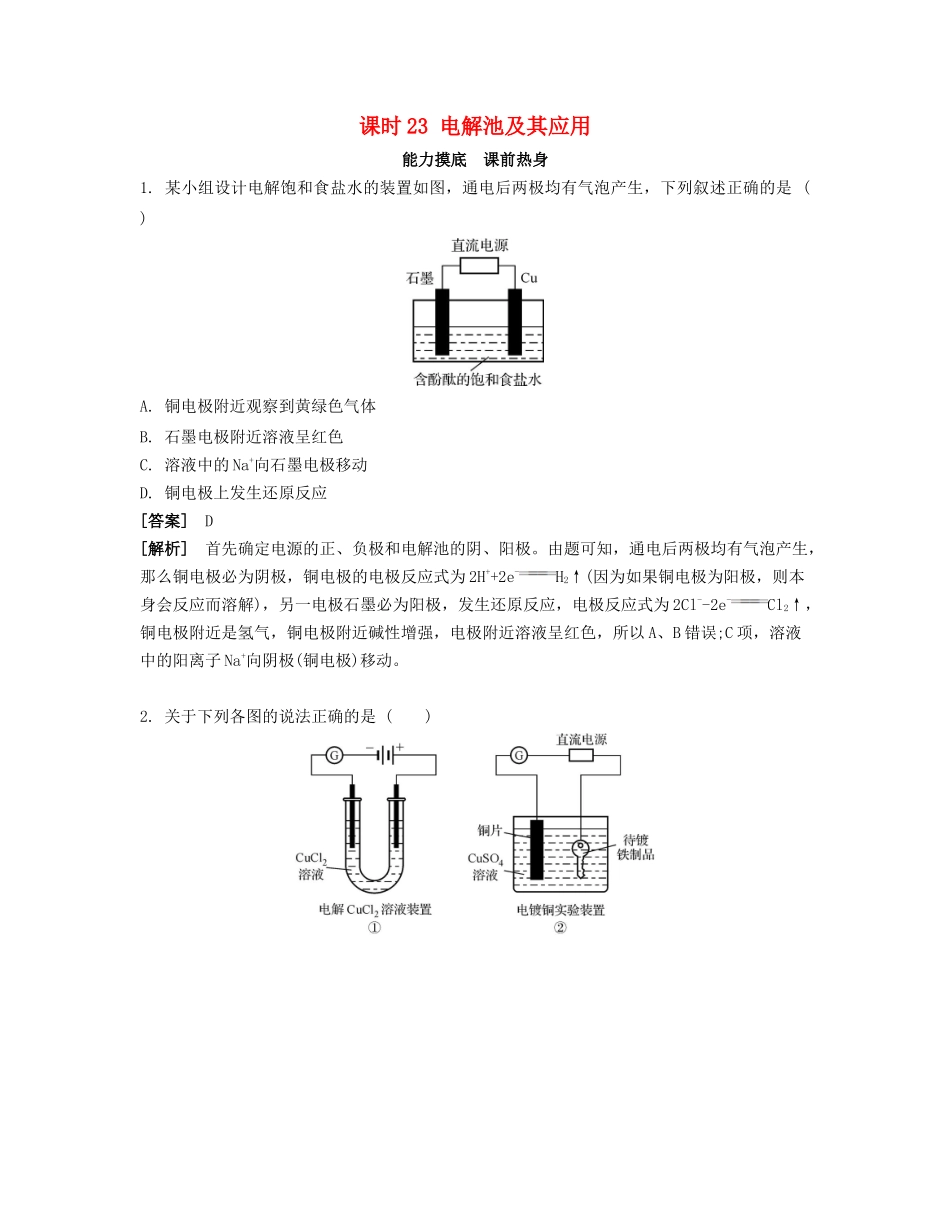
某小组设计电解饱和食盐水的装置如图,通电后两极均有气泡产生,下列叙述正确的是()A
铜电极附近观察到黄绿色气体B
石墨电极附近溶液呈红色C
溶液中的Na+向石墨电极移动D
铜电极上发生还原反应[答案]D[解析]首先确定电源的正、负极和电解池的阴、阳极
由题可知,通电后两极均有气泡产生,那么铜电极必为阴极,铜电极的电极反应式为2H++2e-H2↑(因为如果铜电极为阳极,则本身会反应而溶解),另一电极石墨必为阳极,发生还原反应,电极反应式为2Cl--2e-Cl2↑,铜电极附近是氢气,铜电极附近碱性增强,电极附近溶液呈红色,所以A、B错误;C项,溶液中的阳离子Na+向阴极(铜电极)移动
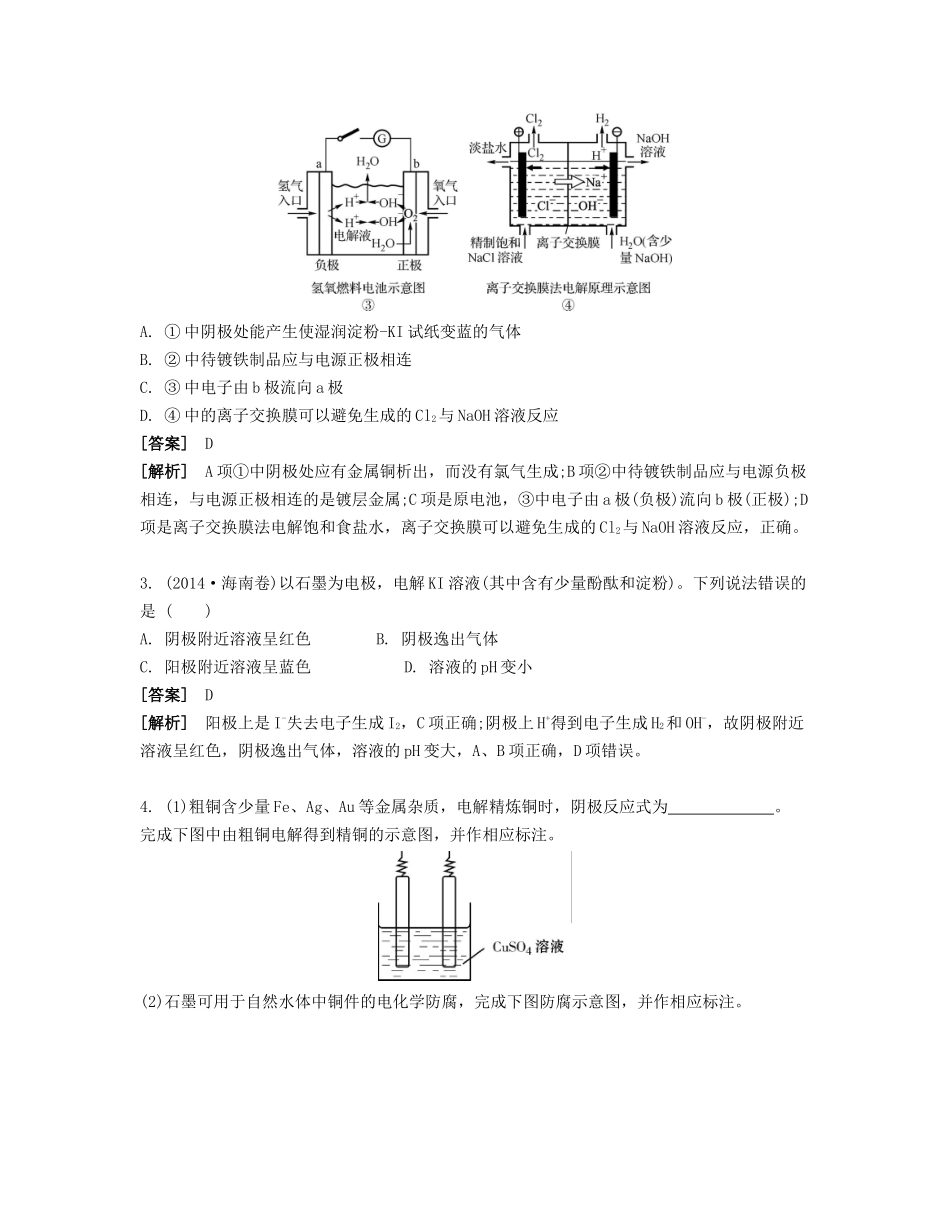
关于下列各图的说法正确的是()A
①中阴极处能产生使湿润淀粉-KI试纸变蓝的气体B
②中待镀铁制品应与电源正极相连C
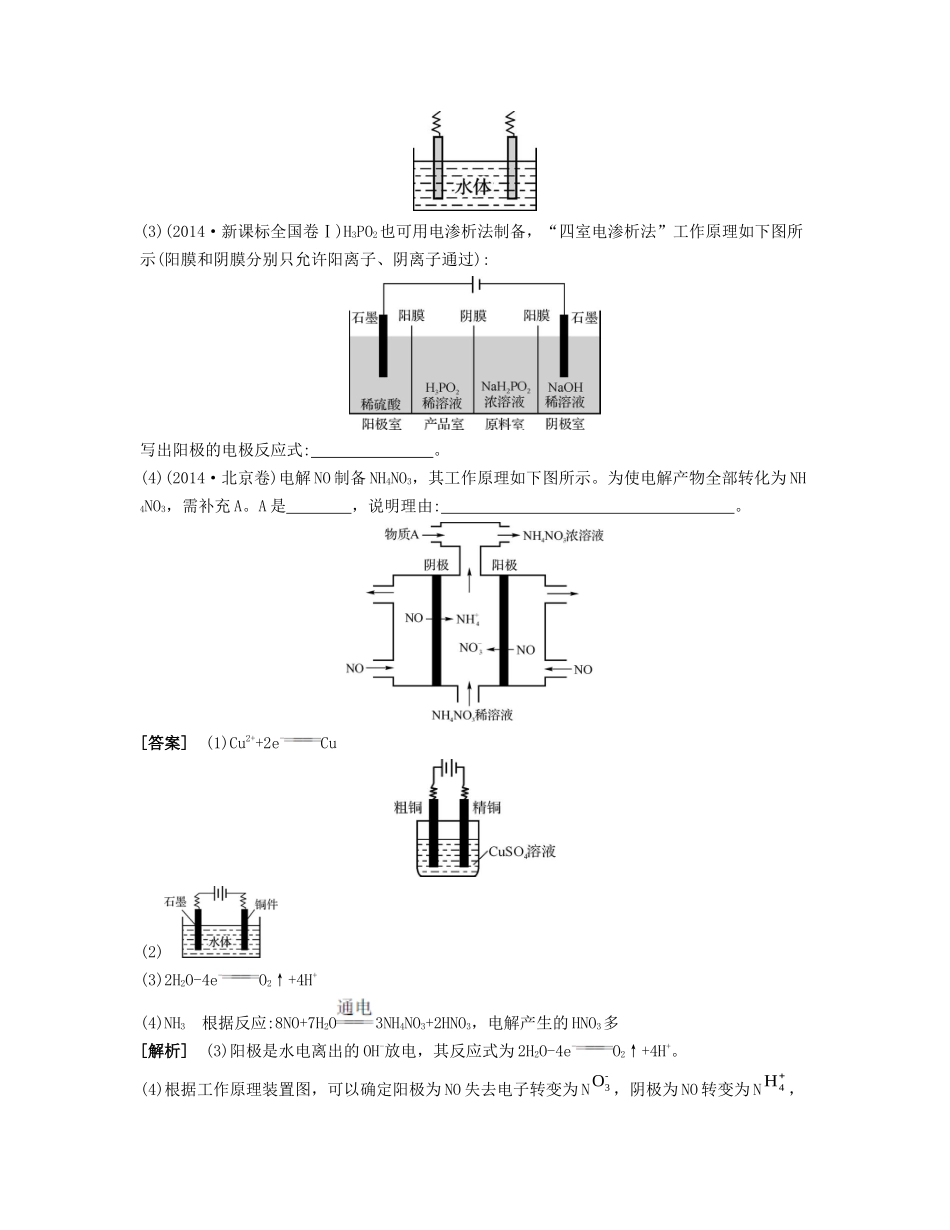
③中电子由b极流向a极D
④中的离子交换膜可以避免生成的Cl2与NaOH溶液反应[答案]D[解析]A项①中阴极处应有金属铜析出,而没有氯气生成;B项②中待镀铁制品应与电源负极相连,与电源正极相连的是镀层金属;C项是原电池,③中电子由a极(负极)流向b极(正极);D项是离子交换膜法电解饱和食盐水,离子交换膜可以避免生成的Cl2与NaOH溶液反应,正确
(2014·海南卷)以石墨为电极,电解KI溶液(其中含有少量酚酞和淀粉)
下列说法错误的是()A
阴极附近溶液呈红色B
阴极逸出气体C
阳极附近溶液呈蓝色D
溶液的pH变小[答案]D[解析]阳极上是I-失去电子生成I2,C项正确;阴极上H+得到电子生成H2和OH-,故阴极附近溶液呈红色,阴极逸出气体,溶液的pH变大,A、B项正确,D项错误
(1)粗铜含少量Fe、Ag、Au等金属杂质,电解精炼铜时,阴极反应式为
完成下图中由粗铜电解得到精铜的示意图,并作相应标注
(2)石墨可用于自然水