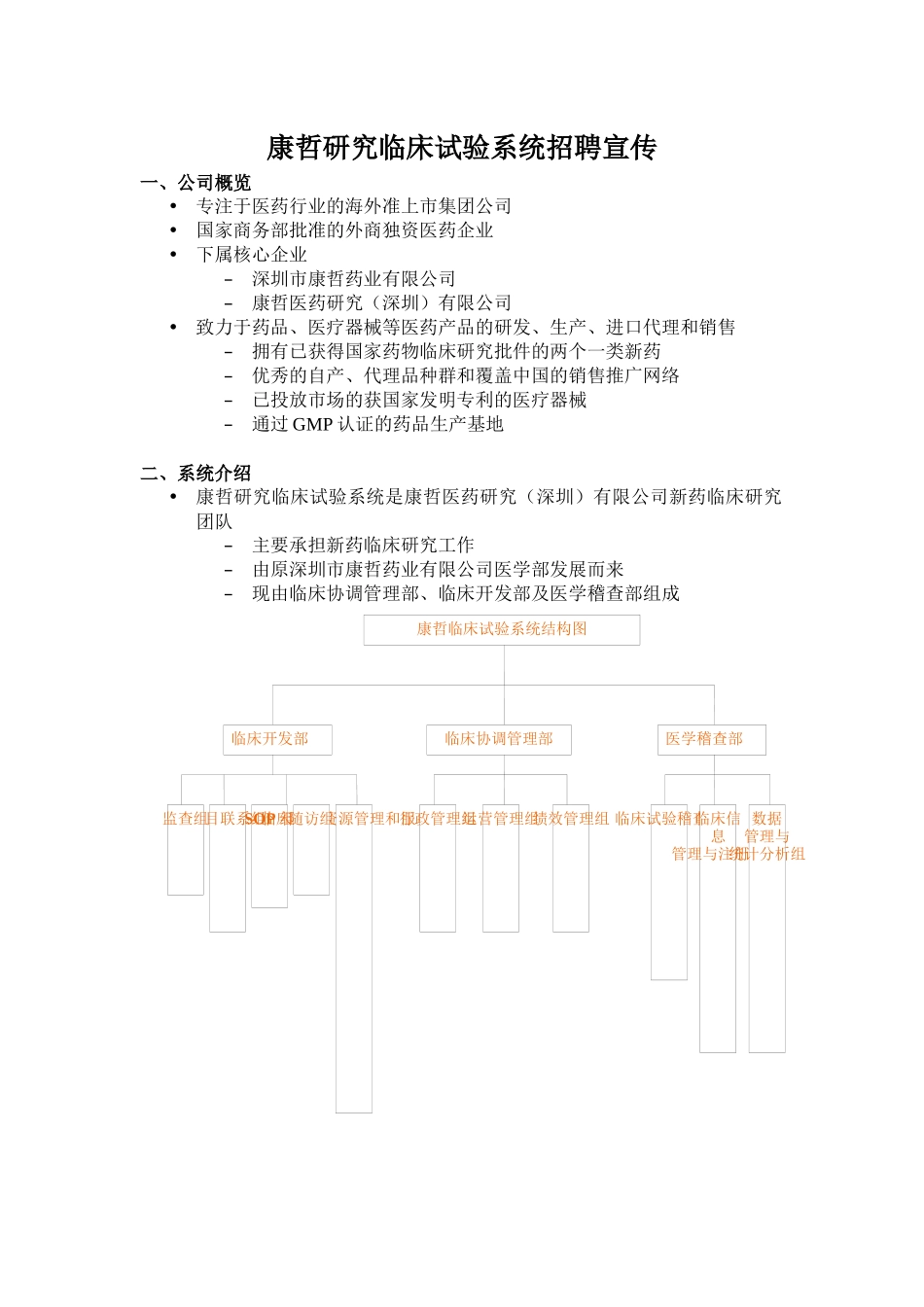
康哲临床试验系统结构图临床开发部医学稽查部临床协调管理部SOP组项目联系组临床专家资源管理和服务组临床试验稽查组临床信息管理与注册组数据管理与统计分析组绩效管理组运营管理组行政管理组监查组随访组康哲研究临床试验系统招聘宣传一、公司概览•专注于医药行业的海外准上市集团公司•国家商务部批准的外商独资医药企业•下属核心企业–深圳市康哲药业有限公司–康哲医药研究(深圳)有限公司•致力于药品、医疗器械等医药产品的研发、生产、进口代理和销售–拥有已获得国家药物临床研究批件的两个一类新药–优秀的自产、代理品种群和覆盖中国的销售推广网络–已投放市场的获国家发明专利的医疗器械–通过GMP认证的药品生产基地二、系统介绍•康哲研究临床试验系统是康哲医药研究(深圳)有限公司新药临床研究团队–主要承担新药临床研究工作–由原深圳市康哲药业有限公司医学部发展而来–现由临床协调管理部、临床开发部及医学稽查部组成康哲研究临床试验系统职位解析图康哲医药研究(深圳)有限公司副总经理临床开发部经理医学稽查部经理临床协调管理部经理SOP专员项目联系专员专家维护专员临床稽查员信息专员统计专员绩效管理专员运营管理专员行政管理专员高级监查员随访专员监查员三、2007年度临床试验系统招聘总则•专业–西医临床(其中数据管理与统计分析专员要求专业为医学统计学专业)•学历–硕士研究生或以上(应聘临床监查员岗位可为本科)•工作地点–临床监查员工作地点为全国范围–其余岗位工作地点为深圳四、待聘岗位介绍(一)临床监查员工作职责:1、跟踪、监查并协调临床试验的全过程,收集、整理相关数据并完成试验报告
2、与医院或研究机构保持良好的合作关系
任职要求:1、临床医学专业、硕士以上学历,熟悉GCP规范
2、良好的沟通和协作能力,良好的团队合作精神
工作地点:北京、上海、天津、成都、西安、武汉、南京、广州、深圳等地招聘人数:9人(二)临床稽查员