第三章物质在水溶液中的行为第3节沉淀溶解平第1课时衡【教学目标】1.知识与技能:关注难溶电解质在水溶液中的化学行为,初步运用平衡移动原理,认识沉淀溶解平衡的主要特征,理解Ksp的含义及其初步应用
2.过程与方法:通过学生提问、讨论和总结,结合实验探究,认识难溶电解质在水溶液中的化学行为,在对沉淀的生成、溶解和转化体验及分析中认识难溶电解质(沉淀)溶解平衡的主要特征学会从离子浓度积Qc与溶度积Ksp大小关系上判断沉淀溶解平衡的移动方向,培养学生分析问题、解决问题的能力
3.情感、态度与价值观:通过探究活动,让学生体验沉淀溶解平衡状态的存在及其移动方向的确定方法,树立对立统一的思想,激发求知的兴趣和求真求是的态度
培养学生学会探究、思考、合作、交流、创新的品质
【教学过程】一、沉淀溶解平衡1.概念在一定条件下,当难溶固体溶解的速率与离子结合成难溶固体的速率相等时,溶液中离子浓度、固体的量保持不变的状态
2.特点(1)动:沉淀溶解平衡是一种动态平衡
(2)等:v(沉淀)=v(溶解)≠0
(3)定:平衡时,离子浓度不变,固体的量不变
(4)变:改变影响平衡的条件,平衡被破坏,会发生沉淀的溶解、生成或转化
3.表示方法如PbI2的沉淀溶解平衡,可表示为PbI2(s)Pb2+(aq)+2I-(aq)
二、溶度积常数1.定义在一定条件下,难溶物质的饱和溶液中,存在沉淀溶解平衡,其平衡常数叫做溶度积常数或溶度积,符号为Ksp
2.表达式以PbI2沉淀溶解平衡为例:PbI2(s)Pb2+(aq)+2I-(aq),Ksp=[Pb2+][I-]2
3.意义溶度积(Ksp)反映了难溶电解质在水中的溶解能力
对于阴阳离子个数比相同的弱电解质,Ksp的数值越大,电解质在水中的溶解能力越强
4.影响因素:Ksp只与难溶电解质的性质和温度有关,与沉淀的量和溶液中离子的浓度无关
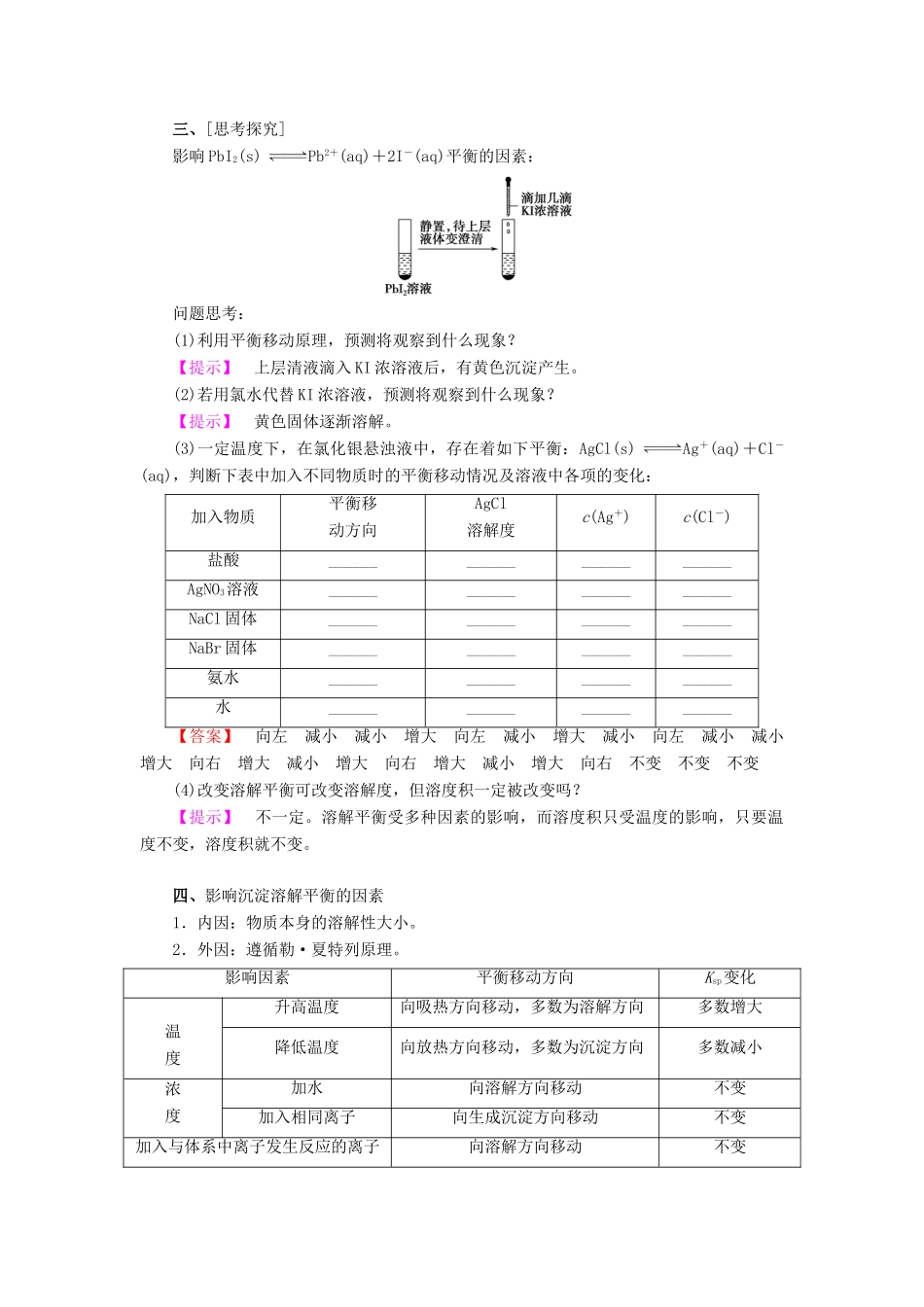
三、[思考探究]影响PbI2