第四节金属的电化学腐蚀与防护[明确学习目标]1
了解金属腐蚀及其危害
了解金属电化学腐蚀的原因及反应原理
了解金属防护的一般方法,特别是电化学防护的方法
一、金属的电化学腐蚀1.金属的腐蚀金属腐蚀是指金属与周围的□气体或液体物质发生□氧化还原反应而引起损耗的现象
一般可分为□化学腐蚀和□电化学腐蚀
2.钢铁的电化学腐蚀二、金属的电化学防护1.牺牲阳极的阴极保护法应用□原电池原理,让被保护金属作□正极,另找一种活泼性较强的金属作□负极
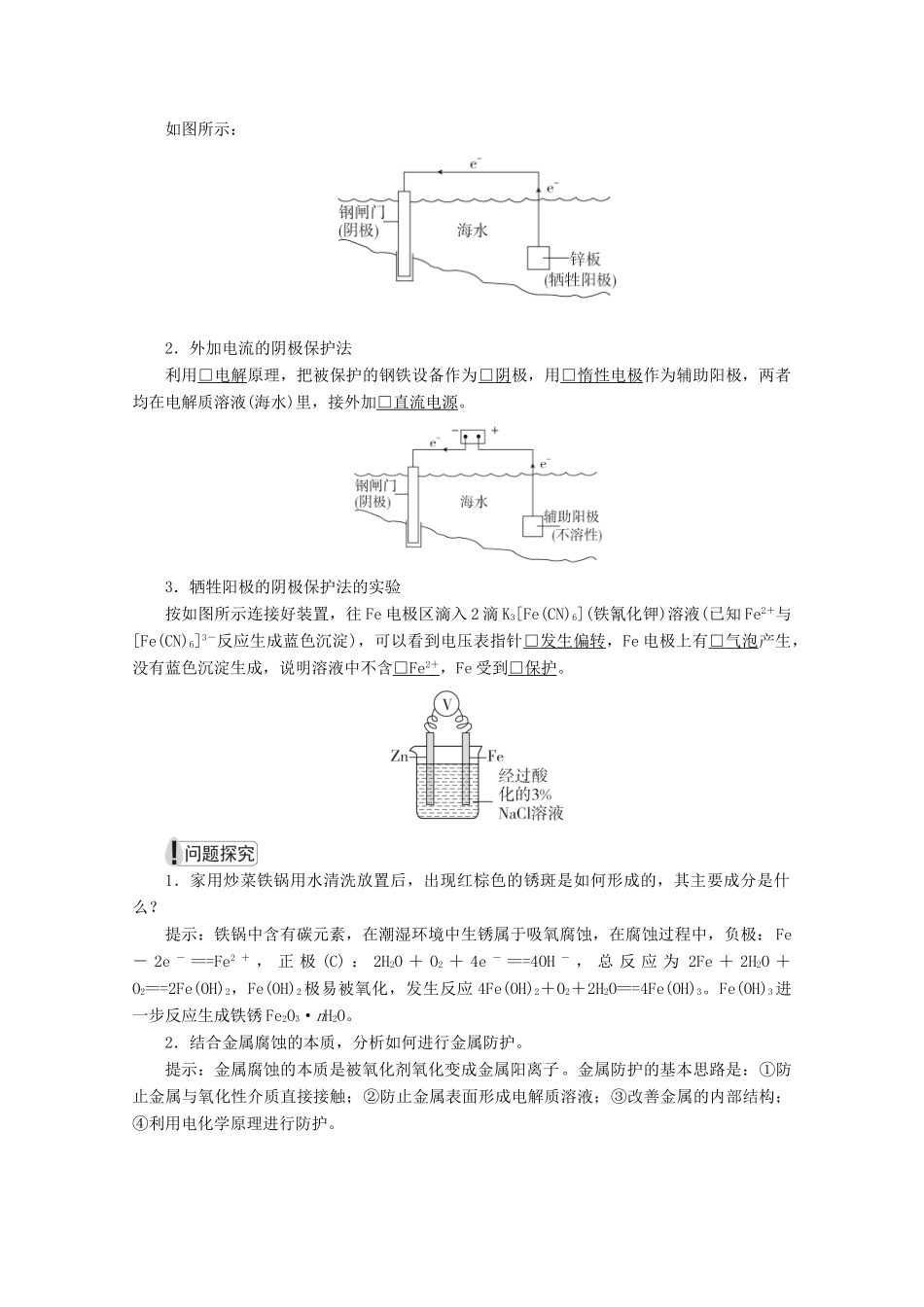
如图所示:2.外加电流的阴极保护法利用□电解原理,把被保护的钢铁设备作为□阴极,用□惰性电极作为辅助阳极,两者均在电解质溶液(海水)里,接外加□直流电源
3.牺牲阳极的阴极保护法的实验按如图所示连接好装置,往Fe电极区滴入2滴K3[Fe(CN)6](铁氰化钾)溶液(已知Fe2+与[Fe(CN)6]3-反应生成蓝色沉淀),可以看到电压表指针□发生偏转,Fe电极上有□气泡产生,没有蓝色沉淀生成,说明溶液中不含□Fe2+,Fe受到□保护
1.家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑是如何形成的,其主要成分是什么
提示:铁锅中含有碳元素,在潮湿环境中生锈属于吸氧腐蚀,在腐蚀过程中,负极:Fe-2e-===Fe2+,正极(C):2H2O+O2+4e-===4OH-,总反应为2Fe+2H2O+O2===2Fe(OH)2,Fe(OH)2极易被氧化,发生反应4Fe(OH)2+O2+2H2O===4Fe(OH)3
Fe(OH)3进一步反应生成铁锈Fe2O3·nH2O
2.结合金属腐蚀的本质,分析如何进行金属防护
提示:金属腐蚀的本质是被氧化剂氧化变成金属阳离子
金属防护的基本思路是:①防止金属与氧化性介质直接接触;②防止金属表面形成电解质溶液;③改善金属的内部结构;④利用电化学原理进行防护
一、金属的化学腐蚀与电化学腐蚀的比较(以铁为例)[即时练]1