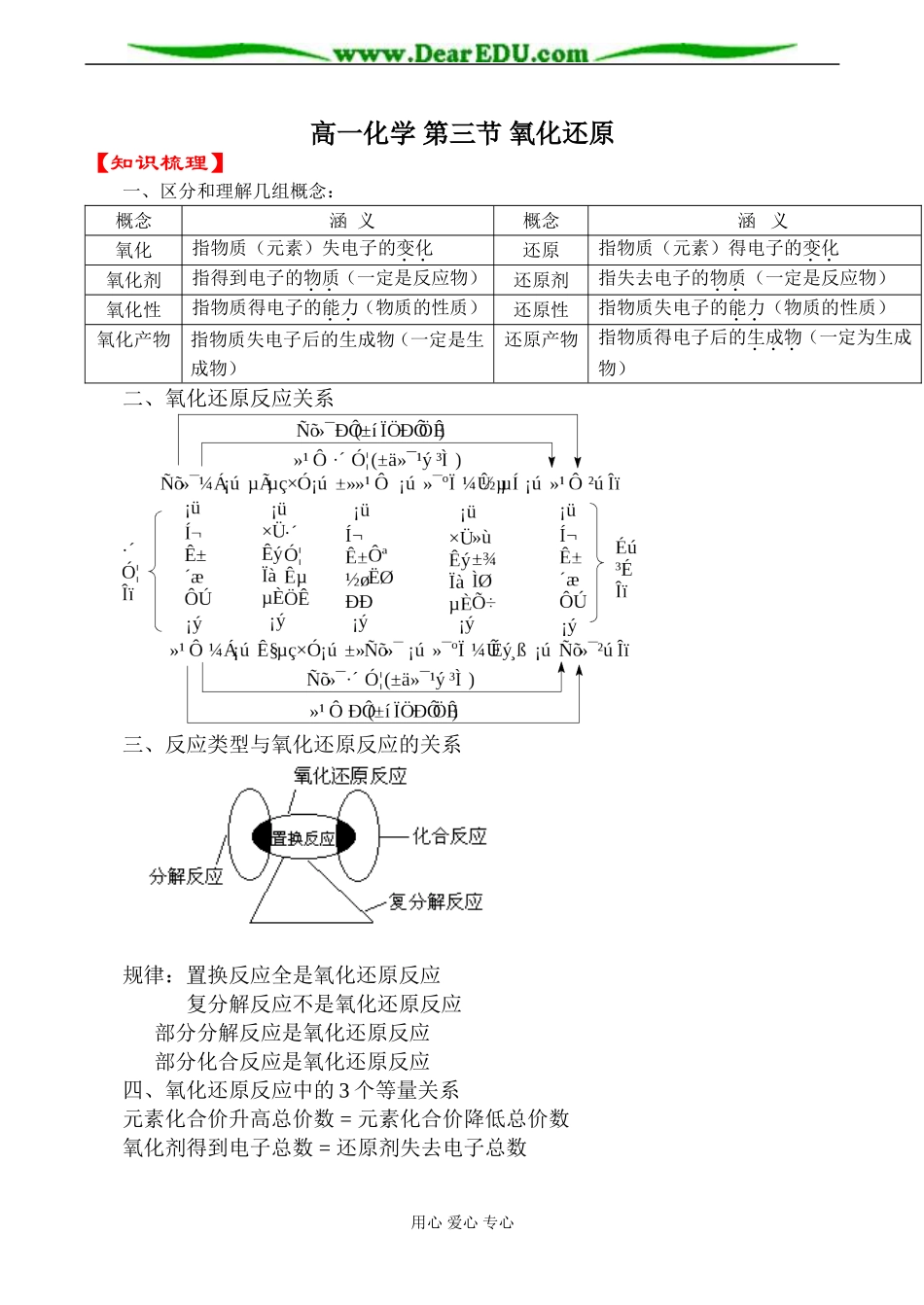
高一化学第三节氧化还原【知识梳理】一、区分和理解几组概念:概念涵义概念涵义氧化指物质(元素)失电子的变化还原指物质(元素)得电子的变化氧化剂指得到电子的物质(一定是反应物)还原剂指失去电子的物质(一定是反应物)氧化性指物质得电子的能力(物质的性质)还原性指物质失电子的能力(物质的性质)氧化产物指物质失电子后的生成物(一定是生成物)还原产物指物质得电子后的生成物(一定为生成物)二、氧化还原反应关系三、反应类型与氧化还原反应的关系规律:置换反应全是氧化还原反应复分解反应不是氧化还原反应部分分解反应是氧化还原反应部分化合反应是氧化还原反应四、氧化还原反应中的3个等量关系元素化合价升高总价数=元素化合价降低总价数氧化剂得到电子总数=还原剂失去电子总数用心爱心专心化合价变化总数=得失电子总数【疑难点悟】(一)氧化还原反应类型1、分子间氧化还原反应:氧化剂与还原剂分别是不同的物质如:SO2+2H2S=3S↓+2H2O2、分子内氧化还原反应:氧化剂与还原剂为同一种反应物,并且被氧化与被还原的元素是该物质中的不同价态的元素
3、歧化反应:不但氧化剂与还原剂是同一种反应物,而且被氧化与被还原的元素还是相同价态的同种元素,这样的氧化还原反应又叫做“自身氧化还原反应”或叫做“歧化反应”
如:Cl2+2NaOH=NaCl+NaClO+H2O4、有的反应既不是氧化剂,又不是还原剂,作“反应介质”
如:Cl2+2NaOH=NaCl+NaCl+H2O中NaOH5、有的反应物参加反应的总量中仅有一部分为氧化剂(或还原剂),另一部分为反应介质
如:Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O中H2SO4一半作为氧化剂,另一半作为酸性介质
(二)氧化性和还原性强弱比较1、根据化学反应判断:在氧化还原反应中氧化剂+还原剂→还原产物+氧化产物
规律是:氧化剂的氧化性>氧化产物的氧化性还原剂的还原性>还原