专题06氧化还原反应一、氧化还原反应基本概念1.概念本质:凡有电子得失或共用电子对偏移的一类反应称氧化还原反应,得失电子数相等
特征:是反应前后有元素化合价发生变化的反应
氧化还原反应电子转移的表示方法①双线桥法:②单线桥法:3
重要的氧化剂和还原剂物质在反应中是作氧化剂还是作还原剂,表观上可通过元素的化合价来判断
一般来说,元素处于最高化合价时,只能作为氧化剂;元素处于最低化合价时,只能作还原剂;元素处于中间化合价时,既可作氧化剂,也可作还原剂
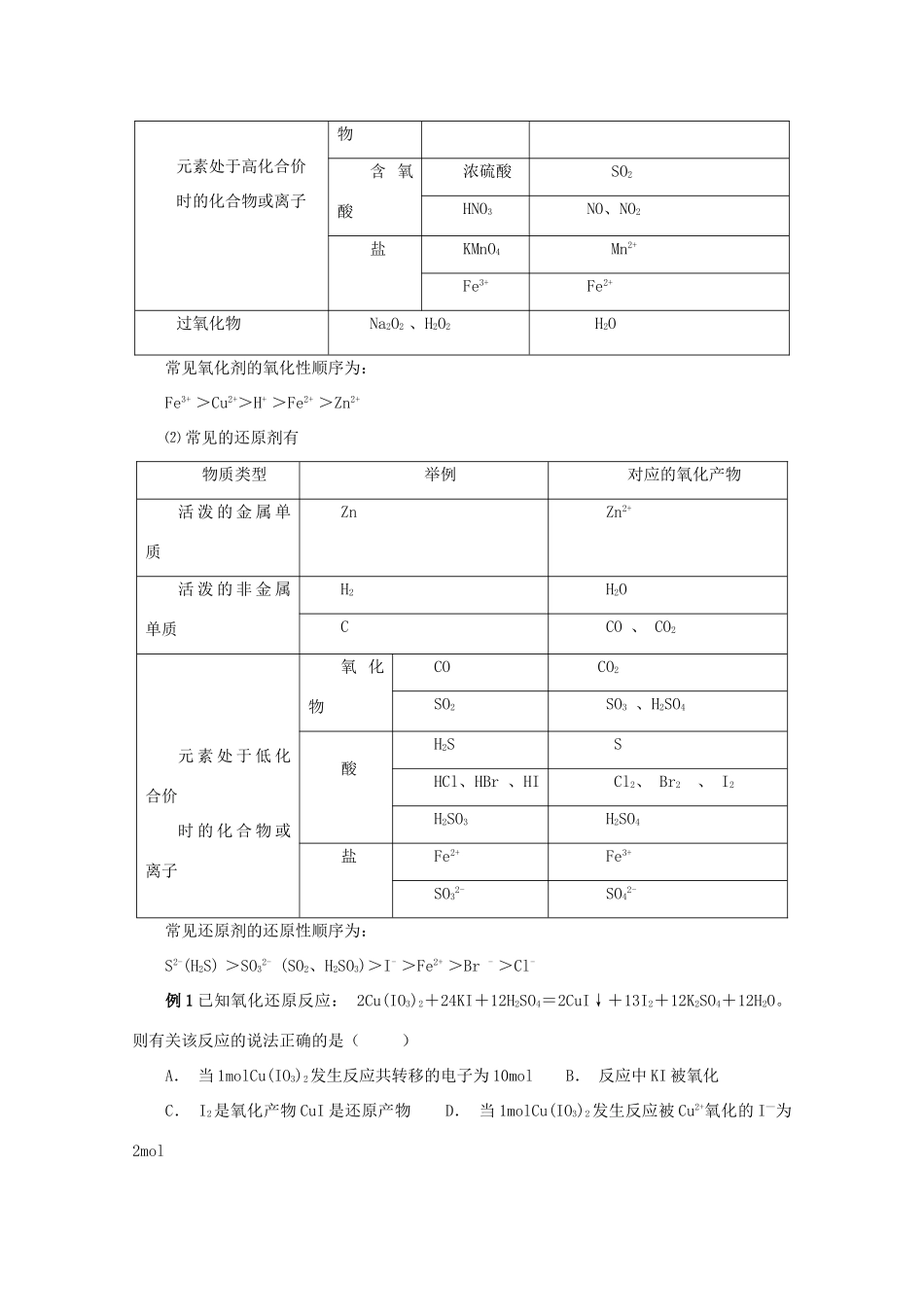
⑴常见的氧化剂物质类型举例对应的还原产物活泼的非金属单质X2(卤素)X-O2O2-、H2O、OH-氧化MnO2Mn2+元素处于高化合价时的化合物或离子物含氧酸浓硫酸SO2HNO3NO、NO2盐KMnO4Mn2+Fe3+Fe2+过氧化物Na2O2、H2O2H2O常见氧化剂的氧化性顺序为:Fe3+>Cu2+>H+>Fe2+>Zn2+⑵常见的还原剂有物质类型举例对应的氧化产物活泼的金属单质ZnZn2+活泼的非金属单质H2H2OCCO、CO2元素处于低化合价时的化合物或离子氧化物COCO2SO2SO3、H2SO4酸H2SSHCl、HBr、HICl2、Br2、I2H2SO3H2SO4盐Fe2+Fe3+SO32-SO42-常见还原剂的还原性顺序为:S2-(H2S)>SO32-(SO2、H2SO3)>I->Fe2+>Br->Cl-例1已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O
则有关该反应的说法正确的是()A.当1molCu(IO3)2发生反应共转移的电子为10molB.反应中KI被氧化C.I2是氧化产物CuI是还原产物D.当1molCu(IO3)2发生反应被Cu2+氧化的I—为2mol例2已知二氯化二硫(S2Cl2)的结构式为Cl—S—S—Cl,它易与水反应2S2Cl2