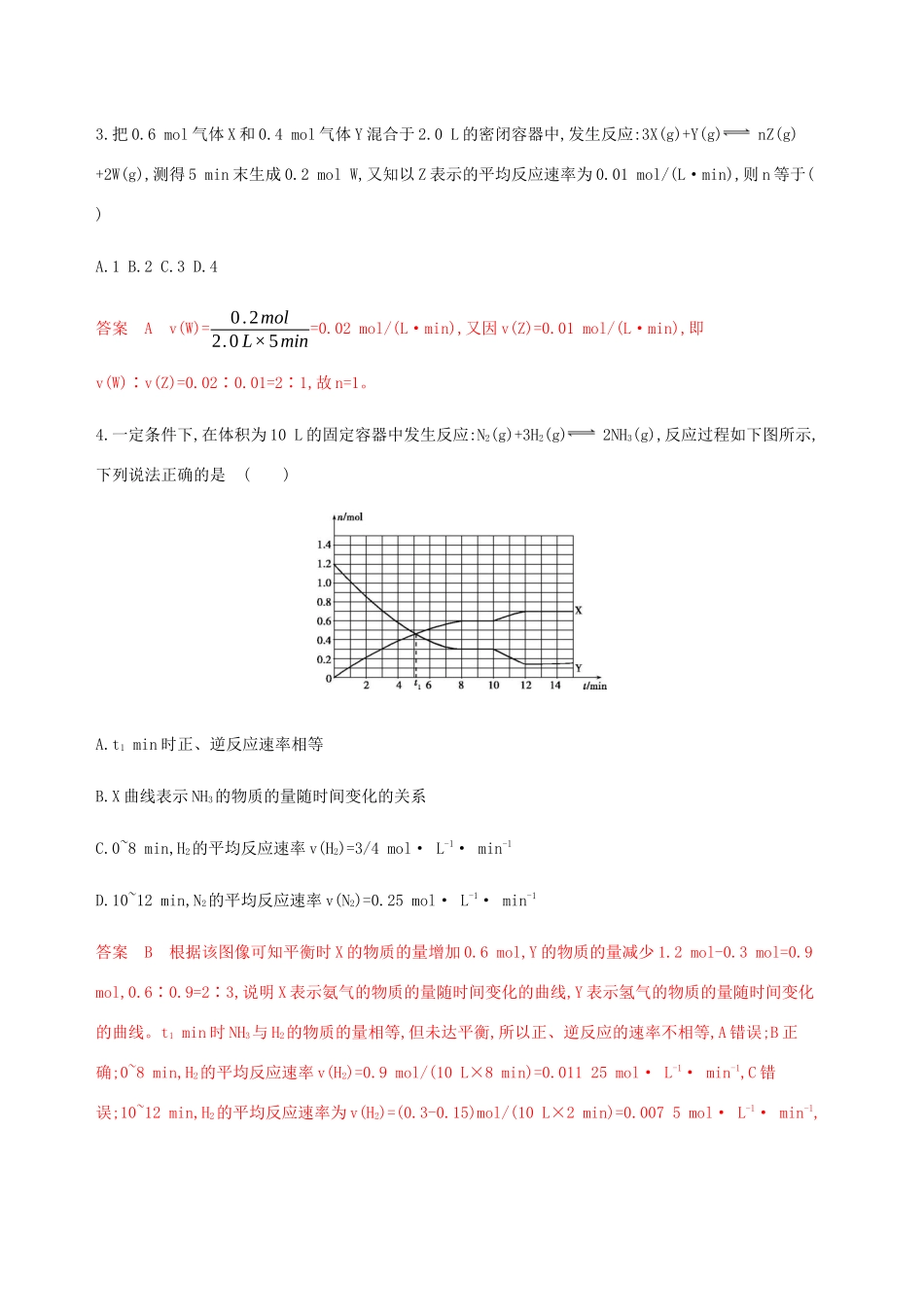
第1讲化学反应速率A组基础题组1.在298K时,实验测得溶液中的反应:H2O2+2HI2H2O+I2,在不同浓度时的化学反应速率见下表,由此可推知当c(HI)=0.500mol·L-1,c(H2O2)=0.400mol·L-1时的反应速率为()实验编号12345c(HI)/mol·L-10.1000.2000.3000.1000.100c(H2O2)/mol·L-10.1000.1000.1000.2000.300v/mol·L-1·s-10.007600.01520.02280.01520.0228A.0.038mol·L-1·s-1B.0.152mol·L-1·s-1C.0.608mol·L-1·s-1D.0.760mol·L-1·s-1答案B由表中数据可知,速率与c(HI)、c(H2O2)成正比。当c(HI)=0.100mol·L-1、c(H2O2)=0.100mol·L-1,v=0.00760mol·L-1·s-1,所以当c(HI)=0.500mol·L-1,c(H2O2)=0.400mol·L-1,v=0.00760mol·L-1·s-1×0.500mol/L0.100mol/L×0.400mol/L0.100mol/L=0.152mol·L-1·s-1。2.可逆反应2A(g)+3B(g)2C(g)+D(g)在四种不同条件下的反应速率分别为①v(A)=0.5mol·L-1·s-1;②v(B)=0.6mol·L-1·s-1;③v(C)=0.35mol·L-1·s-1;④v(D)=0.3mol·L-1·min-1,则该反应在不同条件下反应速率最快的是()A.①B.②C.③D.④答案A转化为用D表示的反应速率分别为:①v(D)=0.25mol·L-1·s-1=15mol·L-1·min-1;②v(D)=0.2mol·L-1·s-1=12mol·L-1·min-1;③v(D)=0.175mol·L-1·s-1=10.5mol·L-1·min-1;④v(D)=0.3mol·L-1·min-1,所以反应速率最快的是①。3.把0.6mol气体X和0.4mol气体Y混合于2.0L的密闭容器中,发生反应:3X(g)+Y(g)nZ(g)+2W(g),测得5min末生成0.2molW,又知以Z表示的平均反应速率为0.01mol/(L·min),则n等于()A.1B.2C.3D.4答案Av(W)=0.2mol2.0L×5min=0.02mol/(L·min),又因v(Z)=0.01mol/(L·min),即v(W)∶v(Z)=0.02∶0.01=2∶1,故n=1。4.一定条件下,在体积为10L的固定容器中发生反应:N2(g)+3H2(g)2NH3(g),反应过程如下图所示,下列说法正确的是()A.t1min时正、逆反应速率相等B.X曲线表示NH3的物质的量随时间变化的关系C.0~8min,H2的平均反应速率v(H2)=3/4mol·L-1·min-1D.10~12min,N2的平均反应速率v(N2)=0.25mol·L-1·min-1答案B根据该图像可知平衡时X的物质的量增加0.6mol,Y的物质的量减少1.2mol-0.3mol=0.9mol,0.6∶0.9=2∶3,说明X表示氨气的物质的量随时间变化的曲线,Y表示氢气的物质的量随时间变化的曲线。t1min时NH3与H2的物质的量相等,但未达平衡,所以正、逆反应的速率不相等,A错误;B正确;0~8min,H2的平均反应速率v(H2)=0.9mol/(10L×8min)=0.01125mol·L-1·min-1,C错误;10~12min,H2的平均反应速率为v(H2)=(0.3-0.15)mol/(10L×2min)=0.0075mol·L-1·min-1,氮气的反应速率是氢气反应速率的1/3,则N2的平均反应速率为v(N2)=0.0075mol·L-1·min-1×13=0.0025mol·L-1·min-1,D错误。5.下列说法正确的是()A.对于反应A(s)+B(g)C(g)+D(g),加入A,反应速率加快B.2NO2N2O4(正反应放热),升高温度,v(正)增大,v(逆)减小C.一定温度下,反应N2(g)+3H2(g)2NH3(g)在密闭容器中进行,恒压,充入He不改变化学反应速率D.100mL2mol·L-1稀盐酸与锌反应时,加入少量硫酸铜固体,生成氢气的速率加快答案D对于反应A(s)+B(g)C(g)+D(g),A为固体,加入A,A的浓度不变,反应速率不变,故A错误;2NO2N2O4(正反应放热),升高温度,v(正)、v(逆)均增大,故B错误;一定温度下,反应N2(g)+3H2(g)2NH3(g)在密闭容器中进行,恒压,充入He,容器的体积增大,浓度减小,化学反应速率减慢,故C错误;100mL2mol·L-1稀盐酸与锌反应时,加入少量硫酸铜固体,锌与硫酸铜发生置换反应析出铜,形成原电池,生成氢气的速率加快,故D正确。6.如图为某化学反应的反应速率与时间的关系示意图。在t1时刻升高温度或增大压强,反应速率的变化都符合示意图中表示的反应是()A.2SO2(g)+O2(g)2SO3(g)ΔH<0B.4NH3(g)+5O2(g)4NO(g)+6H2O(g)ΔH<0C.H2(g)+I2(g)2HI(g)ΔH>0D.2A(g)+B(g)2C(g)ΔH>0答案B在t1时刻升高温度或增大压强,正、逆反应速率都增大,且逆反应速率大于正反应速率,说明平衡向逆反应方向移动,若是升高温度,正反应应为放热反应,若是增大压强,则反应物气体的化学计量数之和小于生成物气体的化学计量数之和,只有B符合。7.(2018河南开封模拟)外界其他条件相同,不同pH条件下,用浓度传感器测得反应2A+B3D中产物D的浓度随时间变...