化学反应原理综合一、非选择题(原理综合题):(本题共15小题)1.Cl2、SO2、CO、NO等不能直接排放到大气中,需经过处理进行回收利用,从而达到减排的目的
回答下列问题:(1)已知S(s)和CO(g)的燃烧热分别是296
0kJ/mol、283
0kJ/mol,则反应2COgSO2g=2CO2gSs的ΔH=___________
(2)一定条件下,Cl2与NO可化合生成重要的化工原料氯化亚硝酰(NOCl),写出该反应的化学方程式:___________;已知NOCl中各原子均满足8电子稳定结构,其电子式为___________
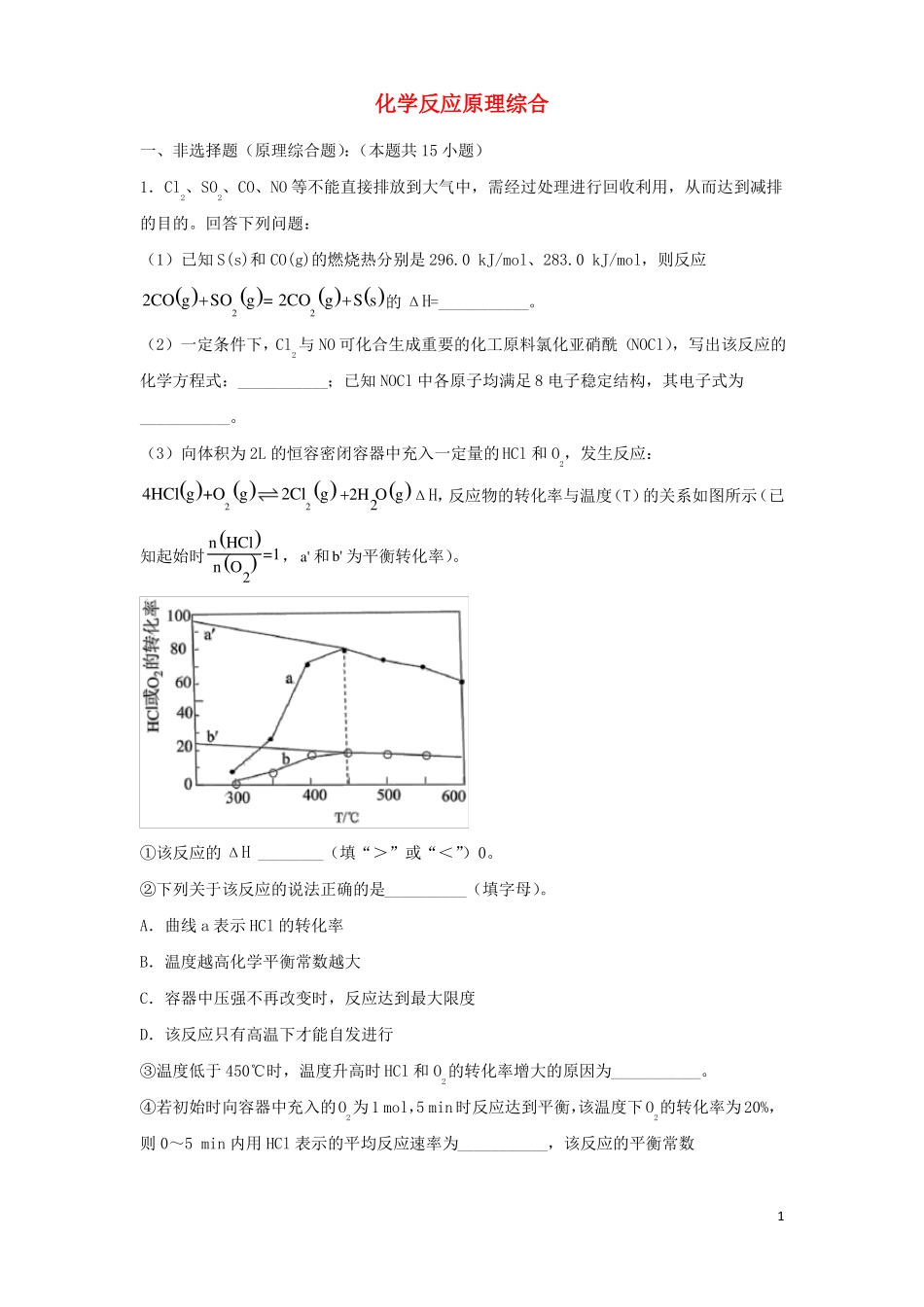
(3)向体积为2L的恒容密闭容器中充入一定量的HCl和O2,发生反应:4HClg+O2g2Cl2g2H2OgΔH,反应物的转化率与温度(T)的关系如图所示(已nHCl=1,a'和b'为平衡转化率)知起始时
nO2①该反应的ΔH________(填“>”或“<”)0
②下列关于该反应的说法正确的是__________(填字母)
A.曲线a表示HCl的转化率B.温度越高化学平衡常数越大C.容器中压强不再改变时,反应达到最大限度D.该反应只有高温下才能自发进行③温度低于450℃时,温度升高时HCl和O2的转化率增大的原因为___________
④若初始时向容器中充入的O2为1mol,5min时反应达到平衡,该温度下O2的转化率为20%,则0~5min内用HCl表示的平均反应速率为___________,该反应的平衡常数1Kp=___________(已知:气体分压(p分)=气体总压(p总)×体积分数,Kp为以分压表示的平衡常数;平衡时容器内的总压为P0)
【答案】(1)-270
0kJ/mol(2)Cl2+2NO一定条件2NOCl(3)<AC平衡前,升温,速率增大,单位时间内反应物的转