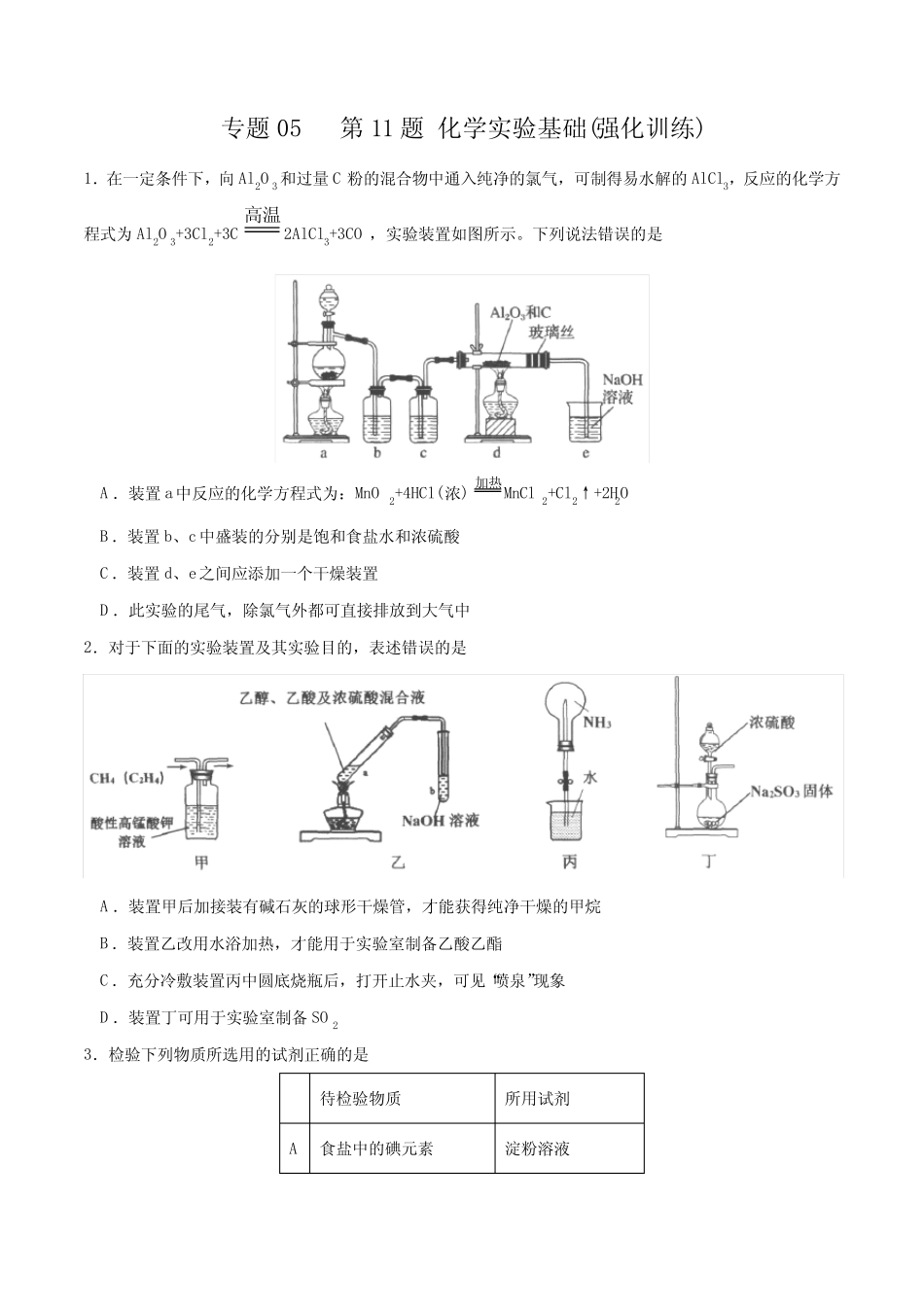
专题05第11题化学实验基础(强化训练)1.在一定条件下,向Al2O3和过量C粉的混合物中通入纯净的氯气,可制得易水解的AlCl3,反应的化学方程式为Al2O3+3Cl2+3C高温2AlCl3+3CO,实验装置如图所示
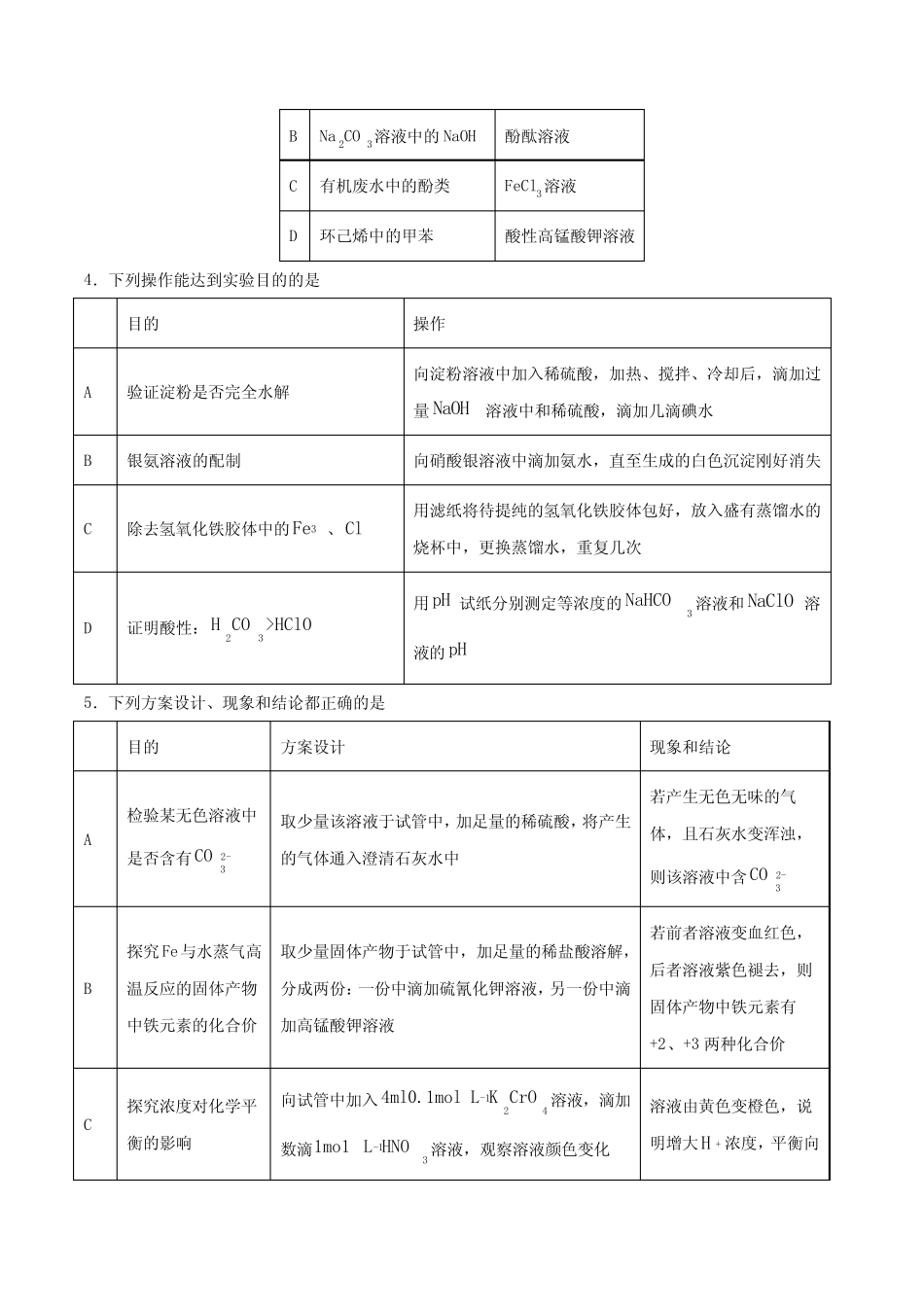
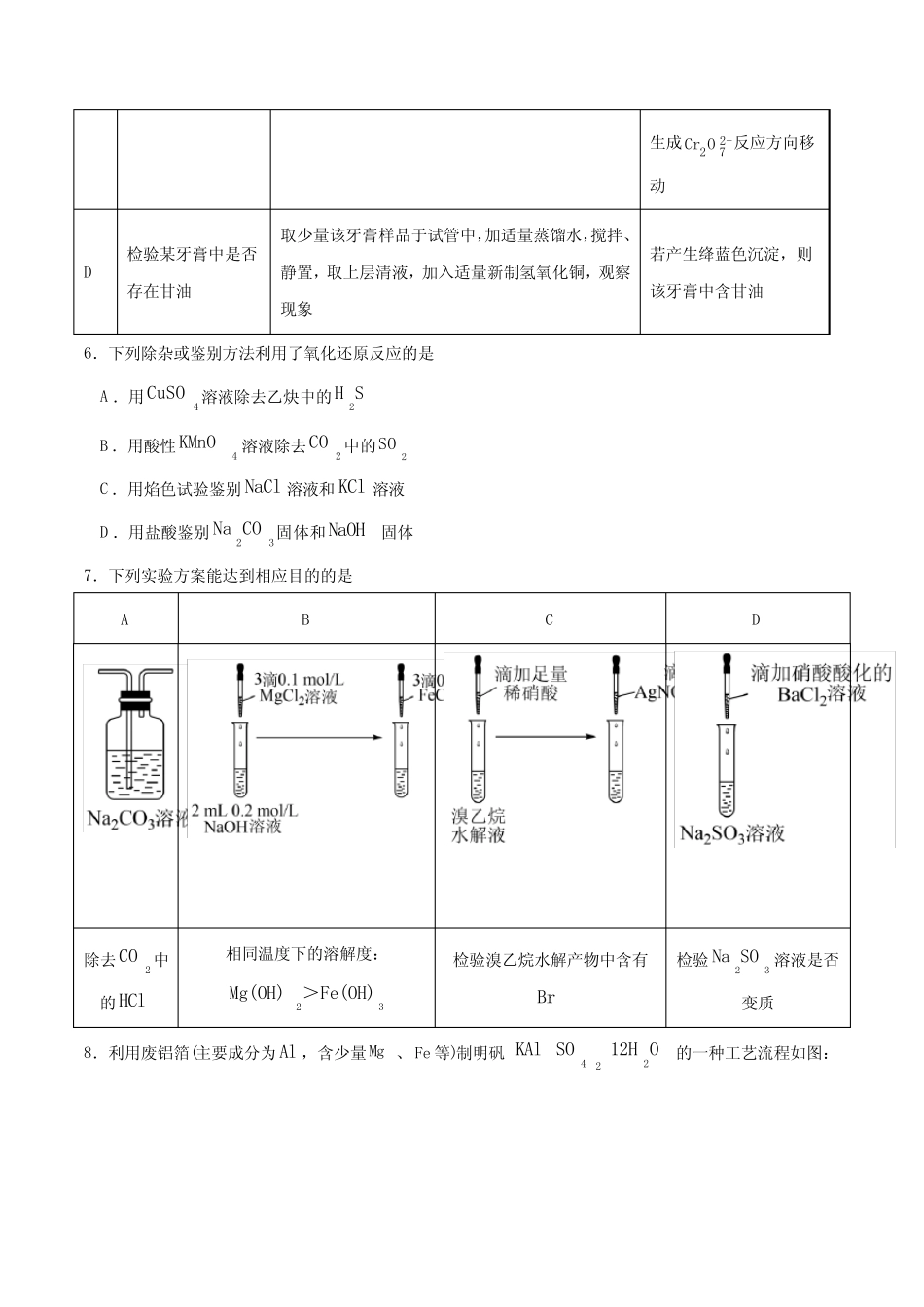
下列说法错误的是A.装置a中反应的化学方程式为:MnO2+4HCl(浓)加热MnCl2+Cl2↑+2H2OB.装置b、c中盛装的分别是饱和食盐水和浓硫酸C.装置d、e之间应添加一个干燥装置D.此实验的尾气,除氯气外都可直接排放到大气中2.对于下面的实验装置及其实验目的,表述错误的是A.装置甲后加接装有碱石灰的球形干燥管,才能获得纯净干燥的甲烷B.装置乙改用水浴加热,才能用于实验室制备乙酸乙酯C.充分冷敷装置丙中圆底烧瓶后,打开止水夹,可见“喷泉”现象D.装置丁可用于实验室制备SO23.检验下列物质所选用的试剂正确的是待检验物质所用试剂A食盐中的碘元素淀粉溶液BNa2CO3溶液中的NaOH酚酞溶液C有机废水中的酚类FeCl3溶液D环己烯中的甲苯酸性高锰酸钾溶液4.下列操作能达到实验目的的是目的操作A验证淀粉是否完全水解向淀粉溶液中加入稀硫酸,加热、搅拌、冷却后,滴加过量NaOH溶液中和稀硫酸,滴加几滴碘水B银氨溶液的配制向硝酸银溶液中滴加氨水,直至生成的白色沉淀刚好消失C除去氢氧化铁胶体中的3Fe、Cl用滤纸将待提纯的氢氧化铁胶体包好,放入盛有蒸馏水的烧杯中,更换蒸馏水,重复几次D证明酸性:23HCO>HClO用pH试纸分别测定等浓度的3NaHCO溶液和NaClO溶液的pH5.下列方案设计、现象和结论都正确的是目的方案设计现象和结论A检验某无色溶液中是否含有2-3CO取少量该溶液于试管中,加足量的稀硫酸,将产生的气体通入澄清石灰水中若产生无色无味的气体,且石灰水变浑浊,则该溶液中含2-3COB探究Fe与水蒸气高温反应的固体产物中铁元素的化合价取少量固体产物