1工业流程题,实验题(铬专题)1某铬贫矿主要成分为Fe(CrO2)2,还含有Fe2O3、MgO、Al2O3,采用次氯酸钠法处理矿石并制备CrO3的工艺流程如图,已知“氧化浸出”时铁以最高价氧化物存在
下列说法错误的是A
“氧化浸出”时煮沸的目的是加快氧化浸出速率B
滤渣的主要成分是MgO、Fe2O3C
化合物I为NaOH,化合物II为NaHCO3D
实验室进行“混合”时,将Na2Cr2O7溶液缓慢倒入浓硫酸中,边倒边搅拌2某铬贫矿主要成分为FeCrO22,还含有Fe2O3、MgO、Al2O3,采用次氯酸钠法处理矿石并制备CrO3的工艺流程如图,已知“氧化浸出”时铁以最高价氧化物存在
下列说法错误的是A
“氧化浸出”时发生的主要反应为:2FeCrO22+7ClO-+2OH-=4CrO2-4+2Fe3++7Cl-+H2OB
滤渣的主要成分是MgO、Fe2O3C
化合物Ⅰ为NaHCO3D
实验室进行“混合”时,将浓硫酸缓慢倒入Na2Cr2O7溶液中,边倒边搅拌3室温时,实验室以含铬废液(主要离子含K+、Fe3+、Cr3+、SO2-4)制取含K2Cr2O7溶液的流程如下:已知:①室温时,KspCrOH3=6×10-31,KspFeOH3=4×10-38②“氧化”时CrOH3转化为CrO2-4下列说法正确的是A
“过滤Ⅰ”所得滤液中cCr3+=6×10-7mol⋅L-1B
“氧化”时的离子方程式为:4OH-+2CrOH3+3H2O2=2CrO2-4+8H2OC
“酸化”时溶液pH越低,CrO2-4转化为Cr2O2-7的比例越低D
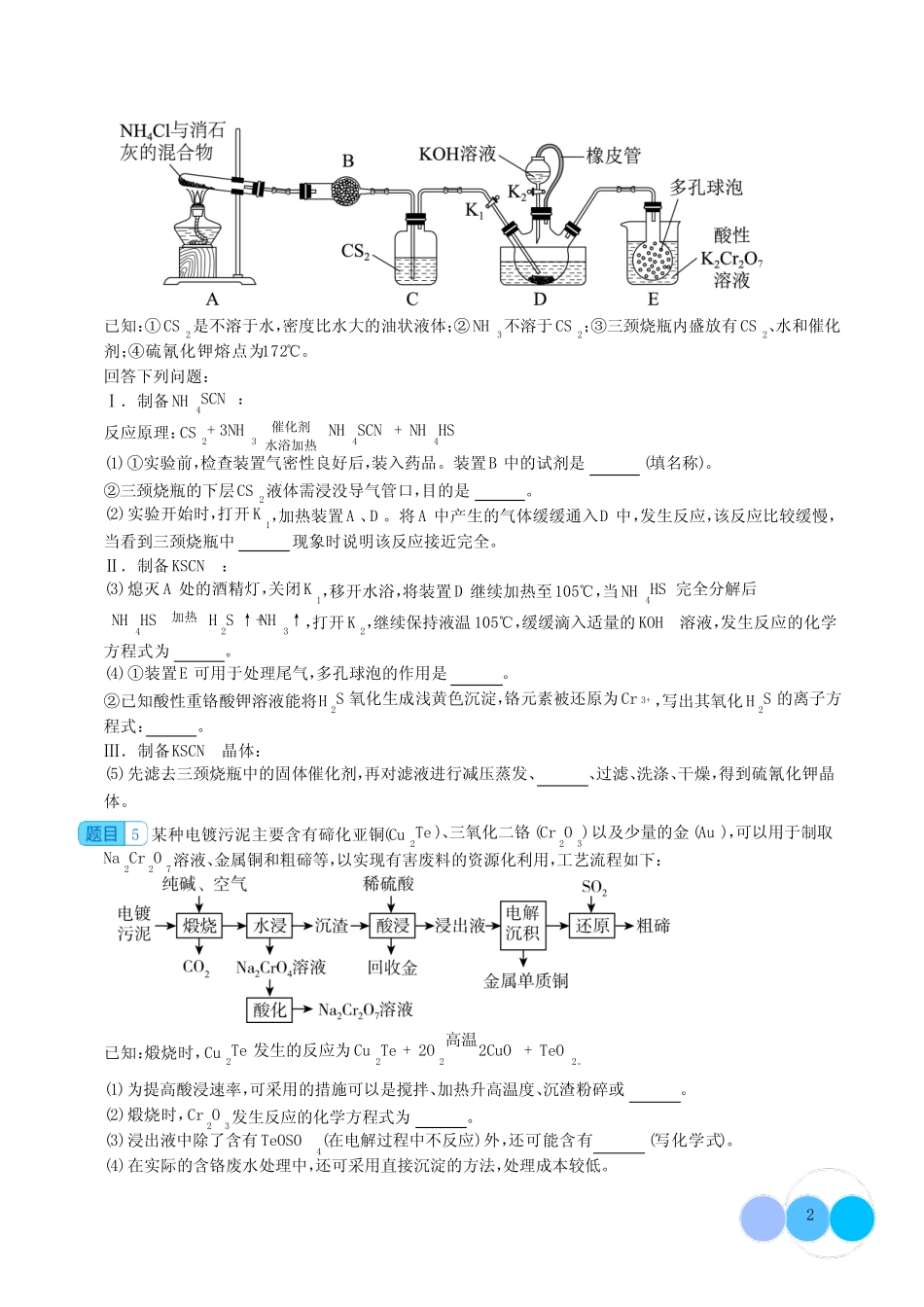
将“含K2Cr2O7溶液”蒸干可得纯净的K2Cr2O7固体4硫氰化钾(KSCN)俗称玫瑰红酸钾,是一种用途广泛的化学药品
实验室模拟工业上的硫氰化铵转化法制备硫氰化钾的实验装置如图所示:2024届高三化学一轮复习--工业流