选修三第二章第三节《分子的性质》的学案设计(第一课时:键的极性和分子的极性)【目标导示】:1
了解极性共价键和非极性共价键;2
结合常见物质分子立体结构,能够辨认常见的极性分子和非极性分子;3
了解化学键的极性与分子极性的关系
【学习重点】:多原子分子中,极性分子和非极性分子的判断
【内容导航】:1
键的极性从共用电子对是否有偏移可把共价键分为极性键和非极性键,键的极性是指_____________________
(1)极性键:由________的原子形成的共价键
成键电子对在两原子间____________
(2)非极性键:由________的原子形成的共价键
成键电子对在两原子间____________
请判断:在O2、HCl、CH4、PCl3、H2O、CO2、H2O2、CH3CH2OH、P4中,只含非极性键的分子是__________________________,只含极性键的分子是___________________________,既含极性键又含非极性键的分子有______________________________________
【点拔】:①键的“极性”其含义是指:共用电子对的偏移
不同种原子形成的共价键可能有极性,也可能无极性
②键的极性大小(强弱)是指共用电子对偏移程度,共用电子对偏移程度越大,键的极性越大(越强)
③形成共价键的两种元素的原子的电负性相差越大,键的极性越大
分子的极性(1)极性分子:正电中心和负电中心_____,使分子的某一部分呈正电性,另一部分呈负电性的分子
(2)非极性分子:正电中心和负电中心______的分子
键的极性和分子极性的关系(1)只含非极性键的分子一定是非极性分子
(2)含有极性键的分子有没有极性,必须依据分子中极性键的极性的向量和是否等于零而定,等于零时是非极性分子,否则是极性分子
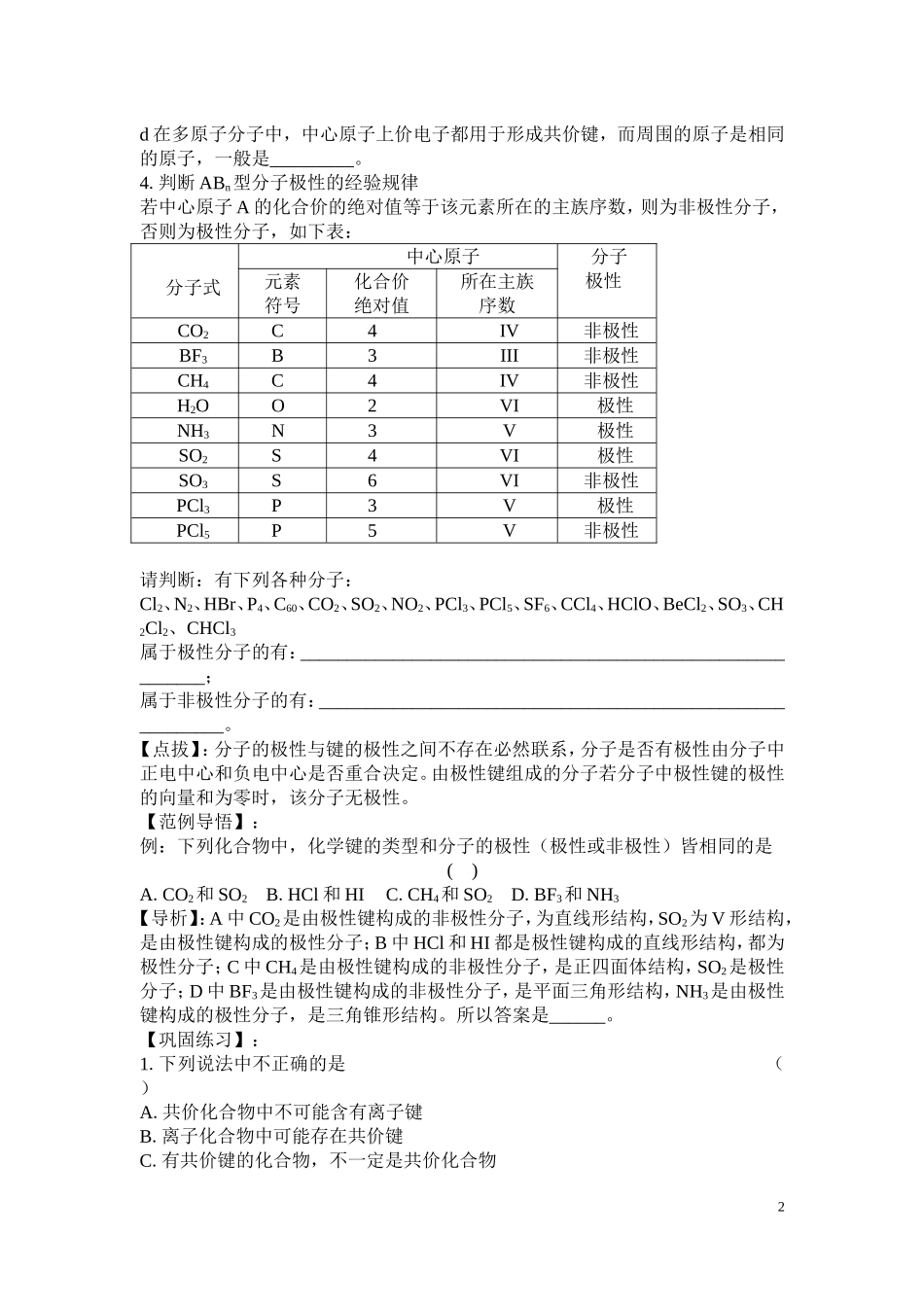
(3)共价键的极性与