水乃生命之源,我们对水又了解多少呢
第二节水的电离和溶液的酸碱性第1课时水的电离溶液的酸碱性与pH如图,是一个电解水的装置
在做这个实验时往往在水中加入几滴稀硫酸,以增强水的导电性
难道纯水真的不导电吗
精确的实验证明:精确的实验证明:水是一种极弱的电解质,它能在水中微弱的电离,生成H3O+(水合氢离子)和OH-
请同学们写出水的电离方程式请同学们写出水的电离方程式研究电解质溶液时往往涉及到溶液的酸碱性
电解质溶液的酸碱性跟水的电离有密切的关系
为了从本质上认识溶液的酸碱性,就要了解水的电离情况
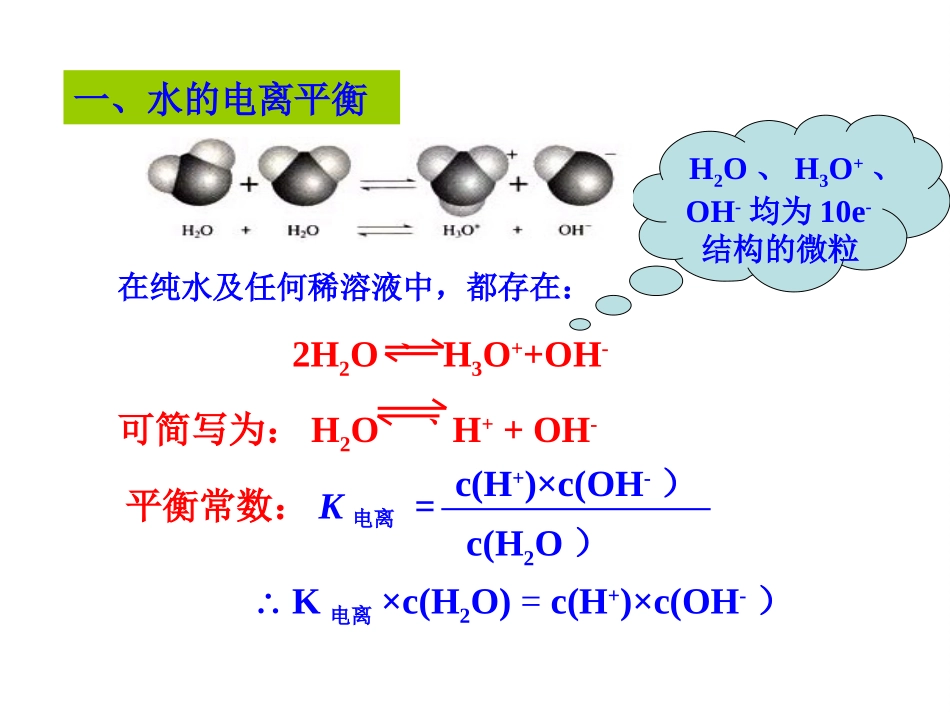
在纯水及任何稀溶液中,都存在:2H2OH3O++OH-可简写为:H2OH++OH-平衡常数:K电离=c(H+)×c(OH-)c(H2O)H2O、H3O+、OH-均为10e-结构的微粒一、水的电离平衡∴K电离×c(H2O)=c(H+)×c(OH-)水的电离极其微弱,25℃时1升纯水为55
6mol,发生电离的水只有1×10-7mol,电离前后水的物质的量几乎不变,c(H2O)可以视为常数
常数乘以常数为一个新的常数,用Kw表示,称为水的离子积常数,简称水的离子积
水的离子积:KW=c(H+)×c(OH-)∴K电离×c(H2O)=c(H+)×c(OH-)升高温度,水的电离平衡向右移动,电离程度增大,Kw越大
水的电离是吸热过程
升高温度,促进水的电离,Kw增大
Kw只与温度有关,与浓度无关
Kw=Kw=2525℃℃::C(HC(H++)=C(OH)=C(OH--)=1×10)=1×10-7-7mol/Lmol/L1×101×10-14-1410010000CC::C(HC(H++)=C(OH)=C(OH--)=)=7
4×10--77mol/Lmol/LKw=Kw=5
5×10-13-13注意哪
水的电离是吸热过程,温度越高,平衡右移,电离程度越大