第三节化学平衡第二章化学反应速率与化学平衡第二章化学反应速率与化学平衡第二课影响化学平衡移动的因第二课影响化学平衡移动的因素素化学平衡状态的特征(3)动:反应未终止,是动态平衡(v(正)=v(逆)≠0)(1)逆:化学平衡的研究对象是可逆反应(4)定:反应混合物中各组分的浓度保持一定,各组分的含量保持不变
(5)(5)变:改变影响平衡的外界条件,旧平变:改变影响平衡的外界条件,旧平衡会发生改变,从而建立新的化学平衡
衡会发生改变,从而建立新的化学平衡
(2)等:v(正)=v(逆)(以同一物质为标准)定义:可逆反应中,旧化学平衡被破坏,新化学平衡建立过程,叫做化学平衡的移动
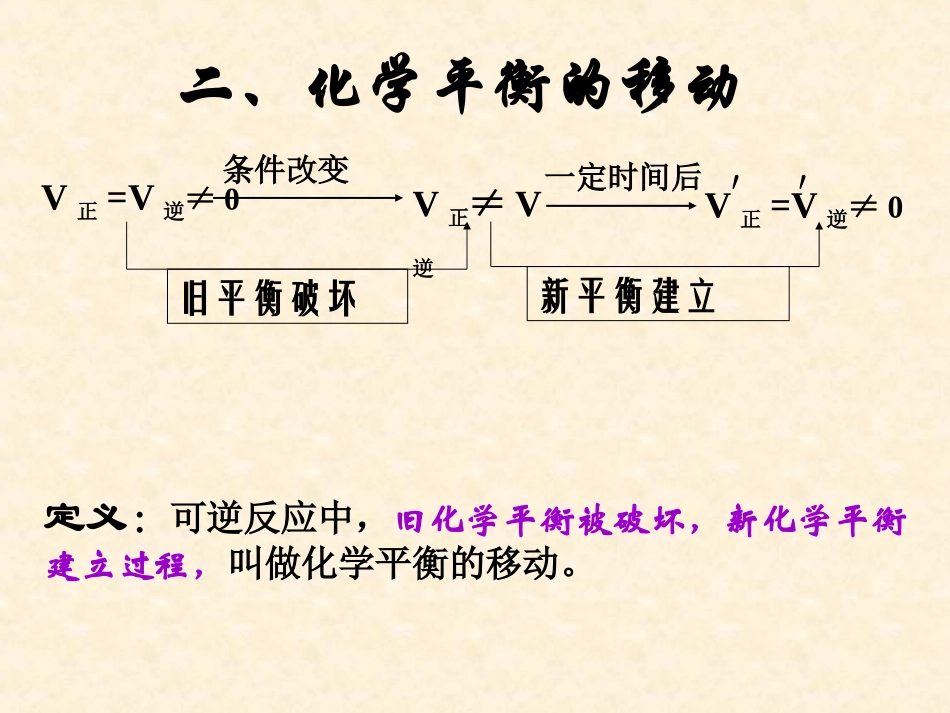
V正=V逆≠0V正≠V逆条件改变新平衡建立旧平衡破坏V正=V逆≠0′′一定时间后二、化学平衡的移动平衡向正反应方向移动
平衡向逆反应方向移动
正逆反应速率与平衡移动的方向:①若V正>V逆,③若V正=V逆,②若V正<V逆,【思考与交流】有哪些条件能改变化学平衡呢
一、浓度对化学平衡的影响(P26)溶液橙色加深溶液黄色加深•实验探究(P27实验2-6)Fe3++3SCN-Fe(SCN)3现象:溶液变成红色(血红色)(无色)(黄色)A
加少量饱和FeCl3溶液:B
加少量浓KSCN溶液:C
在上述两支试管中加少量NaOH溶液:有红褐色沉淀生成,溶液红色变浅红色加深;红色加深;实验结论:实验结论:在其他条件不变时,增大反应物或减小生成物的浓度化学平衡向正反应方向移动减小反应物或增大生成物的浓度化学平衡向逆反应方向移动浓度对化学平衡移动的几个注意点①平衡体系中的固体和纯液体,其浓度可看作一个常数,他们的改变,不会影响化学平衡的移动
②只要是增大浓度(反应物还是生成物),新平衡状态下的反应速率一定大于原平衡状态;减小浓度,新平衡状态下的速率一定小于原平衡状态
③反应物有两种或两种以上,增加一种物质的浓度,