化学键1、定义:相邻原子间强烈的相互作用2、用化学键的观点来分析化学反应的本质一个化学反应的的过程,本质上就是旧化学键断裂和新化学键形成的过程
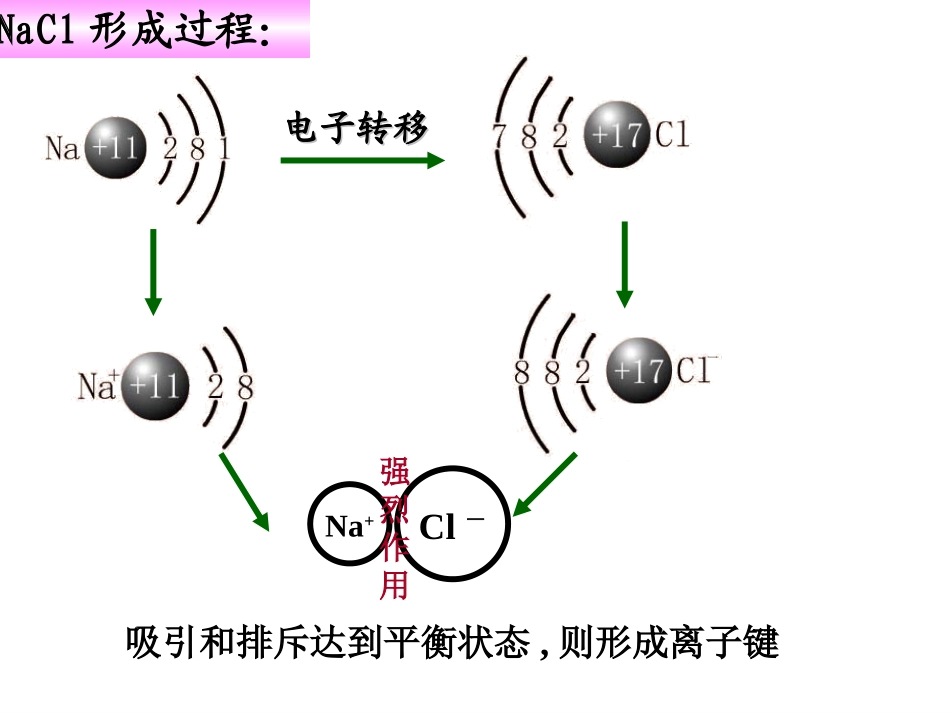
化学键离子键共价键金属键3、化学键的分类Na+Cl-电子转移电子转移NaCl形成过程:吸引和排斥达到平衡状态,则形成离子键强烈作用11、离子键的定义、离子键的定义:使带相反电荷的阴、阳离子阴、阳离子结合的相互(静电)作用
相互作用静电作用静电吸引静电斥力异性电荷之间静电引力原子核间、电子间静电斥力处于平衡状态)形成离子键一、离子键的形成P38静电引力和静电斥力22、离子键的形成过程:、离子键的形成过程:一、离子键33、离子键的成键元素:、离子键的成键元素:{形成化合物的元素的电负性的差>1
7}{形成化合物的元素的电负性的差>1
7}活泼金属元素(IA,IIA)与活泼非金属元素(VIA,VIIA)(包括铵盐)44、离子键的成键特点:、离子键的成键特点:55、离子化合物、离子化合物定义:定义:包括:包括:(1)活泼金属元素活泼金属元素与活泼非金属元素形成的化合物
(2)活泼金属元素和酸根离子(或OH-)形成的盐(或碱)(3)铵根和酸根离子(或活泼非金属元素离子)形成的盐
含有离子键的化合物都是离子化合物(P39)无方向性、无饱和性①MgOAl②2O3MgCl③2④AlCl3NaClNaOH⑤⑥⑦KOHBaSO⑧4除④外除④外练习1
下列化合物中含有离子键()⑴、原子的电子式:ClMgNa①阴离子的电子式简单的阴离子:复杂的阴离子:OH-⑵、离子的电子式:O2-S2-Mg2Na②阳离子的电子式简单的阳离子:复杂的阳离子:即离子符号如NH4+:NH+HHH.要注明最外层电子数及电荷数⑶、离子化合物的电子式:1
电子式:二、用电子式表示离子的形成过程过氧根离子(3)离子化合物的电子式NaClMgCl2Na2SS[]2Na+Na+Cl[]-N