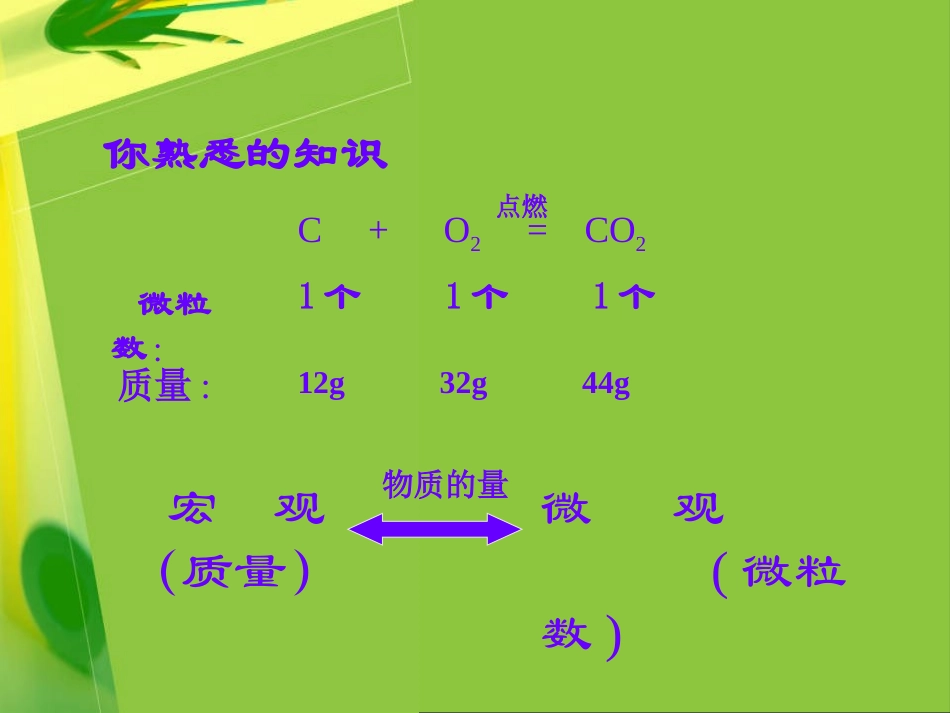
第一节物质的量及其单位取一些大米称其质量,并数出大米粒数,再计算每一粒大米的质量。想想看:你如何用托盘天平称出一粒米的质量(假设每粒大米的质量一样大)你熟悉的知识C+O2=CO2点燃质量:微粒数:12g32g44g1个1个1个宏观(质量)微观(微粒数)物质的量物质的量的引入数量少的东西可以一个个数,可以十个十个的数,但是分子的个数是非常巨大的,你无法一个个数,无法十个十个甚至无法万个万个的数;为了方便,采用1mol、1mol的数,mol读作摩尔,是物质的量的单位,正如千克是重量的单位一样;一、物质的量及其单位(一)物质的量:表示构成物质微观粒子数目的物理量;符号:n,如nB或n(B);“物质的量”是一个整体,是专用名词,不能分开!氢原子的物质的量表示为:nH或n(H)氢分子的物质的量表示为:nH2或n(H2)(二)物质的量的单位——摩尔符号:mol书写:物质的量-摩尔-物质名称或化学式如:0.5mol水等0.5molH2O水分子的物质的量为0.5moln(H2O)=0.5mol原子核内有6个质子和6个中子1mol的标准是什么?(既1mol物质含有多少个微粒呢?)用0.012kg12C所含的碳原子数作为1mol的标准。0.012kg12C[思考]已知:一个碳原子的质量为1.993×10-26kg求:0.012kgC-12中所含的碳原子数?解:碳原子数=0.012kg1.993×10-26kg≈6.02×1023个12C原子(1)1mol粒子的数目是0.012kg12C所含的碳原子数,约为6.02×1023个(2)1mol任何粒子的粒子数叫阿伏加德罗常数(意大利科学家阿伏伽德罗测得并提出的)。见P41。例如:1molC含6.02×1023个C1molNa+含6.02×1023个Na+问题1:阿伏加德罗常数约为6.02×1023,这到底有多大?非常庞大,如果6.02×1023粒稻谷,平均分给全球60亿人,每人每天吃一斤,则需要吃14万年。问题3:能否说1mol小麦约含有6.02×1023个麦粒?为什么?不能,因为物质的量及其单位的使用对象只能是微观粒子,不能用来描述宏观物质。问题2:6.02×1023等于阿伏加德罗常数吗?不等[思考]1mol任何粒子的粒子数=0.012kg12C所含的碳原子数=阿伏加德罗常数6.02ㄨ1023约为归纳:[巩固练习]判断下列说法是否正确(1)1mol氧(2)0.5molH2O(3)3mol大米(4)0.5摩尔CO2正确错误,摩尔不能用来描述宏观物质正确错误,必须指明微粒的种类,是氧原子、氧分子还是氧离子,可改为1molO或1molO2问题探究(1)1molO2中约含有多少个氧气分子?(2)2molO2中约含有多少个氧气分子?(3)nmolO2中约含有多少个氧气分子?(已知阿伏加德罗常数为NA)6.02×10232×6.02×1023n×6.02×1023(n×NA)阿伏加德罗常数微粒个数物质的量NNAnB×=宏观(质量)微观(微粒数)物质的量阿伏加德罗常数物质的量相等的任何物质,所含的粒子数一定相同,反之亦然。在化学反应方程式中,分子式前面的系数之比,就等于物质的量之比。1mol=1000mmol1mmol=1000µmol单位换算二、摩尔质量(一)摩尔质量的定义质量除以物质的量,也就是1mol物质所含的质量(g)。符号:M,要在其右下角或用括号写明物质的化学式。如:MH2OMCO2MH单位:g/mol微观1个C原子1个O原子1个Fe原子↓扩大6.02×10231molC原子1molO原子1molFe↓↓↓相对原子质量1216560.012kg=12g16g56g(二)摩尔质量数值的确定推导:1mol其他原子、分子或者离子的质量各是多少呢?1mol任何原子的质量,以克为单位,在数值上等于该原子的相对原子质量。1mol任何分子的质量在数值上就等于该分子的相对分子质量。对于离子来讲,由于电子的质量很小,可以忽略不计,所以1mol离子的质量在数值上就可以看成是形成该离子的原子或原子团的摩尔质量。[结论]如:C、H、O、S如:H2O、CO2、H2SO4如:Na+、SO42-[课堂练习]1molH2O的质量是g1molNaCl的质量是g1molNa+的质量是g1molS的质量是g1858.52332摩尔质量M:MH2O=18g/molMNaCl=58.5g/molMNa+=23g/molMS=32g/mol计算下列物质的摩尔质量Fe葡萄糖乳酸钠铵根C6H12O6CO32-CO2NH4+NaC3H5O3NaClCaNaOHMNaCl=58.5g/molMFe=56g/molMCa=40g/molMNaOH=40g/molMCO2=44g/mol1801121860表达式:MB=nm任何物质的摩尔质量M,若以g/mol作单位,在数值上等于该物质的相对化学式量。m=n·MB宏观物质的质量与微...