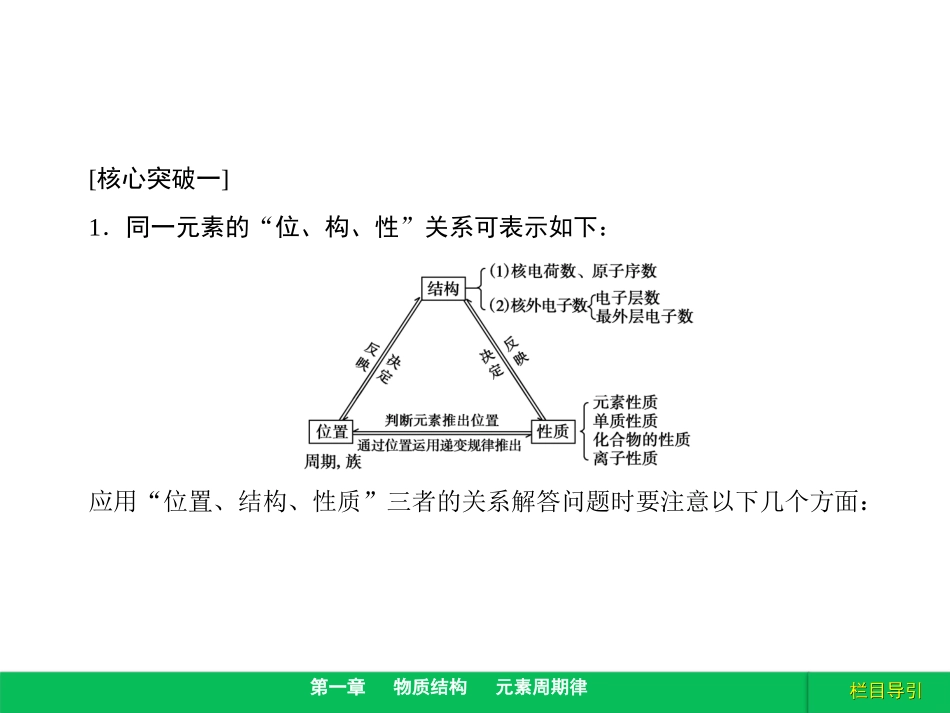
栏目导引栏目导引第一章物质结构元素周期律[核心突破一]1.同一元素的“位、构、性”关系可表示如下:应用“位置、结构、性质”三者的关系解答问题时要注意以下几个方面:栏目导引栏目导引第一章物质结构元素周期律(1)原子结构――→决定元素在周期表中的位置结构最外层电子数=主族序数电子层数=周期数位置(2)原子结构――→决定元素的化学性质①最外层电子数越少,电子层数越多→越易失电子,单质的还原性越强
②最外层电子数越多,电子层数越少→越易得电子,单质的氧化性越强
栏目导引栏目导引第一章物质结构元素周期律(3)元素在周期表中的位置――→体现或推测原子结构和元素性质同周期:[从左到右位置]――――――――――――――→最外层电子数递增结构非金属性增强,金属性减弱性质同主族:[从上到下位置]――――――――――――――→电子层数递增结构金属性增强,非金属性减弱性质(4)元素“位、构、性”规律中的特例①绝大多数原子的原子核是由质子和中子构成的,只有氕(11H)无中子
②元素周期表中的周期一般都是从金属元素开始,但第一周期例外,是从氢元素开始的
栏目导引栏目导引第一章物质结构元素周期律③所有元素中,碳元素形成的化合物种类最多
④非金属单质一般不导电,但石墨导电,晶体硅是半导体
⑤氟无正价,氧无最高正价;在Na2O2中氧显-1价,在NaH中氢显-1价
警示:(1)只有主族元素的最外层电子数等于主族序数
(2)难得电子的原子不一定易失电子,如稀有气体原子
栏目导引栏目导引第一章物质结构元素周期律(5)推断陌生元素性质时要从以下三个角度分析①与同周期前、后元素相比较,依据同周期元素性质的递变规律推测元素的性质
②与同主族上、下元素相比较,依据同主族元素性质的递变规律推测元素的性质
③比较不同周期、不同主族元素的性质时,可借助“三角”规律进行推断