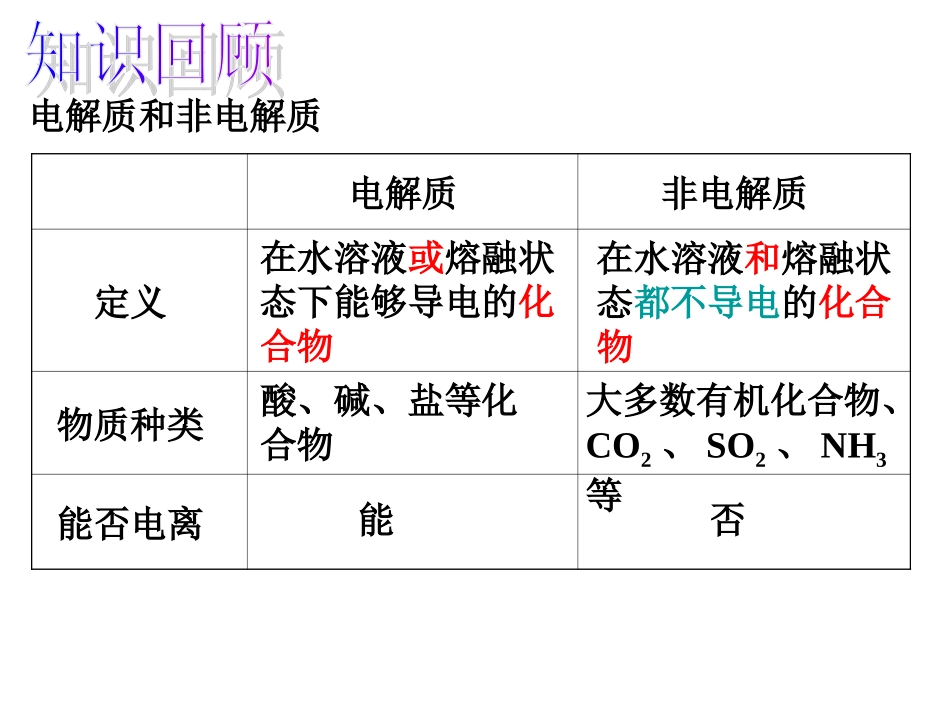
电解质和非电解质电解质非电解质定义物质种类能否电离在水溶液或熔融状态下能够导电的化合物在水溶液和熔融状态都不导电的化合物酸、碱、盐等化合物大多数有机化合物、CO2、SO2、NH3等能否根据定义,判断下列说法是否正确
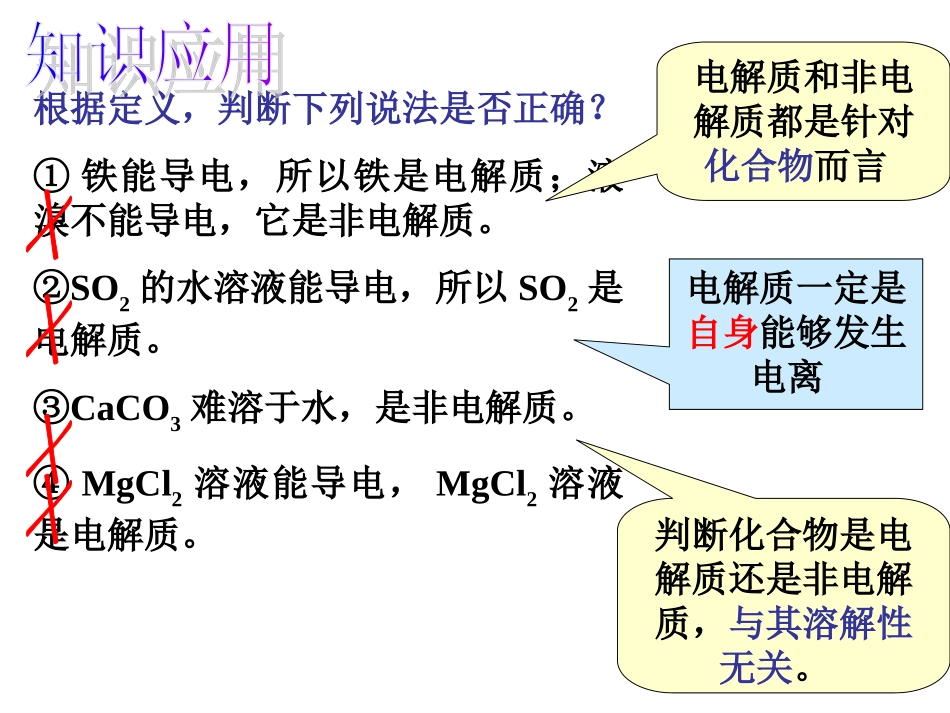
①铁能导电,所以铁是电解质;液溴不能导电,它是非电解质
②SO2的水溶液能导电,所以SO2是电解质
③CaCO3难溶于水,是非电解质
④MgCl2溶液能导电,MgCl2溶液是电解质
电解质和非电解质都是针对化合物而言电解质一定是自身能够发生电离判断化合物是电解质还是非电解质,与其溶解性无关
[活动与探究]比较相同条件下,浓度为0
5mol/L的醋酸、盐酸、食盐水、NaOH溶液、氨水、蒸馏水的导电能力(1)实验现象:(2)实验结论:思考:电解质的导电能力是否一致呢
思考:电解质的导电能力是否一致呢
盐酸、食盐水、NaOH溶液灯泡较亮;醋酸、氨水灯泡较暗;蒸馏水不亮
相同物质的量浓度盐酸、食盐水、NaOH溶液导电能力强,醋酸、氨水、蒸馏水导电能力弱H2OH+Cl-H2OCH3COOHH+CH3COO-盐酸溶液醋酸溶液HCl在水中全部电离CH3COOH在水中部分电离强酸强碱大部分盐活泼金属氧化物弱酸弱碱水电解质强电解质弱电解质是否完全电离一、强电解质和弱电解质强电解质——在水溶液中全部电离
弱电解质——在水溶液中部分电离
分类下列物质属于强电解质的是(),属于弱电解质的是(),属于非电解质的是(),能够导电的是()
①铜②一水合氨③氯化钠固体④硝酸钾溶液⑤碳酸钙⑥二氧化碳⑦蔗糖⑧冰醋酸⑨液态KNO3⑩液态HCl③⑤⑨⑩②⑧⑥⑦①④⑨3
电离和电离方程式⑴电离电解质在水溶液中或熔融状态下离解出自由移动的离子的过程
⑵电离方程式:[思考]试写出H2CO3,HClO,碳酸氢钠的电离方程式
例如:CH3COOHCH3COO-+H+二、离子反应[思考]下列反应能发生