第三章水溶液中的离子平衡第二节水的电离和溶液的酸碱性+++-探究实验精确的纯水导电实验现象:指针摆动不亮HH22OO++HH22OHOH33OO++++OHOH--HH22OO++HH22OHOH33OO++++OHOH--HH22OHOH++++OHOH--HH22OHOH++++OHOH--灵敏电流计灯泡结论:水是电解质能发生电离极弱微弱实验测定:纯水中25℃1L水中只有1×10-7mol水发生了电离25°C55
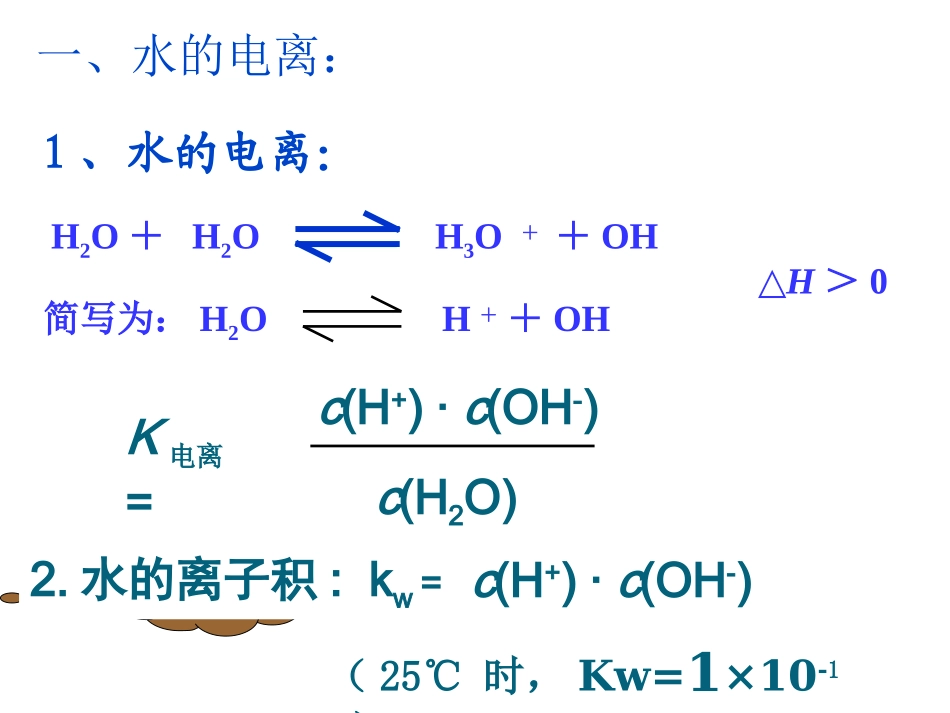
6×107个水分子才有1个电离一、水的电离:H2O+H2OH3O++OH-简写为:H2OH++OH-1、水的电离:△H>0K电离=c(H+)·c(OH-)c(H2O)c(H+)·c(OH-)c(H2O)·K电离=为常数2
水的离子积:kw=(25℃时,Kw=1×10-14)对常温下的纯水进行下列操作,完成下表:酸碱性水的电离平衡移动方向C(H+)C(OH-)c(H+)与c(OH-)大小关系Kw变化加热加HCl加NaOH中性→↑↑=↑酸性←↑↓>不变碱性←↓↑<不变中性不移动不变不变=不变加NaCl讨论:分析下表中的数据温度0℃20℃25℃50℃100℃Kw1
14×10-156
81×10-151×10-145
47×10-141×10-12讨论:根据前面所学知识,水的电离会受什么外界条件影响
水的离子积又如何改变
3、影响水的电离平衡的因素:(2)酸、碱(2)酸、碱(1)温度(1)温度(3)盐(3)盐升温促进水的电离加入酸或碱,抑制水的电离(第三节详细介绍)(第三节详细介绍)KKWW不变不变KKWW增大增大c(H+)水=c(OH-)水<1×10-7mol/Lc(H+)水=c(OH-)水<1×10-7mol/L常温下(25℃),任何稀的水溶液中总满足:Kw=C(H+)×C(OH-)=1×10-14注意:②任何水溶液中(不论是在中性溶液还是在酸、碱性溶液),H+