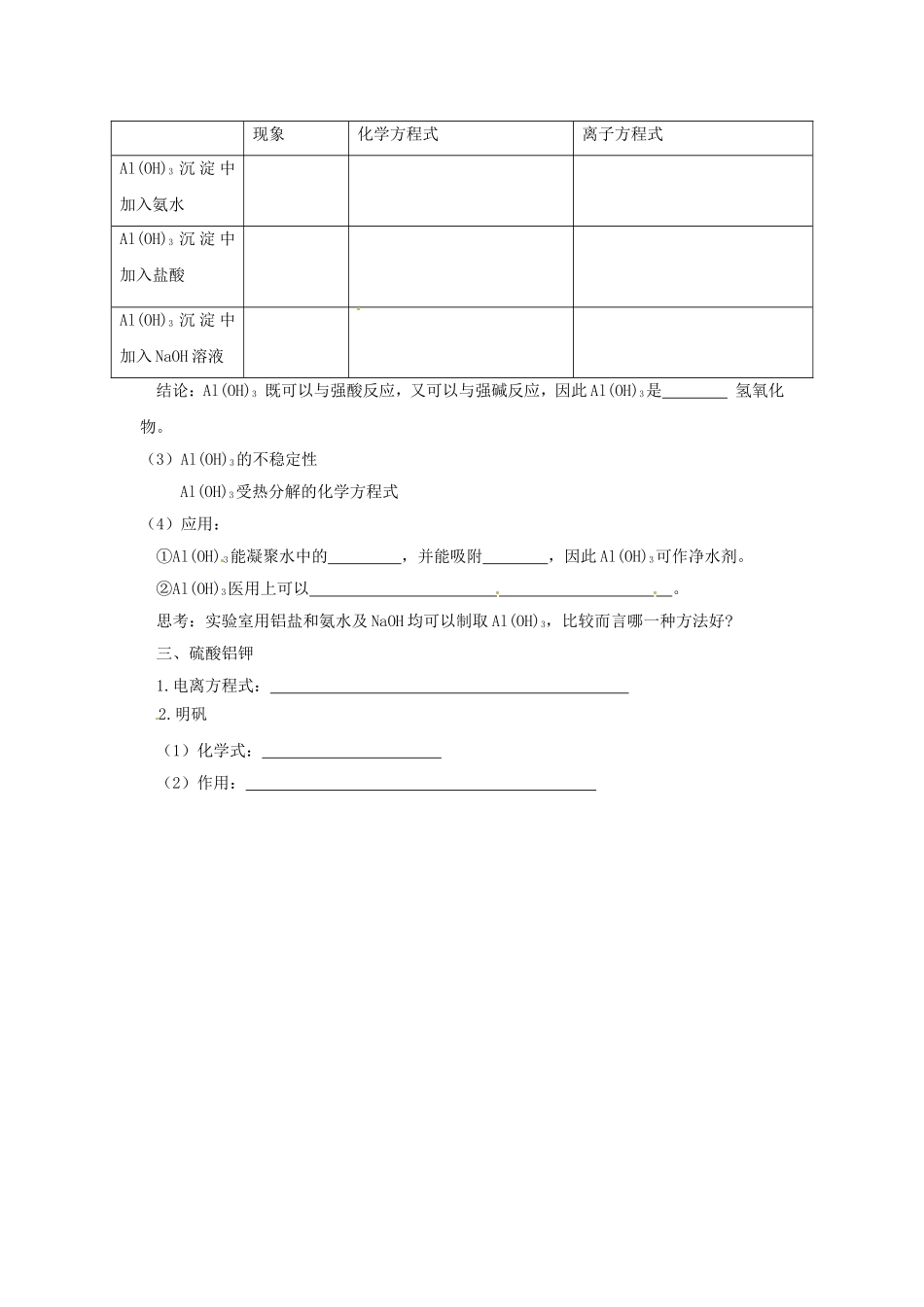
整理:***【学习目标】1.掌握Al2O3、Al(OH)3的两性2、掌握Al(OH)3的制备方法3、了解明矾的组成和用途。【学习重点】1.Al2O3、Al(OH)3的两性2.Al(OH)3的制备方法【预备知识】①②③酸性氧化物:能和反应只生成盐和水的氧化物。写出NaOH溶液和少量CO2反应的化学方程式:碱性氧化物:能和反应只生成盐和水的氧化物写出Na2O和盐酸反应的化学方程式:【基础知识】一.氧化铝1.物理性质:Al2O3溶于水;熔点,硬度,能有效地保护内层金属。2.用途:氧化铝是的原料,也是一种较好的材料。3.化学性质:写出下列反应的化学方程式,并改成离子方程式。Al2O3和HCl,Al2O3和NaOH,结论:Al2O3既可以与酸反应,又可以与强碱反应,因此Al2O3是氧化物。两性氧化物:既能和反应生成盐和水,又可以和反应生成盐和水的氧化物。二、氢氧化铝(1)Al(OH)3生成实验:向试管中加入0.5mol/LAl2(SO4)3溶液,滴加氨水。现象:生成色状沉淀。化学反应方程式:。离子方程式:.(2)Al(OH)3的两性填写实验表格AlCl3AlAl2O3NaAlO2①②③现象化学方程式离子方程式Al(OH)3沉淀中加入氨水Al(OH)3沉淀中加入盐酸Al(OH)3沉淀中加入NaOH溶液结论:Al(OH)3既可以与强酸反应,又可以与强碱反应,因此Al(OH)3是氢氧化物。(3)Al(OH)3的不稳定性Al(OH)3受热分解的化学方程式(4)应用:①Al(OH)3能凝聚水中的,并能吸附,因此Al(OH)3可作净水剂。②Al(OH)3医用上可以。思考:实验室用铝盐和氨水及NaOH均可以制取Al(OH)3,比较而言哪一种方法好?三、硫酸铝钾1.电离方程式:2.明矾(1)化学式:(2)作用: