第三讲化学反应速率化学平衡3
1化学反应速率(一)
化学反应速率及表示方法1
化学反应速率指单位时间内反应物或生成物浓度的变化,通常用mol/L•s或mol/L•min表示
同一反应的反应速率可用不同反应物或生成物的浓度变化来表示
反应A2+3B22AB3的反应速率可以用下列各种不同物质的浓度变化来表示,其中反应速率最快的是()
(A)v(A2)=0
4mol/L•min(B)v(B2)=0
6mol/L•min(C)v(AB3)=0
5mol/L•min(D)v(B2)=1
0mol/L•min比较化学反应速率应注意的问题:2
瞬时速率和平均速率(二)影响化学反应速率的因素化学反应速率首先取决于反应物本身的性质(内因),另外浓度、压强、温度、催化剂等外界条件(外因)也影响化学反应速率
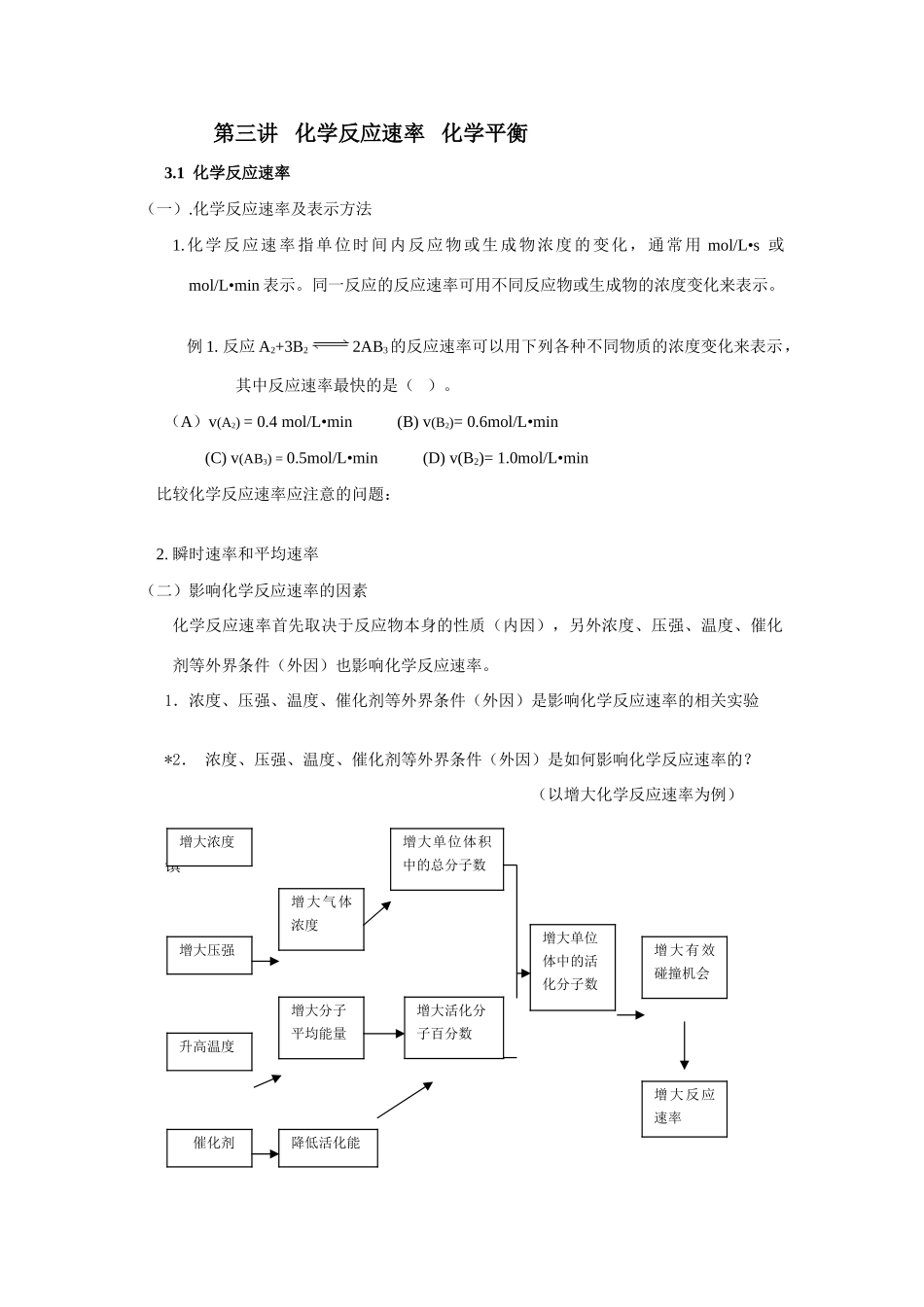
1.浓度、压强、温度、催化剂等外界条件(外因)是影响化学反应速率的相关实验*2.浓度、压强、温度、催化剂等外界条件(外因)是如何影响化学反应速率的
(以增大化学反应速率为例)镇增大浓度增大压强升高温度催化剂增大气体浓度增大分子平均能量增大单位体积中的总分子数增大活化分子百分数增大单位体中的活化分子数增大有效碰撞机会增大反应速率降低活化能*3.催化剂的特性例1.化学反应A+BC+D,在以下各组不同条件下进行时,反应速率最大的一组是()(A)常温下20ml含A和B各0
001mol的溶液(B)常温下50ml含A和B各0
01mol的溶液(C)常温下,将0
3mol/L的A、B溶液各10ml混合(D)标准状况下,将0
3mol/L的A、B溶液各20ml混合2.Fe3+和I-在水溶液中的反应如下:2Fe3++2I-→2Fe2++I2,该反应的反应速率和Fe3+、I-的浓度关系如下:V=R[c(I-)]m[c(Fe3+)]n(R为常数)c(I-)(mol/L)C(Fe3+)(mol/L)V[mo