第二节构成物质的基本微粒(第二课时原子的构成)学案[教学目标]1、了解原子、原子核的构成
2、知道原子质量的表示方法──相对原子质量
会查相对原子质量表
3、知道原子中的一些数量关系
4、培养善于想像、勇于探索、敢于创新的精神;体验探究学习的过程,树立学习的信心
重点原子、原子核的构成难点原子、原子核的构成[温故知新]:(口述)1、什么是分子
2、什么是原子
3、分子和原子的最大区别是什么
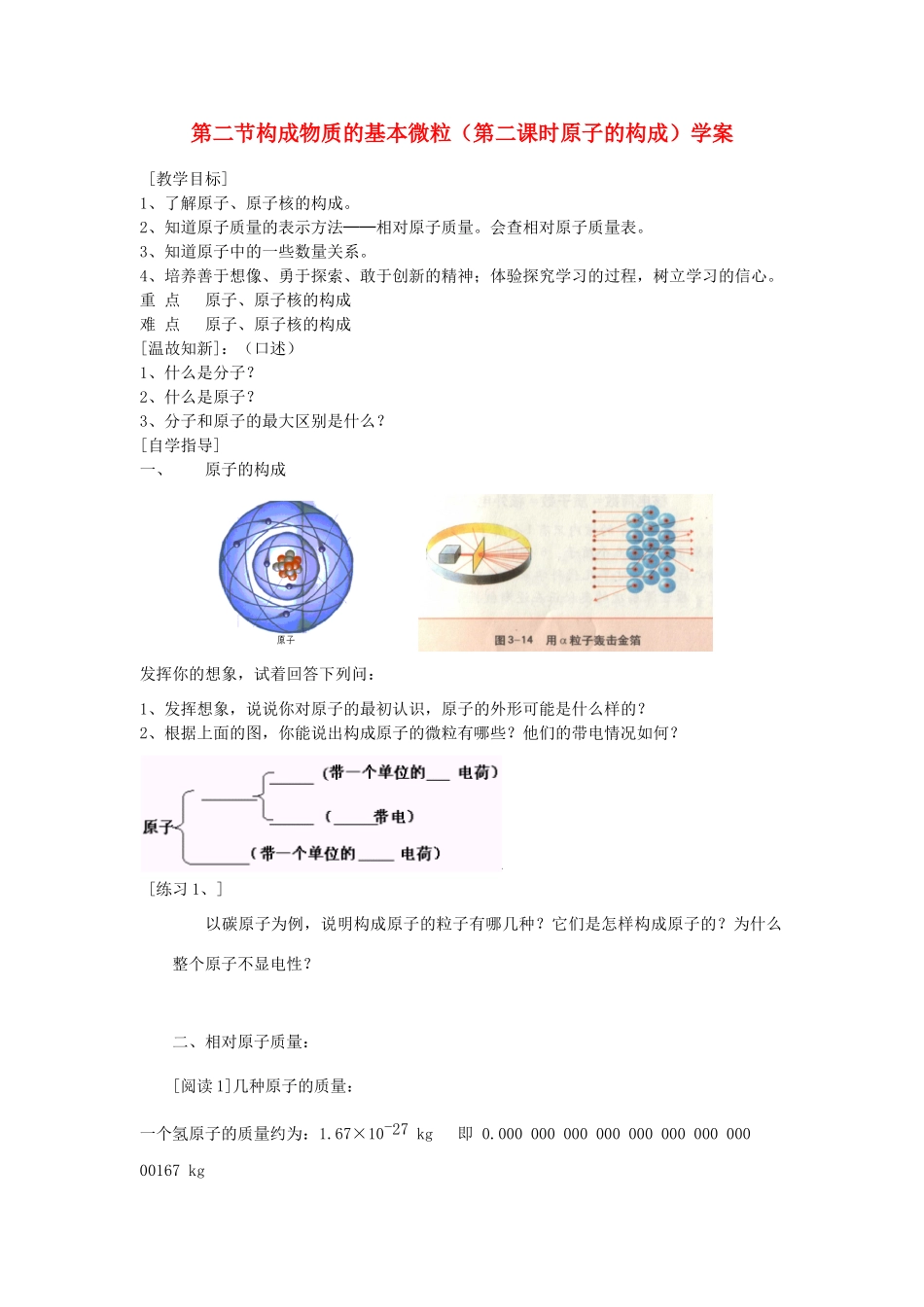
[自学指导]一、原子的构成发挥你的想象,试着回答下列问:1、发挥想象,说说你对原子的最初认识,原子的外形可能是什么样的
2、根据上面的图,你能说出构成原子的微粒有哪些
他们的带电情况如何
[练习1、]以碳原子为例,说明构成原子的粒子有哪几种
它们是怎样构成原子的
为什么整个原子不显电性
二、相对原子质量:[阅读1]几种原子的质量:一个氢原子的质量约为:1
67×10-27kg即0
00000000000000000000000000167kg一个碳原子的质量约为:1
993×10-26kg即0
00000000000000000000000001993kg一个氧原子的质量约为:2
657×10-26kg即0
00000000000000000000000002657kg一个铁原子的质量约为:9
288×10-26kg即0
00000000000000000000000009288kg[思考1]看上面几种原子的质量,你认为为什么要引进相对原子质量
[阅读2][思考2]看课本68页和上面的图,写出相对原子质量的计算公式
相对原子质量=[练习]2、从元素周期表中查阅下列元素的相对原子质量:Na=O=Mg=3、氢的相对原子质量为()A
67×10-27kg4、若标准碳原子的质量为m,某种原子的相对质量为n,求这种原子的实际质量三、原子中的几个数量关系[思考3]观察下表