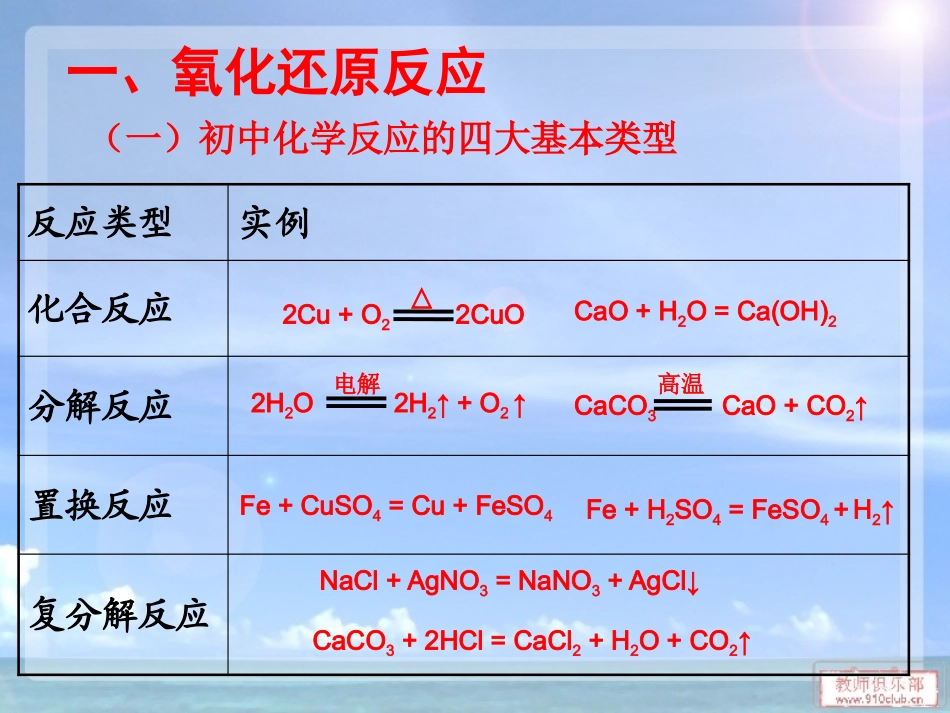
第一课时一、氧化还原反应(一)初中化学反应的四大基本类型反应类型实例化合反应分解反应置换反应复分解反应2Cu+O22CuO△CaO+H2O=Ca(OH)22H2O2H2↑+O2↑电解CaCO3CaO+CO2↑高温Fe+CuSO4=Cu+FeSO4Fe+H2SO4=FeSO4+H2↑NaCl+AgNO3=NaNO3+AgCl↓CaCO3+2HCl=CaCl2+H2O+CO2↑优点:例:Fe2O3+3CO2Fe+3CO2△根据反应物和生成物的类别和种类多少分类,直观、易懂、易判断
缺点:①不能反映化学反应的本质②不能包含所有化学反应
氧化还原反应1、从得失氧的角度进行分类氧化反应还原反应物质得到氧的反应物质失去氧的反应2CuO+C=2Cu+CO2↑△失氧,被还原(发生还原反应)得氧,被氧化(发生氧化反应)氧化反应——得氧;还原反应——失氧
开动脑筋:氧化反应和还原反应是分别独立进行的吗
从整体上看,氧化反应和还原反应同时发生,不能分开,有氧化必有还原
这样的反应称为氧化还原反应
氧化还原反应概念一种物质被氧化,另一种物质同时被还原的反应在Mg+O2=2MgO反应中,对于镁来说,Mg——MgO的反应是氧化反应,那么有还原反应存在吗
【思考】氧化反应和还原反应同时存在,同时发生,两者既对立,又统一,不能截然分开
因此2Mg+O2=2MgO是氧化反应的说法是片面的,应该是氧化还原反应
【小结】从得失氧的角度分析N2+3H2=2NH3、2Na+Cl2=2NaCl、H2+Cl2=2HCl三个反应是否属于氧化还原反应
上面的三个反应中虽无氧的得失,但属于氧化还原反应
因此,初中所学的概念有一定的局限性,有待于进一步的研究和学习
那么氧化还原反应的本质是什么呢
【思考】2CuO+C=2Cu+CO2↑△化合价降低,被还原化合价升高,被氧化+200+42、从元素化合价的角度分析下面反应【练习】F