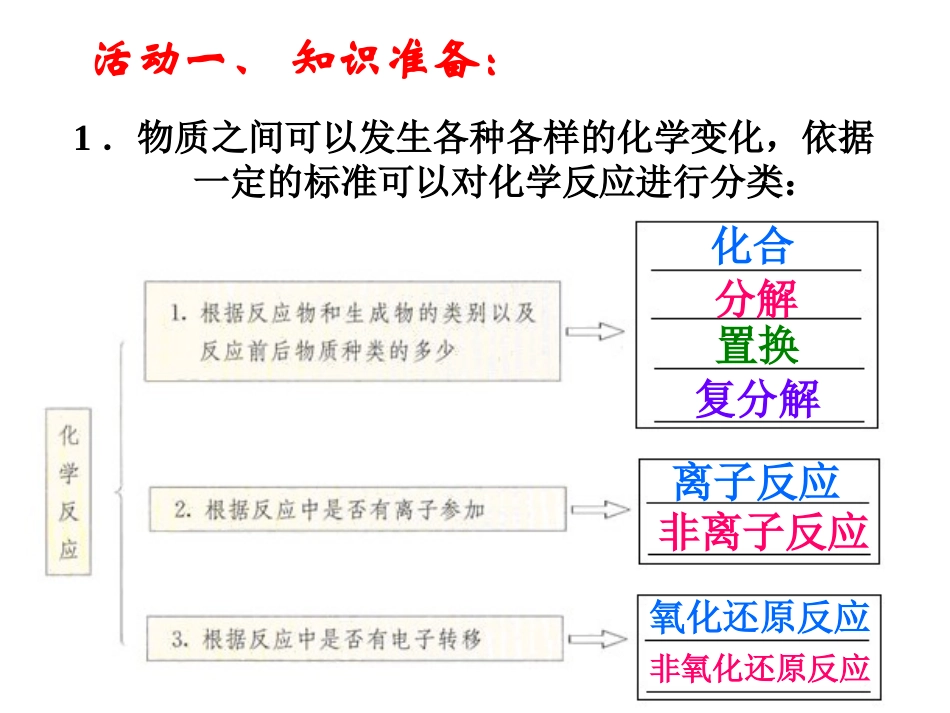
§2-3氧化还原反应课题一:氧化还原反应的概念和本质活动一、知识准备:1.物质之间可以发生各种各样的化学变化,依据一定的标准可以对化学反应进行分类:化合分解复分解置换离子反应非离子反应氧化还原反应非氧化还原反应2.2CuO+C2Cu+CO2反应属于基本反应类型;若从氧化还原角度来分析CuO发生反应,H2发生反应
氧化反应和还原反应(能、不能)分别独立进行
高温置换还原氧化不能C得氧:氧化失氧:还原表面现象,认识肤浅因为有的反应没有出现氧元素,却属于氧化还原反应
经典的氧化还原反应:H2+CuOCu+H2OΔ得氧失氧活动二、从化合价升降角度来分析:2CuO+C2Cu+CO2高温氧化还原反应的定义:____________________________________凡是有元素化合价升降的化学反应
氧化还原反应的特征及判断依据:化合价升降非氧化还原反应:凡是没有元素化合价升降的化学反应
NaCl,HClO,KClO3,KI,CuS,Cu2O,NH3,N2H4,NO2,NH4NO3,Na2SO3,H2S,Na2O,Na2O2,KMnO4,MnO2,MnSO4,CaH2,FeCl2,Fe2O3
练习1、写出下列常见物质中加点元素的化合价
-1+1+5-1+2+1-3-2+4-3+5+4-2-2-1+7+4+2-1+2+3练习2、从化合价升降的角度判断下列反应属于氧化还原反应的是
①NH4HCO3NH3↑+CO2↑+H2O↑②CaCl2+Na2CO3=CaCO3↓+2NaCl③2Na+2H2O=2NaOH+H2↑④2Na+Cl22NaClΔ点燃③④练习3、反应2FeCl3+2KI=2FeCl2+2KCl+I2,其中________元素化合价升高,则该元素被________,_____元素化合价降低,则该元素被________;_______