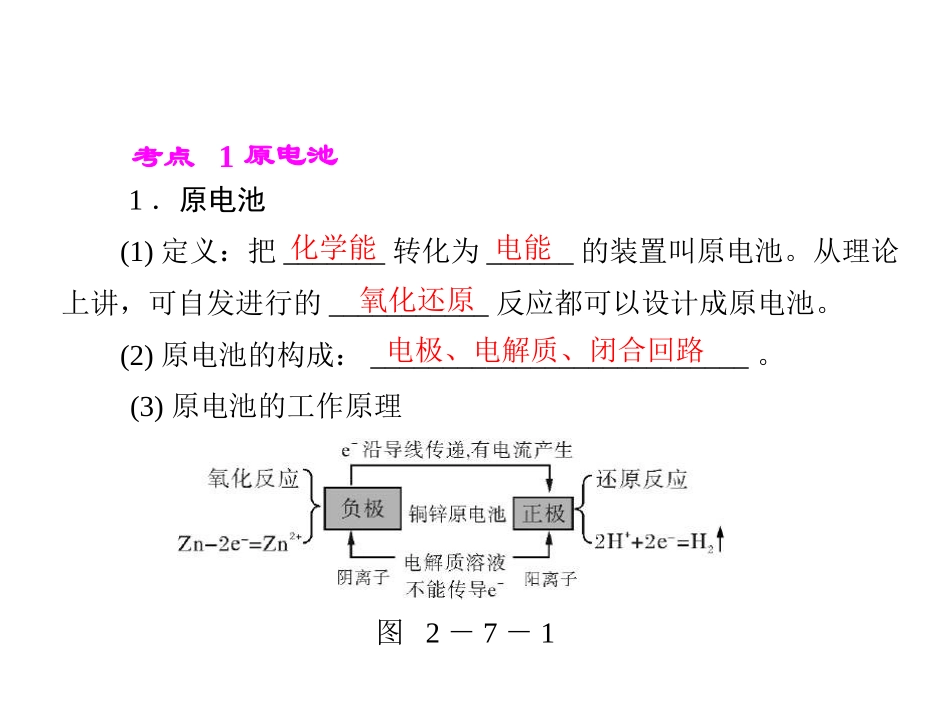
第七单元(第22、23讲)电化学基本考点1原电池1.原电池化学能电能氧化还原(1)定义:把_______转化为______的装置叫原电池
从理论上讲,可自发进行的___________反应都可以设计成原电池
(2)原电池的构成:__________________________
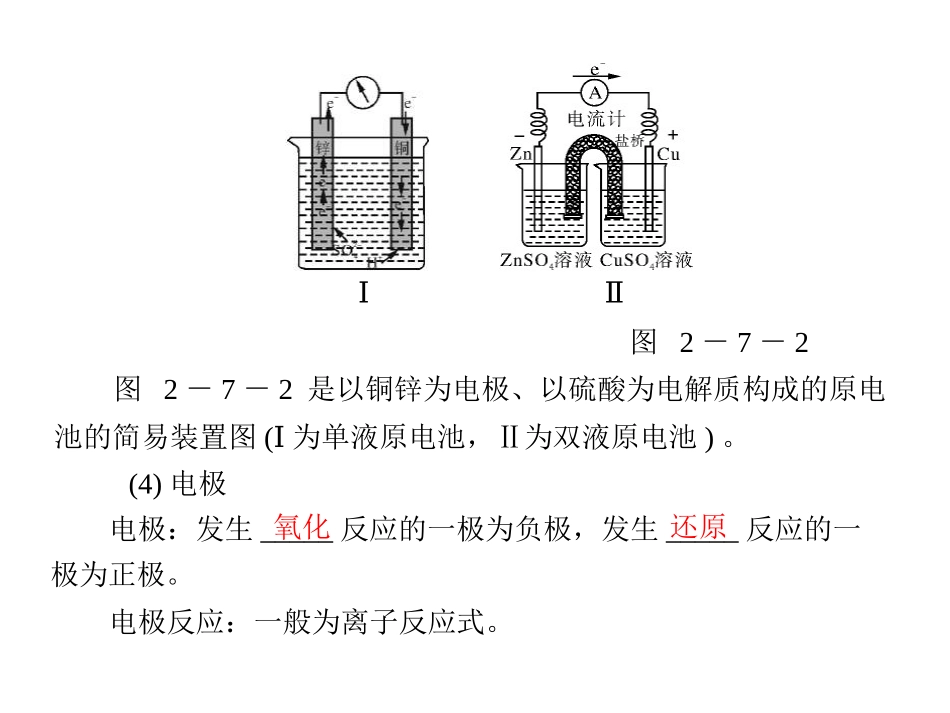
(3)原电池的工作原理电极、电解质、闭合回路图2-7-1ⅠⅡ图2-7-2图2-7-2是以铜锌为电极、以硫酸为电解质构成的原电池的简易装置图(Ⅰ为单液原电池,Ⅱ为双液原电池)
(4)电极氧化还原电极:发生_____反应的一极为负极,发生_____反应的一极为正极
电极反应:一般为离子反应式
2.化学电源干电池可充电电池(1)一次电池:也就是______,如锌锰干电池、银锌电池等
(2)二次电池:又叫__________
如铅蓄电池、现在广泛使用的手机电池、便携式计算机用电池等
(3)燃料电池:连续地将燃料和氧化剂的化学能直接转换成电能的化学电池
电极本身不包含活性物质,只是催化转化元件,本身不发生氧化还原反应
如氢氧燃料电池等
除氢气外,还有一些燃料如肼、甲醇、氨、煤气等都可作燃料电池的燃料
燃料电池的能量转化率远高于普通的燃烧过程,有利于节约能源
(4)废旧电池要回收,既保护环境又节约资源
3.电极及应式的书写(1)一般电极反应式的书写(普通原电池)负极材料:____,正极材料:_______
(2)复杂电极反应式的书写(燃料电池)复杂电极反应式较简单一极的电极反应式如①碱性锌锰干电池②铅蓄电池PbPbO2=总反应式-正极反应:____________________________________;负极反应:__________________________;2MnO2+2H2O+2e-===2MnOOH+2OH-Zn+2OH--2e-===Zn(OH)2放电时负极反应:Pb+SO2-4-2e