活动导学案选修四化学平衡常数【2013年考纲要求】1、理解化学平衡常数的含义,能够利用化学平衡常数进行简单的计算
2、了解弱电解质在水溶液中的电离平衡
了解水的电离及离子积常数3、了解难溶电解质在水中存在沉淀溶解平衡
了解溶度积的含义
【学习目标】1、理解化学平衡常数K、电离平衡常数(Ka、Kb、Kw)、溶度积常数Ksp的含义,会书写相应的表达式
2、知道平衡常数的应用【活动方案】活动一完成基础回顾11、对于可逆反应:aA(g)+bB(g)⇌cC(g)+dD(g),其中a、b、c、d分别表示化学方程式中各反应物和生成物的化学计量数
当在一定温度下达到化学平衡时,这个反应的平衡常数表达式为:
2、如CH3COOHCH⇌3COO-+H+,电离平衡常数
3、Kw的数学表达式是Kw=
4、Fe(OH)3(s)Fe⇌3+(aq)+3OH-(aq),溶度积常数思考:在相同温度下,对于同一个可逆反应,若书写方式不一样,平衡常数表达式是否一样
以合成氨反应为例进行说明
活动导学案K1、K2、K3间的相互关系为
活动二完成基础回顾2
思考平衡常数的影响因素
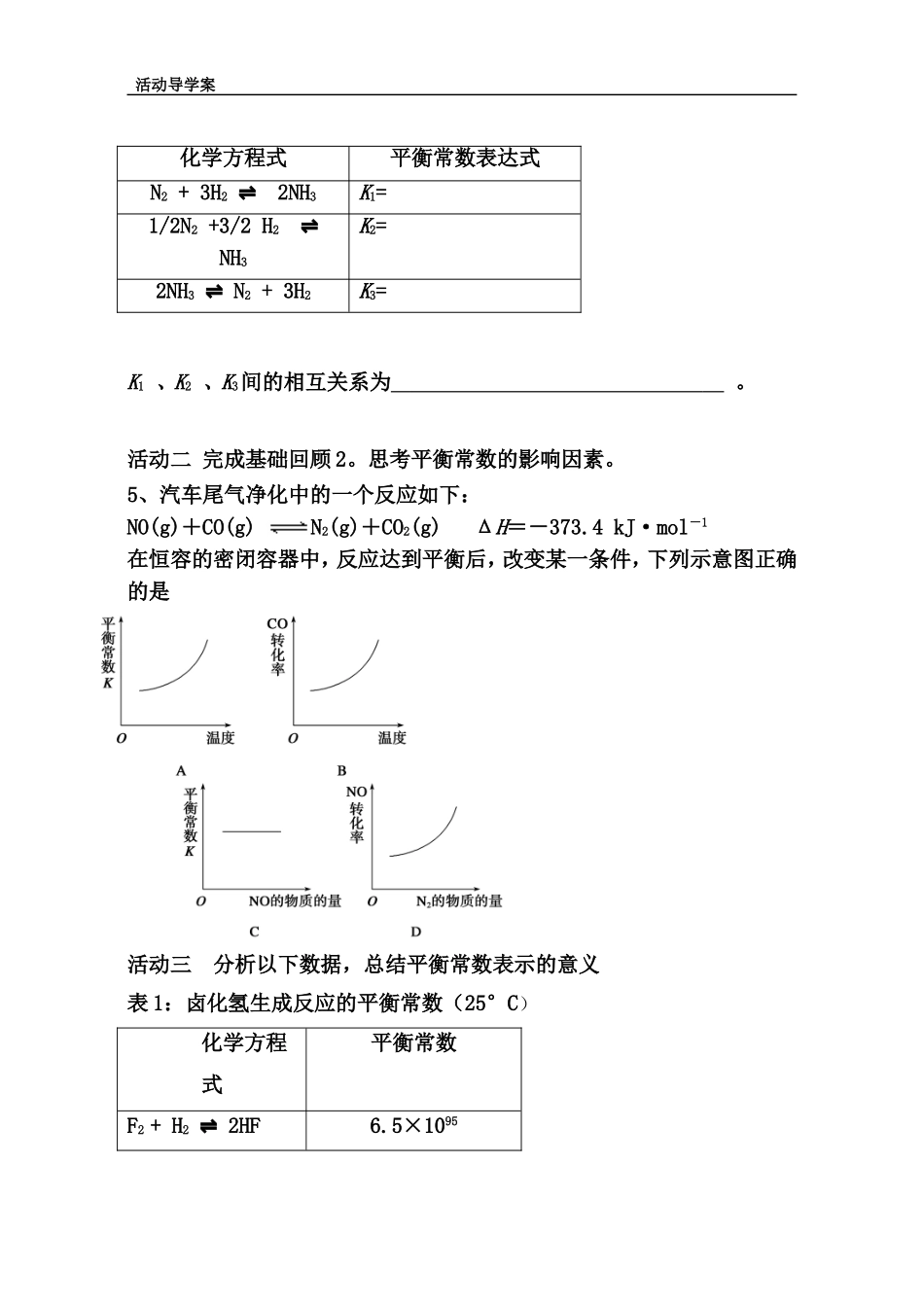
5、汽车尾气净化中的一个反应如下:NO(g)+CO(g)N2(g)+CO2(g)ΔH=-373
4kJ·mol-1在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意图正确的是活动三分析以下数据,总结平衡常数表示的意义表1:卤化氢生成反应的平衡常数(25°C)化学方程式平衡常数F2+H22HF⇌6
5×1095化学方程式平衡常数表达式N2+3H22NH⇌3K1=1/2N2+3/2H2⇌NH3K2=2NH3N⇌2+3H2K3=活动导学案Cl2+H22HCl⇌2
57×1033Br2+H22HBr⇌1
91×1019I2+H22HI⇌8
67×102表2:常见难溶电解质的溶度积常数和溶解度(25°C)难溶物Ksp溶解度/g难溶物Ksp溶