1.已知:N2(g)+3H2(g)2NH3(g)ΔH=-92
4kJ·mol-1
(1)在500℃、2
02×107Pa和铁催化条件下2L密闭容器中充入1molN2和3molH2,10min时达到平衡,有0
2molNH3生成,则10min内用氢气表示的该反应的平均速率v(H2)为,H2的转化率为__________
(2)充分反应后,放出的热量______(填“”“=”)92
4kJ,理由是
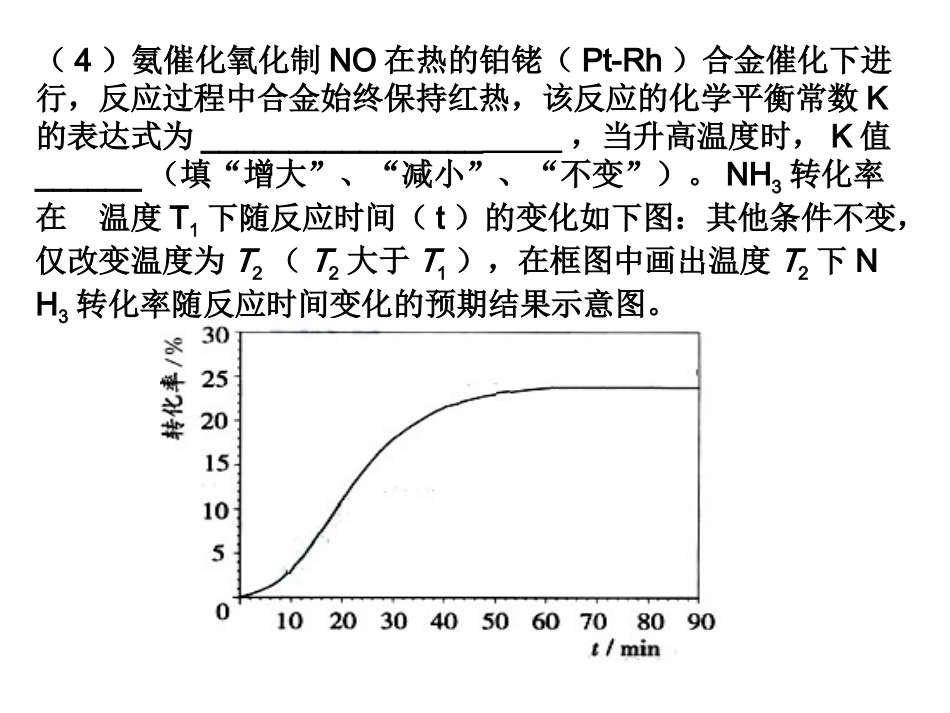
(3)为有效提高氢气的转化率,实际生产中宜采取的措施有____________A.降低温度B.不断补充氮气C.恒容下充入He来增大压强D.升高温度E.原料气不断循环F.及时移出氨(4)氨催化氧化制NO在热的铂铑(Pt-Rh)合金催化下进行,反应过程中合金始终保持红热,该反应的化学平衡常数K的表达式为________________,当升高温度时,K值______(填“增大”、“减小”、“不变”)
NH3转化率在温度T1下随反应时间(t)的变化如下图:其他条件不变,仅改变温度为T2(T2大于T1),在框图中画出温度T2下NH3转化率随反应时间变化的预期结果示意图
2:超音速飞机在平流层飞行时,尾气中的会破坏臭氧层
科学家正在研究利用催化技术将尾气中的和转变成和,化学方程式如下:为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:(1)在上述条件下反应能够自发进行,则反应的0(填写“>”、“