第二节离子反应的本质【提问】离子反应的本质及离子反应发生的条件是什么
离子反应发生的条件除了发生复分解反应即生成难溶、难电离及挥发性物质外,还有常见的一类反应就是氧化还原反应
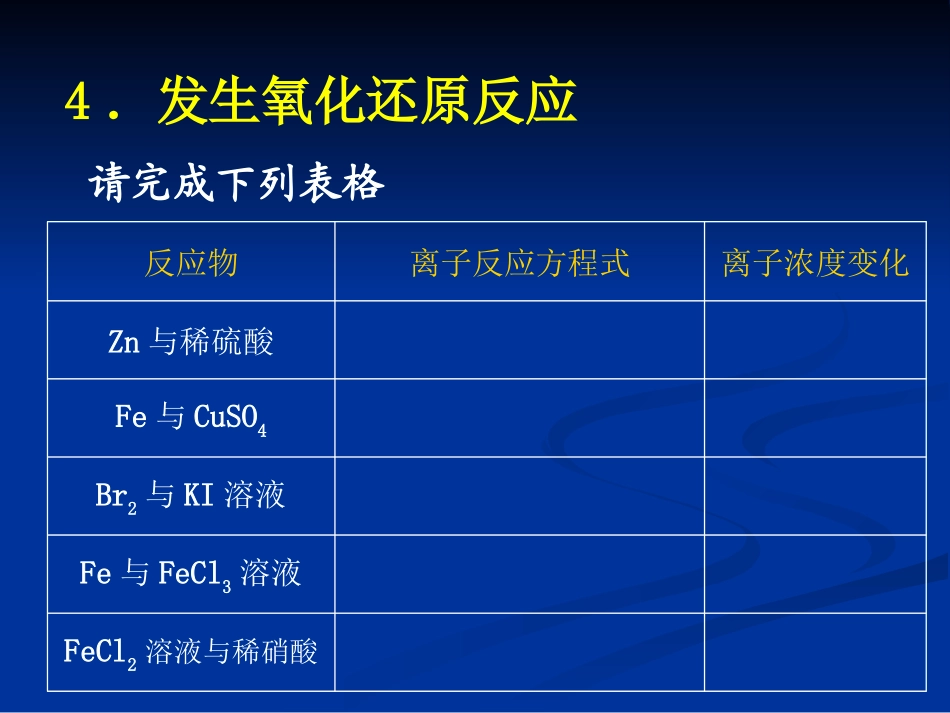
4.发生氧化还原反应FeCl2溶液与稀硝酸Fe与FeCl3溶液Br2与KI溶液Fe与CuSO4Zn与稀硫酸离子浓度变化离子反应方程式反应物请完成下列表格1.氧化还原反应中离子浓度变化的特点:如果反应物的某些离子浓度减小,也能发生离子反应,这时生成物中有离子时,其离子浓度升高,如上表中,c(H+)降低,c(Zn2+)升高
2.氧化还原反应离子方程式的配平,不仅要符合质量守恒定律,而且氧化剂和还原剂得失电子总数也应相等,同时满足电荷守恒
【讨论】根据离子反应发生的条件,以举例方式小结,哪些离子在溶液中不能大量共存
三、离子能否共存问题凡是在溶液中能发生反应的离子均不能大量共存
常见的不能共存的离子有:(1)生成难溶物:Ba2+与CO32-、SO42-;Ag+与Cl-、Br-、I-;Fe3+与OH-等
(2)生成气体或挥发性物质:NH4+与OH-;H+与CO32-、HCO3-、SO32-等
(3)生成难电离的物质:H+与OH-、CH3COO-、F-等
(4)发生氧化还原反应:Fe3+与I-、S2-;ClO-与S2-等
离子组不能共存规律离子组不能共存规律能生成难溶物能生成难溶物能生成气体能生成气体能生成难电离物能生成难电离物能发生氧化还原反应的能发生氧化还原反应的能发生双水解的能发生双水解的弱酸酸式根离子不能与弱酸酸式根离子不能与HH++、、OHOH--共存共存在题目中提示酸性溶液(在题目中提示酸性溶液(pHpH7)应在各选答案中均加入)应在各选答案中均加入HH++或或OOHH--考虑考虑在题目中告知是无色溶液,应在各待选答案在题目中告知是无色溶液,应在各待选答案中排除具有颜色的离子